题目内容
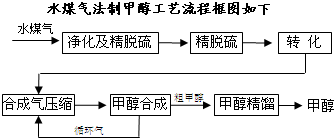 将煤气化转化成合成气,然后通过一碳化工路线合成各种油品和石化产品是一碳化工的极为重要的领域,具有广阔的前景,在未来相当一段时期将成为一碳化工的主要领域.
将煤气化转化成合成气,然后通过一碳化工路线合成各种油品和石化产品是一碳化工的极为重要的领域,具有广阔的前景,在未来相当一段时期将成为一碳化工的主要领域.除去水蒸气后的水煤气含55~59%的H2,15~18%的CO,11~13%的CO2,少量的H2S、CH4,除去H2S后,可采用催化或非催化转化技术,将CH4转化成CO,得到CO、CO2和H2的混合气体,是理想的合成甲醇原料气,即可进行甲醇合成.
(1)制水煤气的主要化学反应方程式为:C(s)+H2O(g)
| 高温 |
①此反应的化学平衡常数表达式为
②下列能增大碳的转化率的措施是
A.加入C(s) B.加入H2O(g) C.升高温度 D.增大压强
(2)将CH4转化成CO,工业上常采用催化转化技术,其反应原理为:
CH4(g)+
| 3 |
| 2 |
①X在T1℃时催化效率最高,能使正反应速率加快约3×105倍;
②Y在T2℃时催化效率最高,能使正反应速率加快约3×105倍;
③Z在T3℃时催化效率最高,能使逆反应速率加快约1×106倍;
已知:T1>T2>T3,根据上述信息,你认为在生产中应该选择的适宜催化剂是
(3)合成气经压缩升温后进入10m3甲醇合成塔,在催化剂作用下,进行甲醇合成,主要反应如下:
2H2(g)+CO(g)?CH3OH(g);△H=-90.8kJ?mol-1,T4℃下此反应的平衡常数为160.此温度下,在密闭容器中加入CO、H2,反应到某时刻测得各组分的浓度如下:
| 物质 | H2 | CO | CH3OH |
| 浓度/(mol?L-1) | 0.2 | 0.1 | 0.4 |
②若加入CO、H2后,在T5℃反应10min达到平衡,c(H2)=0.4mol?L-1,则该时间内反应速率v(CH3OH)=
(4)生产过程中,合成气要进行循环,其目的是
考点:化学平衡常数的含义,化学平衡建立的过程,化学平衡的影响因素
专题:化学平衡专题
分析:(1)①化学平衡常数,是指在一定温度下,可逆反应达到平衡时各生成物浓度的化学计量数次幂的乘积除以各反应物浓度的化学计量数次幂的乘积所得的比值,据此书写;
②增大碳的转化率,应采取措施使平衡向正反应移动,结合外界条件对平衡移动影响分析;
(2)该反应正反应为放热反应,应选择催化活性高、速度快、反应温度较低;
(3)①计算此时的浓度商Qc,与平衡常数比较,判断反应进行的方向,据此解答;
②依据图表数据计算起始量,结合三段式列式计算,根据甲氢气的浓度变化计算甲醇的浓度变化量,再根据v=
计算v(CH3OH);
(4)合成气进行循环,可以提高原料利用率.
②增大碳的转化率,应采取措施使平衡向正反应移动,结合外界条件对平衡移动影响分析;
(2)该反应正反应为放热反应,应选择催化活性高、速度快、反应温度较低;
(3)①计算此时的浓度商Qc,与平衡常数比较,判断反应进行的方向,据此解答;
②依据图表数据计算起始量,结合三段式列式计算,根据甲氢气的浓度变化计算甲醇的浓度变化量,再根据v=
| △c |
| △t |
(4)合成气进行循环,可以提高原料利用率.
解答:
解:(1)①C(s)+H2O(g)
CO(g)+H2(g)的平衡常数K=
,故答案为:
;
②A.加入固体C(s),不影响平衡移动,故A错误;
B.加入H2O(g),水蒸气的浓度增大,平衡向正反应方向移动,碳的转化率增大,故B正确;
C.正反应是吸热反应,升高温度平衡向正反应方向移动,碳的转化率增大,故C正确;
D.增大压强,平衡向逆反应方向移动,碳的转化率降低,故D错误;
故答案为:BC;
(2)该反应正反应为放热反应,应选择催化活性高、速度快、反应温度较低,故选择Z,
故答案为:Z;催化活性高、速度快、反应温度较低;
(3)①由表中数据可知,10min时氢气的浓度为0.2mol/L、CO的浓度为0.1mol/L、甲醇的浓度为0.4mol/L,则此时的浓度商Qc=
=100,小于平衡常数160,故反应向正反应方向进行,故V正>V逆,故答案为:>;
②依据图表计算起始量;
2H2(g)+CO(g)?CH3OH(g)
起始量(mol/L) 1 0.5 0
变化量(mol/L) 0.8 0.4 0.4
T4时(mol/L) 0.2 0.1 0.4
若加入CO、H2后,在T5℃反应10min达到平衡,c(H2)=0.4mol?L-1,由表中数据可知,l0min内氢气的浓度变化量为0.6mol/L,故甲醇的浓度变化量为0.3mol/L,故v(CH3OH)=
=0.03mol/(L?min),
故答案为:0.03;
(4)生产过程中,合成气要进行循环,这样可以提高原料利用率,故答案为:提高原料利用率(或提高产量、产率亦可).
| ||
| c(CH3OH) |
| c(CO)×c(H2) |
| c(CH3OH) |
| c(CO)×c(H2) |
②A.加入固体C(s),不影响平衡移动,故A错误;
B.加入H2O(g),水蒸气的浓度增大,平衡向正反应方向移动,碳的转化率增大,故B正确;
C.正反应是吸热反应,升高温度平衡向正反应方向移动,碳的转化率增大,故C正确;
D.增大压强,平衡向逆反应方向移动,碳的转化率降低,故D错误;
故答案为:BC;
(2)该反应正反应为放热反应,应选择催化活性高、速度快、反应温度较低,故选择Z,
故答案为:Z;催化活性高、速度快、反应温度较低;
(3)①由表中数据可知,10min时氢气的浓度为0.2mol/L、CO的浓度为0.1mol/L、甲醇的浓度为0.4mol/L,则此时的浓度商Qc=
| 0.4 |
| 0.22×0.1 |
②依据图表计算起始量;
2H2(g)+CO(g)?CH3OH(g)
起始量(mol/L) 1 0.5 0
变化量(mol/L) 0.8 0.4 0.4
T4时(mol/L) 0.2 0.1 0.4
若加入CO、H2后,在T5℃反应10min达到平衡,c(H2)=0.4mol?L-1,由表中数据可知,l0min内氢气的浓度变化量为0.6mol/L,故甲醇的浓度变化量为0.3mol/L,故v(CH3OH)=
| 0.3mol/L |
| 10min |
故答案为:0.03;
(4)生产过程中,合成气要进行循环,这样可以提高原料利用率,故答案为:提高原料利用率(或提高产量、产率亦可).
点评:本题考查化学平衡常数、化学平衡影响因素、反应速率计算、反应中能量变化等,难度中等,注意理解掌握平衡常数的用途.

练习册系列答案
相关题目
下列有关实验原理、方法和结论都正确的是( )
| A、向溴水中滴入植物油,振荡后,油层显无色,说明溴不溶于油脂 |
| B、向蛋白质溶液中加入硫酸铜溶液,将得到的沉淀分离出来,再加水可重新溶解 |
| C、pH都为3的酸HA和HB分别与足量Mg反应,HA放出的H2多,说明酸性HA<HB |
| D、淀粉在稀硫酸的作用下水解后,加入氢氧化钠使溶液呈碱性,再加入新制Cu(OH)2后加热,若有砖红色沉淀生成,则淀粉已经开始水解 |
常温下,将20mL 0.1mol/L的HCl溶液逐滴加入到20mL 0.1mol/L Na2C2O4溶液中.已知NaHC2O4溶液显酸性,关于反应混合溶液的下列判断不正确的是( )
| A、加水稀释时,溶液中c(OH-)增大,其余离子浓度均减小 | ||
B、
| ||
| C、c(Na+)>c(Cl-)>c(HC2O4-)>c(C2O42-)>c(H2C2O4) | ||
| D、c(Cl-)=c(HC2O4-)+2c(C2O42-)+c(HC2O4) |
能正确表示下列反应的离子方程式的是( )
A、用铜作电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| B、0.01mol/L NH4Al(SO4)2溶液与0.02 mol/L Ba(OH)2溶液等体积混合:A13++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O | ||||
| C、少量二氧化硫通入次氯酸钠碱性溶液中:SO2+ClO-+2OH-═SO42-+Cl-+H2O | ||||
| D、Ca(HCO3)2溶液与过量NaOH溶液反应:Ca2++HCO3-+OH-═CaCO3↓+H2O |
关于化学计量的应用,下列说法正确的是( )
| A、室温下,106g碳酸钠固体所含有的离子总的物质的量小于3mol |
| B、在同压不同温的情况下,质量相同的氧气和臭氧所含氧原子数不相同 |
| C、将物质的量浓度分别为1mol/L和2mol/L的硫酸等质量混合(假设体积可以加和),则混合后硫酸溶液的浓度为1.5mol/L |
| D、标况下,22.4L CH3Cl分子数约为6.02×1023 |
下列说法正确的是( )
| A、SO2通入品红溶液,溶液褪色的原理与SO2通入溴水后褪色的原理相同 |
| B、浓硫酸具有强氧化性,稀硫酸不具有氧化性 |
| C、用浓FeCl3溶液和NaOH溶液混合制备Fe(OH)3胶体 |
| D、明矾和漂白粉常用于自来水的净化和杀菌消毒,但二者的作用原理不同 |