题目内容
12.研究人员研制出一种锂水电池,可作为鱼雷和潜艇的储备电源.该电池以金属锂和钢板为电极材料,以LiOH为电解质,使用时加入水即可放电.关于该电池的下列说法不正确的是( )| A. | 放电时金属锂作负极 | B. | 放电时OH-向正极移动 | ||
| C. | 水既是氧化剂又是溶剂 | D. | 总反应为:2Li+2H2O=2LiOH+H2↑ |
分析 锂水电池中,自发的氧化还原反应是金属锂和水之间反应生成氢氧化锂和氢气的过程,根据原电池的工作原理以及电极反应特点和规律来回答.
解答 解:A.放电时活泼金属锂失电子作负极,故A正确;
B.原电池中,阴离子移向原电池的负极,即放电时OH-向负极移动,故B错误;
C.金属锂和水之间反应生成氢氧化锂和氢气,该反应中,水是氧化剂,在电池中还可以担当溶剂,故C正确;
D.锂水电池中,自发的氧化还原反应是金属锂和水之间反应生成氢氧化锂和氢气,即总反应为:2Li+2H2O=2LiOH+H2↑,故D正确;
故选B.
点评 本题考查电化学的热点-锂离子电池,根据总反应式判断出正负极和阴阳极的反应,从化合价变化的角度分析,难度中等.

练习册系列答案
相关题目
17.下列说法正确的是( )
| A. | 所有不锈钢都只含有金属元素 | |
| B. | 大多数金属元素均以单质形式存在于自然界 | |
| C. | 广东正在打捞的明代沉船上存在大量铝制餐具 | |
| D. | 镁合金的硬度和强度均高于纯镁 |
1.下列有关实验操作的叙述中不正确的是( )
| A. | 少量白磷贮存在水中,切割时再取出放在干燥玻璃片下进行 | |
| B. | 不慎接触到过多氨时,要及时吸入新鲜空气和水蒸气 | |
| C. | 硝酸不慎滴在手上要立刻用大量水冲洗,再用小苏打水或肥皂洗涤 | |
| D. | 酒精灯在桌上歪倒失火后,立即用湿布盖下 |
2.下列反应属于氧化还原反应的是( )
| A. | NaOH+HCl=NaCl+H2O | B. | Fe+2HCl=FeCl2+H2↑ | ||
| C. | 2NaOH+CO2=Na2CO3+H2O |
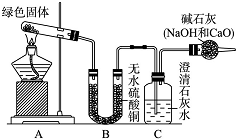 铜器久置,表面会生成一层绿色固体,为了解铜在空气中的腐蚀情况,某化学兴趣小组收集家中铜器表面的绿色固体进行探究.查阅相关资料后,猜想该绿色物质可能是铜的碳酸盐.
铜器久置,表面会生成一层绿色固体,为了解铜在空气中的腐蚀情况,某化学兴趣小组收集家中铜器表面的绿色固体进行探究.查阅相关资料后,猜想该绿色物质可能是铜的碳酸盐.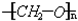 ,是通过加聚反应制得的,合成人造象牙的单体是HCHO
,是通过加聚反应制得的,合成人造象牙的单体是HCHO