题目内容
 X、Y、Z、R、W均为周期表中前四周期的元素,其中原子序数依次增大;X2-和Y+有相同的核外电子排布;Z的气态氢化物的沸点比其上一周期同族元素气态氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气体单质.回答下列问题(相关回答均用元素符号表示):
X、Y、Z、R、W均为周期表中前四周期的元素,其中原子序数依次增大;X2-和Y+有相同的核外电子排布;Z的气态氢化物的沸点比其上一周期同族元素气态氢化物的沸点低;R的基态原子在前四周期元素的基态原子中单电子数最多;W为金属元素,X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气体单质.回答下列问题(相关回答均用元素符号表示):(1)R的基态原子的核外电子排布式是
(2)X与Z中电负性较大的是
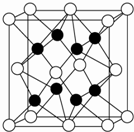
(3)X与Y形成的化合物Y2X的晶胞如图所示.其中X离子的配位数为
(4)已知该化合物的晶胞边长为a pm,则该化合物的密度为
考点:晶胞的计算,元素电离能、电负性的含义及应用,判断简单分子或离子的构型
专题:原子组成与结构专题,化学键与晶体结构
分析:X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气体单质,且Z的气态氢化物的沸点比其上一周期同族元素气态氢化物的沸点低,则Z为Cl元素,W为Mn元素;前四周期中基态原子中单电子数最多也即价层电子排布式为3d54s1(单电子数为6),则R为铬元素;X、Y、Z原子序数依次增大,X2-和Y+有相同的核外电子排布,则X为O元素,Y为Na元素;X与W形成的某种化合物与Z的氢化物的浓溶液加热时反应可用于实验室制取Z的气体单质,可知W为Mn元素.
解答:
(1)依据洪特规则可推知前四周期中基态原子中单电子数最多也即价层电子排布式为3d54s1(单电子数为6),则R为铬元素,其基态原子核外电子排布式为[Ar]3d54s1,故答案为:1s22s22p63s23p63d54s1或[Ar]3d54s1;
(2)O与Cl中电负性较大的是O;Cl的含氧酸盐中用于实验室制取氧气的盐为KClO3,ClO3-的价层电子对数为4(3个σ键、1个孤电子对),故ClO3-的空间构型与NH3相同为三角锥形;ClO3-中Cl、O间为共价键,故答案为:O、三角锥形、共价键;
(3)由晶胞结构可知,白球位于顶点和面心,数目为:8×
+6×
=4,黑球位于体内,数目为8,则白球代表O2-,黑球代表Na+,O2-位于顶点被8个晶胞共有,即与其距离相等且最近的Na+数目为8,其配位数为8,这8个Na+构成正方体或立方体,
故答案为:8,正方体或立方体;
(4)利用均摊法可知一个晶胞中含有4个Na2O微粒,故该晶胞的质量为
,晶胞体积为a3×10-30cm3,密度为:
g?cm-3,故答案为:
.
化合物的密度为NA×a3×10-30(4×62)g?cm-3(注:1 pm=10-10 cm).
(2)O与Cl中电负性较大的是O;Cl的含氧酸盐中用于实验室制取氧气的盐为KClO3,ClO3-的价层电子对数为4(3个σ键、1个孤电子对),故ClO3-的空间构型与NH3相同为三角锥形;ClO3-中Cl、O间为共价键,故答案为:O、三角锥形、共价键;
(3)由晶胞结构可知,白球位于顶点和面心,数目为:8×
| 1 |
| 8 |
| 1 |
| 2 |
故答案为:8,正方体或立方体;
(4)利用均摊法可知一个晶胞中含有4个Na2O微粒,故该晶胞的质量为
| 4×62 |
| NA |
| 4×62 |
| a3×10-30×NA |
| 4×62 |
| a3×10-30×NA |
化合物的密度为NA×a3×10-30(4×62)g?cm-3(注:1 pm=10-10 cm).
点评:本题考查元素推断、杂化类型、配位数和晶胞密度计算,难度不大,应利用均摊法计算出晶胞中所含微粒数.

练习册系列答案
 口算心算速算应用题系列答案
口算心算速算应用题系列答案 同步拓展阅读系列答案
同步拓展阅读系列答案
相关题目
根据热化学方程式(在101kPa时):S(s)+O2(g)=SO2(g)△H=-297.23kJ?mol-1,分析下列说法中不正确的是( )
| A、S(g)+O2(g)=SO2(g)放出热量小于297.23kJ |
| B、S(g)+O2(g)=SO2(g)放出热量大于297.23kJ |
| C、S的燃烧热为297.23kJ?mol-1 |
| D、形成1molSO2的化学键释放的总能量大于断裂1molS(s)和1molO2(g)的化学键吸收的总能量 |
已知化学能与其他形式的能可以相互转化,下列反应中能量的转化形式是由化学能转化为热能的是( )
A、CH4+2O2
| ||||
B、CaCO3
| ||||
C、2H2O
| ||||
D、Pb+PbO2+2H2SO4
|
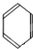 、
、 五种烃,
五种烃,