题目内容
下列说法中正确的是( )
| A、NO2溶于水得到HNO3,所以NO2属于酸性氧化物 |
| B、过氧化钠与水反应的离子方程式为:Na2O2+2H2O═2Na++2OH-+O2↑ |
| C、漂白粉和水玻璃长期暴露在空气中失效,其原理完全相同 |
| D、足量Zn与一定量浓硫酸充分反应得到混合气体 |
考点:氮的氧化物的性质及其对环境的影响,氯、溴、碘及其化合物的综合应用,浓硫酸的性质,钠的重要化合物
专题:元素及其化合物
分析:A.能和碱反应生成盐和水的氧化物属于酸性氧化物;
B.氢原子个数不守恒;
C.依据漂白粉的有效成分次氯酸钙的性质和水玻璃中硅酸钠的性质解答;
D.锌与浓硫酸反应生成二氧化硫,稀硫酸与锌反应生成氢气.
B.氢原子个数不守恒;
C.依据漂白粉的有效成分次氯酸钙的性质和水玻璃中硅酸钠的性质解答;
D.锌与浓硫酸反应生成二氧化硫,稀硫酸与锌反应生成氢气.
解答:
解:A.能和碱反应生成盐和水的氧化物属于酸性氧化物,NO2与碱发生氧化还原反应,不是酸性氧化物,故A错误;
B.过氧化钠与水反应的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑,故B错误;
C.漂白粉中次氯酸钙易和二氧化碳、水反应生成碳酸钙和次氯酸,次氯酸不稳定,光照条件下易分解生成氯化氢和氧气,所以放置在空气中易变质;水玻璃是硅酸钠的水溶液,能和二氧化碳反应生成硅酸和碳酸钠,所以放置在空气中易变质,二者变质的原理不同,故C错误;
D.足量Zn与一定量浓硫酸开始反应生成气体为二氧化硫,随着反应的进行硫酸浓度减小,变为稀硫酸,反应生成氢气,故D正确;
故选:D.
B.过氧化钠与水反应的离子方程式为:2Na2O2+2H2O═4Na++4OH-+O2↑,故B错误;
C.漂白粉中次氯酸钙易和二氧化碳、水反应生成碳酸钙和次氯酸,次氯酸不稳定,光照条件下易分解生成氯化氢和氧气,所以放置在空气中易变质;水玻璃是硅酸钠的水溶液,能和二氧化碳反应生成硅酸和碳酸钠,所以放置在空气中易变质,二者变质的原理不同,故C错误;
D.足量Zn与一定量浓硫酸开始反应生成气体为二氧化硫,随着反应的进行硫酸浓度减小,变为稀硫酸,反应生成氢气,故D正确;
故选:D.
点评:本题考查了二氧化氮、浓硫酸、漂白粉、硅酸钠的性质,离子方程式的书写,题目难度不大,注意浓硫酸与稀硫酸性质的差别导致与金属反应生成气体的不同.

练习册系列答案
 快捷英语周周练系列答案
快捷英语周周练系列答案
相关题目
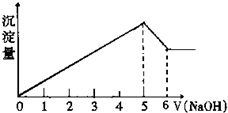 有一镁、铝合金,在适量稀硫酸中恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠溶液的体积变化如图所示,则合金中镁、铝的物质的量之比为( )
有一镁、铝合金,在适量稀硫酸中恰好完全溶解,再加入氢氧化钠溶液,析出沉淀的物质的量随氢氧化钠溶液的体积变化如图所示,则合金中镁、铝的物质的量之比为( )| A、2:1 | B、4:1 |
| C、1:1 | D、1:2 |
下列有关物质性质的应用正确的是( )
| A、P2O5能与水反应,可用于干燥氨气 |
| B、MgO是一种电解质,工业上常用电解MgO冶镁 |
| C、福尔马林具有防腐杀菌效果,可用于浸制生物标本 |
| D、PbO2具有氧化性和导电性,可用作铅蓄电池负极材料 |
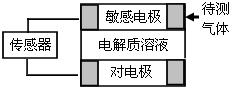 气体的自动化检测中常常应用原电池原理.如图为该电池工作的示意图:气体扩散进入敏感电极,发生反应,传感器就会接收到电信号.下表列出了待测气体及敏感电极上部分反应产物.(对电极:即与敏感电极对应相反的电极)则下列说法中正确的是( )
气体的自动化检测中常常应用原电池原理.如图为该电池工作的示意图:气体扩散进入敏感电极,发生反应,传感器就会接收到电信号.下表列出了待测气体及敏感电极上部分反应产物.(对电极:即与敏感电极对应相反的电极)则下列说法中正确的是( )| 待测气体 | 部分电极反应产物 |
| NO2 | NO |
| Cl2 | HCl |
| CO | CO2 |
| H2S | H2SO4 |
| A、检测Cl2时,电解质溶液中的阴离子向敏感电极移动 |
| B、上表气体检测时,敏感电极均作电池正极 |
| C、检测含相同物质的量的H2S和CO两份空气样本时,传感器上流过的电子物质的量之比为4:1 |
| D、检测H2S气体时,在对电极上充入空气,对电极上的电极反应式为:O2+2H2O+4e-═4OH- |
下列对应化学反应的离子方程式正确的是( )
| A、氨水中通入过量SO2:SO2+NH3?H2O═NH4++HSO3- | ||||
| B、(CH3COO)2Ba溶液中加入稀硫酸:Ba2++SO42-═BaSO4↓ | ||||
C、用铜作电极电解CuSO4溶液:2Cu2++2H2O
| ||||
| D、Al2(SO4)3溶液中加入足量Ba(OH)2溶液:Al3++2SO42-+2Ba2++4OH-═2BaSO4↓+AlO2-+2H2O |
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A、
| ||
| B、0.1mol?L-1 FeCl3溶液:NH4+、H+、I-、SCN- | ||
| C、0.1mol?L-1 Na2CO3溶液:K+、Ca2+、HCO3-、SO42- | ||
| D、使酚酞变红色的溶液:Na+、Ba2+、NO3-、Cl- |
 .
.