题目内容
15.下列有关化学键的说法正确的是( )| A. | HCl溶于水、NaCl溶于水破坏的化学键类型相同 | |
| B. | 碘升华、NaCl 颗粒被粉碎,均破坏化学键 | |
| C. | 氦气、液溴、硫磺中均存在共价键 | |
| D. | 钠与水反应、钠与氧气反应,均存在离子键的形成 |
分析 A.HCl溶于水破坏的是共价键,NaCl溶于水破坏的是离子键;
B.碘分子之间只存在分子间作用力;
C.稀有气体为单原子分子;
D.活泼金属与活泼非金属原子之间一般形成离子键.
解答 解:A.HCl溶于水破坏的是共价键,NaCl溶于水破坏的是离子键,化学键的种类不同,故A错误;
B.碘分子之间只存在分子间作用力,碘升华破坏分子间作用力,不破坏化学键,故B错误;
C.稀有气体为单原子分子,没有共价键,只存在分子间作用力,故C错误;
D.活泼金属与活泼非金属原子之间一般形成离子键,钠与水反应生成NaOH、钠与氧气反应生成氧化钠或过氧化钠,均存在离子键的形成,故D正确.
故选D.
点评 本题考查了化学键、分子间作用力等,难度不大,侧重对基础知识的巩固,注意理解晶体中微粒之间的作用力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
3.下列有关实验的说法正确的是( )
| A. | 用KI滴定FeCl3溶液时可选用淀粉作指示剂 | |
| B. | 向硅酸钠溶液中滴加酚酞,溶液变红,可说明H2SiO3为弱酸 | |
| C. | 除去铜器表面的铜绿[Cu2(OH)2CO3],可用稀硝酸浸泡,再用清水冲洗 | |
| D. | 将浓硫酸加入浓盐酸中可制取氯化氢气体,说明硫酸的酸性比盐酸强 |
20.乙烯的产量是衡量一个国家石油化工发展水平的重要标志.下列表述正确的是( )
| A. | 乙烯的电子式是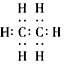 | B. | 乙烯的结构式 CH2=CH2 | ||
| C. | 乙烯分子中所有原子公平面 | D. | 5.6 L乙烯中含有1 mol C-H键 |
7.下列各组中的物质均能发生加成反应的是( )
| A. | 乙烯和溴乙烷 | B. | 溴苯和环己烷 | C. | 苯酚和乙醛 | D. | 丙烯和乙酸乙酯 |
4.下列分子中既能发生消去反应,又能发生氧化反应的是( )
| A. | CH2CH=CHCH2CH2Cl | B. | CH3OH | ||
| C. | 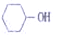 | D. | 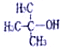 |
15.A、B、C为短周期元素,在周期表中所处的位置如表所示.
A、C两元素的原子核外电子数之和等于B原子的质子数.
(1)写出B、C元素的名称硫、氟.
(2)B位于元素周期表中第3周期第ⅥA族.
(3)用石墨为电极,电解B元素的最高价氧化物的水化物的水溶液,当电路中转移0.4mol电子时,在阴极收集到的产物是H2,质量为0.4g,电解的总反应方程式为2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑;
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式NH3+HNO3═NH4NO3.
| A | C | |
| B |
(1)写出B、C元素的名称硫、氟.
(2)B位于元素周期表中第3周期第ⅥA族.
(3)用石墨为电极,电解B元素的最高价氧化物的水化物的水溶液,当电路中转移0.4mol电子时,在阴极收集到的产物是H2,质量为0.4g,电解的总反应方程式为2H2O$\frac{\underline{\;电解\;}}{\;}$2H2↑+O2↑;
(4)写出A的气态氢化物与其最高价氧化物对应的水化物反应的化学方程式NH3+HNO3═NH4NO3.