题目内容
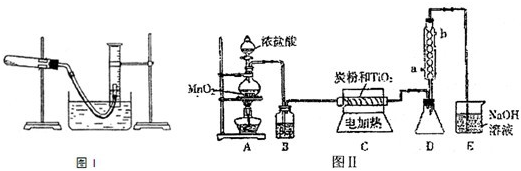
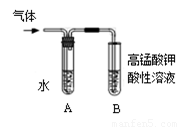
实验室利用如图装置进行中和热的测定,请回答下列问题:(1)在操作正确的前提下,提高中和热测定准确性的关键是______
(2)做1次完整的中和热测定实验,温度计需使用______次,
某同学为了省去清洗温度计的麻烦,建议实验时使用两支温度计分别测量酸和碱的温度,你是否同意该同学的观点,为什么?______
(3)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热为57.3kJ/mol)______
(4)倒入NaOH溶液的正确操作是(从下列选出).______
A.沿玻璃棒缓慢倒入 B.分三次少量倒入 C.一次迅速倒入
(5)使硫酸与NaOH溶液混合均匀的正确操作是E(从下列选出).______
A.用温度计小心搅拌 B.揭开硬纸片用玻璃棒搅拌
C.轻轻地振荡烧杯 D.用套在温度计上的环形玻璃棒轻轻地搅动.
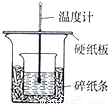
【答案】分析:(1)在中和反应中,必须确保热量不散失;
(2)根据温度计要测反应前酸溶液的温度,测反应前碱溶液的温度,混合反应后测最高温度一共3次;根据不同温度计的误差不同;
(3)根据中和热的概念来分析;
(4)根据硫酸和氢氧化钠反应反应迅速剧烈,并且释放大量热,一次性快速倒入可以减少热量散发而引来的误差;
(5)根据环形玻璃棒可以使硫酸与NaOH溶液混合均匀;
解答:解:(1)在中和反应中,必须确保热量不散失,故答案为:保温;
(2)温度计要测反应前酸溶液的温度,测反应前碱溶液的温度,混合反应后测最高温度一共3次;不同温度计的误差不同,故答案为:3;不同意,因为不同温度计误差不差;
(3)稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式: H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)= Na2SO4(l)+H2O(l)△H=-57.3KJ/mol,故答案为:
Na2SO4(l)+H2O(l)△H=-57.3KJ/mol,故答案为: H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)= Na2SO4(l)+H2O(l)△H=-57.3KJ/mol;
Na2SO4(l)+H2O(l)△H=-57.3KJ/mol;
(4)根据硫酸和氢氧化钠反应反应迅速剧烈,并且释放大量热,一次性快速倒入可以减少热量散发而引来的误差,故选:C;
(5)用套在温度计上的环形玻璃棒轻轻地搅动使硫酸与NaOH溶液混合均匀,故选:D.
点评:本题考查学生中和热测定的实验,保温工作是实验的重点,可以根据所学内容来回答,难度不大.
(2)根据温度计要测反应前酸溶液的温度,测反应前碱溶液的温度,混合反应后测最高温度一共3次;根据不同温度计的误差不同;
(3)根据中和热的概念来分析;
(4)根据硫酸和氢氧化钠反应反应迅速剧烈,并且释放大量热,一次性快速倒入可以减少热量散发而引来的误差;
(5)根据环形玻璃棒可以使硫酸与NaOH溶液混合均匀;
解答:解:(1)在中和反应中,必须确保热量不散失,故答案为:保温;
(2)温度计要测反应前酸溶液的温度,测反应前碱溶液的温度,混合反应后测最高温度一共3次;不同温度计的误差不同,故答案为:3;不同意,因为不同温度计误差不差;
(3)稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式:
 H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)= Na2SO4(l)+H2O(l)△H=-57.3KJ/mol,故答案为:
Na2SO4(l)+H2O(l)△H=-57.3KJ/mol,故答案为: H2SO4(l)+NaOH(l)=
H2SO4(l)+NaOH(l)= Na2SO4(l)+H2O(l)△H=-57.3KJ/mol;
Na2SO4(l)+H2O(l)△H=-57.3KJ/mol;(4)根据硫酸和氢氧化钠反应反应迅速剧烈,并且释放大量热,一次性快速倒入可以减少热量散发而引来的误差,故选:C;
(5)用套在温度计上的环形玻璃棒轻轻地搅动使硫酸与NaOH溶液混合均匀,故选:D.
点评:本题考查学生中和热测定的实验,保温工作是实验的重点,可以根据所学内容来回答,难度不大.

练习册系列答案
相关题目
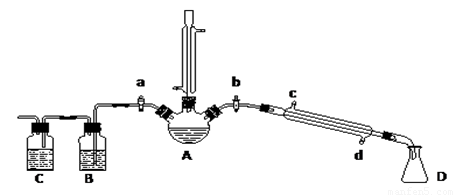
利用如图1所示实验装置可以测定一条条件下1mol气体的体积,图1中仪器C称为液体量瓶,瓶颈上有110~130mL刻度线.将一定质量的镁带和过量的衡硫酸在仪器A瓶中完全反应,产生的H2将B瓶中的液体压入液体量瓶中,根据液体的体积可以转换成H2的体积.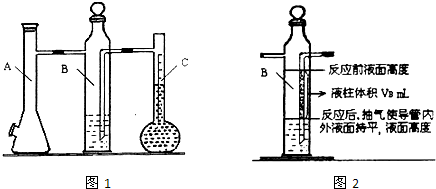
实验步骤:
(1)装配好化学反应气体体积测定仪,作气密性检查.
(2)用砂皮擦去镁带表面的氧化物,然后称取0.100g~0.110g的镁带,把数据记录于表格.
(3)取下A瓶加料口的橡皮塞,用小烧杯加入20mL水,再把已称量的镁带加到A瓶的底部,用橡皮塞塞紧加料口.
(4)用注射器从A瓶加料口处抽气,使B瓶导管内外液面持平.
(5)用注射器吸取10mL 3mol/L硫酸,用针头扎进A瓶加料口橡皮塞,将破酸注入A瓶,注入后迅速拔出针头.
(6)当镁带完全反应后,读取C瓶中液体的体积,把数据记录于表格.
(7)用注射器从A瓶加料口处抽气,使B瓶中导管内外液面持平,记录抽出气体的体积,把数据记录于表格.
重复上述操作进行第二次实验,避免偶然误差.
根据上述实验方法回答下列问题:
实验室温度:25℃,压强:101kPa.该条件下1mol氢气体积的理论值:为24.5L
(1)连接装置及气密性检查:当A瓶加料口塞上橡胶塞, 可以确认装置气密性合格.
(2)B中所装液体一般是 (填“水”或“品红”).A中发生反应的离子方程式为 .
(3)实验数据如下:温度:25℃(镁元素的相对原子质量为24.3)
①上表中X= .
②计算1mol氢气体积两次实验的平均值= L.
③计算实验误差:(实验值-理论值)/理论值×100%= .
④引起该误关的可能原因 (填字母).
A.镁带中含有跟硫酸不反应的杂质
B.没有除去镁带表面的氧化镁
C.镁带中含有杂质铝
D.所用稀硫酸不足量
(4)许多同学在实验中测得的数据偏高(记录数据时已恢复至室温).为此,某化兴趣小组的同学对此实验方案提出了两条修正建议:
①A、B瓶的气体中含有水汽,增加的气体体积中所含的水汽,不该计入氢气的体积.
②B瓶中导管(图2中阴影部分VB)内液柱部分在反应后为空气所占据,不该计入氢气的体积.
你认为他们的意见合理的是 (合理则填序号,否则填“无”).如有合理之处,请根据下面的数据给出修正的1mol氢气体积的数学表达式.(镁元素的相对原子质量为24.3)
1mol氢气体积= L(填写数学表达式).

实验步骤:
(1)装配好化学反应气体体积测定仪,作气密性检查.
(2)用砂皮擦去镁带表面的氧化物,然后称取0.100g~0.110g的镁带,把数据记录于表格.
(3)取下A瓶加料口的橡皮塞,用小烧杯加入20mL水,再把已称量的镁带加到A瓶的底部,用橡皮塞塞紧加料口.
(4)用注射器从A瓶加料口处抽气,使B瓶导管内外液面持平.
(5)用注射器吸取10mL 3mol/L硫酸,用针头扎进A瓶加料口橡皮塞,将破酸注入A瓶,注入后迅速拔出针头.
(6)当镁带完全反应后,读取C瓶中液体的体积,把数据记录于表格.
(7)用注射器从A瓶加料口处抽气,使B瓶中导管内外液面持平,记录抽出气体的体积,把数据记录于表格.
重复上述操作进行第二次实验,避免偶然误差.
根据上述实验方法回答下列问题:
实验室温度:25℃,压强:101kPa.该条件下1mol氢气体积的理论值:为24.5L
(1)连接装置及气密性检查:当A瓶加料口塞上橡胶塞,
(2)B中所装液体一般是
(3)实验数据如下:温度:25℃(镁元素的相对原子质量为24.3)
| 实验次数 | m(Mg)/g | 硫酸体积/mL | 液体量瓶中液体体积/mL | 抽出气体体积/mL | 氢气体积/mL | 计算1mol氢体积/L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | X | |
| 2 | 0.115 | 10.0 | 121.0 | 8.0 |
②计算1mol氢气体积两次实验的平均值=
③计算实验误差:(实验值-理论值)/理论值×100%=
④引起该误关的可能原因
A.镁带中含有跟硫酸不反应的杂质
B.没有除去镁带表面的氧化镁
C.镁带中含有杂质铝
D.所用稀硫酸不足量
(4)许多同学在实验中测得的数据偏高(记录数据时已恢复至室温).为此,某化兴趣小组的同学对此实验方案提出了两条修正建议:
①A、B瓶的气体中含有水汽,增加的气体体积中所含的水汽,不该计入氢气的体积.
②B瓶中导管(图2中阴影部分VB)内液柱部分在反应后为空气所占据,不该计入氢气的体积.
你认为他们的意见合理的是
| 实验次数 | m(Mg) g |
硫酸体积mL | 液体量瓶中液体体积mL | 抽出气体体积mL | B瓶的一段液柱体积mL | 水汽体积百分含量 | 计算1mol氢体积L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | VB | a% |