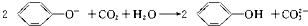题目内容
下列有关实验原理或实验操作正确的是
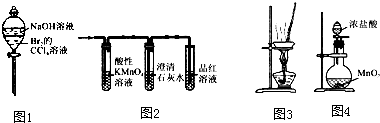
- A.图1装置可以用于除去溶解在CCl4中的Br2
- B.实验室用图2装置检验制得的乙烯中是否混有SO2和CO2
- C.用图3装置在蒸发皿中灼烧CuSO4?5H2O晶体以除去结晶水
- D.实验室常用图4装置制取少量氯气
A
分析:A.溴单质可与氢氧化钠反应;
B.乙烯能被酸性高锰酸钾氧化;
C.灼烧结晶水合物应在坩埚进行;
D.反应需要加热.
解答:A.溴单质可与氢氧化钠反应生成溴化钠和次溴酸钠,二者易溶于水,故A正确;
B.乙烯被酸性高锰酸钾氧化生成二氧化碳,且SO2被酸性高锰酸钾氧化掉,不能使品红褪色,不能确定是否含有SO2,故B错误;
C.灼烧结晶水合物应在坩埚进行,故C错误;
D.浓盐酸和二氧化锰反应需要加热,故D错误.
故选A.
点评:本题考查化学实验,难度中等,注意灼烧结晶水合物应在坩埚进行.
分析:A.溴单质可与氢氧化钠反应;
B.乙烯能被酸性高锰酸钾氧化;
C.灼烧结晶水合物应在坩埚进行;
D.反应需要加热.
解答:A.溴单质可与氢氧化钠反应生成溴化钠和次溴酸钠,二者易溶于水,故A正确;
B.乙烯被酸性高锰酸钾氧化生成二氧化碳,且SO2被酸性高锰酸钾氧化掉,不能使品红褪色,不能确定是否含有SO2,故B错误;
C.灼烧结晶水合物应在坩埚进行,故C错误;
D.浓盐酸和二氧化锰反应需要加热,故D错误.
故选A.
点评:本题考查化学实验,难度中等,注意灼烧结晶水合物应在坩埚进行.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
某同学将一定量铁粉与Cl2恰好完全反应得到一固体物质R,然后通过实验确定其成分.探究过程如下:
(1)提出假设:(请把下列假设补充完整)
假设A:该固体物质是FeCl3;假设B:______;假设C:______.
(2)设计实验方案:
取少量固体物质R于烧杯中,加适量水溶解,然后取两份R溶液分别进行实验,实验现象与结论如下表,请在表格内填写实验现象:
| 实验方法 | 实验现象 | 结论 |
| ①向R溶液中加KSCN溶液 | ______ | 固体物质中有FeCl3 |
| ②向R溶液中滴加酸性KMnO4溶液 | ______ | 固体物质中不含FeCl2 |
(3)写出向R溶液中滴加少量KSCN溶液的离子方程式:______.25℃时,测得该反应达平衡时的平衡常数为K1,保持温度不变,继续滴加少量KSCN溶液,达新平衡时,测得平衡常数为K2,则K1______K2(填“>”,“<”或“=”),溶液的颜色______(填“变深”,“变浅”或“不变”).
(4)R溶液常作印刷电路铜板的腐蚀剂,写出该反应的离子方程式:______.
 2H2O+O2↑
2H2O+O2↑