题目内容
下列陈述I、II均正确且有因果关系的是( )
| 选项 | 陈述I | 陈述II |
| A | 常温下铁与浓硫酸不反应 | 可用铁槽车密封运送浓硫酸 |
| B | NaHCO3溶于水完全电力 | NaHCO3是强电解质 |
| C | NH4Cl为强酸弱碱盐 | 用加热法除去NaCl中的NH4Cl |
| D | H2O2、SO2能使酸性KMnO4溶液褪色 | H2O2表现还原性,SO2表现漂白性 |
| A、A | B、B | C、C | D、D |
考点:铝的化学性质,铵盐,二氧化硫的化学性质,钠的重要化合物
专题:元素及其化合物
分析:A.常温下铁与浓硫酸发生钝化;
B.NaHCO3为强电解质;
C.NH4Cl受热易分解;
D.H2O2、SO2都能使酸性KMnO4溶液褪色,都可被高锰酸钾氧化.
B.NaHCO3为强电解质;
C.NH4Cl受热易分解;
D.H2O2、SO2都能使酸性KMnO4溶液褪色,都可被高锰酸钾氧化.
解答:
解:A.常温下铁与浓硫酸发生钝化,生成致密的氧化膜阻止反应的进一步发生,则可用铁槽车密封运送浓硫酸,陈述I不合理,故A不选;
B.NaHCO3为强电解质,则NaHCO3溶于水完全电离,陈述均合理,存在因果关系,故B选;
C.NH4Cl受热易分解,则用加热法除去NaCl中的NH4Cl,陈述均合理,但不存在因果关系,故C不选;
D.H2O2、SO2都能使酸性KMnO4溶液褪色,都可被高锰酸钾氧化,H2O2、SO2均表现还原性,陈述II不合理,故D不选;
故选B.
B.NaHCO3为强电解质,则NaHCO3溶于水完全电离,陈述均合理,存在因果关系,故B选;
C.NH4Cl受热易分解,则用加热法除去NaCl中的NH4Cl,陈述均合理,但不存在因果关系,故C不选;
D.H2O2、SO2都能使酸性KMnO4溶液褪色,都可被高锰酸钾氧化,H2O2、SO2均表现还原性,陈述II不合理,故D不选;
故选B.
点评:本题考查物质的性质,综合考查元素化合物知识,为高频考点,把握物质的性质、发生的反应、混合物分离方法等为解答的关键,题目难度不大.

练习册系列答案
相关题目
化学与生活密切相关,下列说法正确的是( )
| A、富含N、P元素的生活用水可以直接用来灌溉农田 |
| B、淀粉、纤维素、蛋白质、葡萄糖都是天然高分子化合物 |
| C、“地沟油”虽然对人体有害,但对“地沟油”进行分馏可制得汽油、煤油,达到变废为宝的目的 |
| D、蛋白质、油脂、蔗糖都能水解,但水解产物都不相同 |
下列表示对应化学反应的离子方程式正确的是( )
| A、漂白粉溶液在空气中失效:ClO-+CO2+H2O=HClO+HCO3- |
| B、用KIO3 氧化酸性溶液中的KI:5I-+IO3-+3H2O=3I2+6OH- |
| C、氯化铁溶液与铜反应:Fe3++Cu=Fe2++Cu2+ |
| D、0.01 mol?L-1NH4Al(SO4)2溶液与0.02 mol?L-1Ba(OH)2溶液等体积混合:NH4++Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+Al(OH)3↓+NH3?H2O |
1-溴丙烯能发生如图所示的4个不同反应,其中产物只含有一种官能团的反应是( )
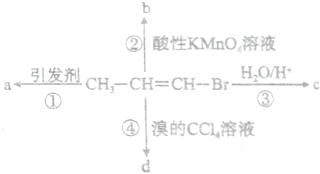

| A、①② | B、②③ | C、③④ | D、①④ |
在加入铝粉能放出氢气的溶液中,可能大量共存的是( )
| A、NH4+、NO3-、SiO32-、Na+ |
| B、Na+、Ba2+、HCO3-、AlO2- |
| C、NO3-、Mg2+、K+、Cl- |
| D、NO3-、K+、AlO2-、OH- |
下列化学反应中,不属于的氧化还原反应是( )
| A、CaO+H2O═Ca(OH)2 | ||||
| B、2Na2O2+2H2O═4NaOH+O2↑ | ||||
| C、2Na+2H2O═2NaOH+H2↑ | ||||
D、C+H2O
|
 铅有+2和+4两种价态,铅的常见氧化物四氧化三铅(Pb2O4)和二氧化铅(PbO2)均常用于蓄电池中,回答下列问题:
铅有+2和+4两种价态,铅的常见氧化物四氧化三铅(Pb2O4)和二氧化铅(PbO2)均常用于蓄电池中,回答下列问题: