题目内容
为了除去MgCl2溶液中的Fe3+,可在加热搅拌的条件下加入的一种试剂是( )
| A、NaOH |
| B、Na2CO3 |
| C、氨水 |
| D、MgO |
考点:物质的分离、提纯的基本方法选择与应用,盐类水解的应用
专题:
分析:Fe3+易水解生成沉淀,可通过调节溶液pH的方法促进Fe3+的水解,注意不能引入新的杂质.
解答:
解:FeCl3易水解生成氢氧化铁,加入Mg(OH)2粉末、MgO或MgCO3,调节溶液的pH,促进铁离子的水解,且不引入新的杂质,故选D.
点评:本题考查物质的分离和提纯,为高频考点,注意根据铁离子易水解的性质用调节溶液pH的方法除杂,注意不能引入新的杂质.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
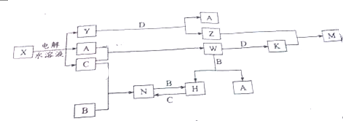
在常温常压下,某实验小组按如图做完实验后,实验报告记录如下.其中描述合理的是( )

| A、①②③ | B、②③④ |
| C、②⑤⑥ | D、③④⑥ |
室温下,下列溶液说法正确的是( )
| A、pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(NH4+)>c(Cl-)>c(OH-)>c(H+) |
| B、0.1mol/LNaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(OH-)>c(HCO3-) |
| C、pH=5的H2S溶液中,c(H+)=c(HS-)=1×10-5 mol?L-1 |
| D、CH3COONa和CaCl2混合溶液:c(Na+)+c(Ca2+)=c(CH3COO-)+c(CH3COOH)+2c(Cl-) |
向含有Fe2+,Al3+,NH4+,Na+,K+的溶液中加入过量的Na2O2固体,微热溶液使其充分反应,再通入过量的HCl气体,则反应后溶液中离子浓度大量减小的是( )
| A、Na+和K+ |
| B、Al3+和Na+ |
| C、Fe2+和NH4+ |
| D、Fe2+和K+ |
下列有机化合物有顺反异构体的是( )
A、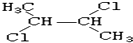 |
| B、CH3CH=CH2 |
| C、CH3CH2CH=CHCH2CH3 |
| D、CH3CH=C(CH3)2 |
 光气(COCl2)、联氨(N2H4)和H2O2具有重要的工业价值.
光气(COCl2)、联氨(N2H4)和H2O2具有重要的工业价值.