题目内容
11.常温下,滴有两滴酚酞试液的Na2CO3溶液中存在CO32-+H2O?HCO3-+OH-平衡,溶液呈红色.下列说法不正确的是( )| A. | 稀释溶液,$\frac{c(HC{O}_{3}^{-})•c(O{H}^{-})}{c(C{O}_{3}^{2-})•c({H}^{+})}$增大 | |
| B. | 通入CO2,或者加入少量氯化铵溶液,溶液pH均减小 | |
| C. | 升高温度,红色变深,平衡常数增大 | |
| D. | 加入NaOH固体,$\frac{c(HCO_3^-)}{{c(CO_3^{2-})}}$减小 |
分析 A、稀释溶液,水解平衡常数不变,而溶液的碱性变弱,即c(H+)增大;
B、通入CO2,或者加入少量氯化铵溶液,均能消耗掉氢氧根,导致c(OH-)减小;
C、盐类水解吸热;
D、加入氢氧化钠固体,增大了c(OH-),结合水解平衡常数来分析.
解答 解:A、稀释溶液,水解平衡常数Kh=$\frac{c(HC{{O}_{3}}^{-})•c(O{H}^{-})}{c(C{{O}_{3}}^{2-})}$不变,而溶液的碱性变弱,即c(H+)增大,故$\frac{c(HC{O}_{3}^{-})•c(O{H}^{-})}{c(C{O}_{3}^{2-})•c({H}^{+})}$变小,故A错误;
B、通入CO2,或者加入少量氯化铵溶液,均能消耗掉氢氧根,导致c(OH-)减小,c(H+)增大,故溶液pH减小,故B正确;
C、盐类水解吸热,故升高温度,水解平衡右移,水解平衡常数增大,且溶液中c(OH-)增大,故红色变深,故C正确;
D、加入氢氧化钠固体,增大了c(OH-),而水解平衡常数Kh=$\frac{c(HC{{O}_{3}}^{-})•c(O{H}^{-})}{c(C{{O}_{3}}^{2-})}$不变,故$\frac{c(HCO_3^-)}{{c(CO_3^{2-})}}$减小,故D正确.
故选A.
点评 本题考查了盐类的水解平衡的移动以及水解平衡常数的应用,应注意的是水解平衡常数和其他的平衡常数相同,均只受温度的影响.

练习册系列答案
相关题目
5.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | 无色透明的溶液中:Fe3+、Mg2+、SCN -、Cl - | |
| B. | c(H+)/c(OH-)=1×10 -12的溶液中:K+、Na+、CO32-、NO3- | |
| C. | c(Fe2+ )=1 mol•L-1的溶液中:K+、NH4+、MnO4-、SO42- | |
| D. | 能使甲基橙变红的溶液中:Na+、NH4+、SO42-、HCO3- |
19.明代《本草纲目》记载了民间酿酒的工艺:“凡破坏之酒,皆可蒸烧”,“以烧酒复烧二次,…,价值数倍也”,这里用到的方法可用于分离( )
| A. | 丙烯酸甲酯和甲醇 | B. | 对硝基甲苯和含硝酸的水层 | ||
| C. | 硝酸钾和氯化钠 | D. | 氯化铵和碳酸铵 |
6.短周期主族元素A、B、C、D、E的原子序数依次增大,考古时利用A元素的某种同位素可以测定一些文物的年代,A原子的最外层比B原子的最外层少2个电子,A、B、C三种元素能组成离子化合物C2AB3,B、D同主族.下列说法正确的是( )
| A. | 含氧酸的酸性由强到弱的顺序:E、D、A | |
| B. | 简单气态氢化物的稳定性由强到弱的顺序:B、D、E | |
| C. | B、C、E形成的共价化合物CEB可以用来杀菌消毒 | |
| D. | 简单离子半径由大到小的顺序:D、E、B、C |
16.下列有关说法中正确的是( )
| A. | 已知25℃时NH4CN溶液显碱性,则25℃时的电离常数K(NH3•H2O)>K(HCN) | |
| B. | 室温时,相同体积、相同pH的盐酸和醋酸溶液中由水电离出的c(H+):盐酸小于醋酸溶液 | |
| C. | 已知Ksp(AgCl)=1.56×10-10,Ksp(Ag2CrO4)=9.0×10-12,向含有Cl-、CrO2-4且浓度均为0.010 mol•L-1溶液中逐滴加入0.010 mol•L-1的AgNO3溶液时,CrO2-4先产生沉淀 | |
| D. | 常温下pH=7的CH3COOH和NaOH混合溶液中,c(Na+)>c(CH3COO-) |
3.关于生活中的化学问题,下列说法错误的是( )
| A. | 地球上的绝大多数金属元素是以化合态形式存在 | |
| B. | 铜盐溶液都有毒,这主要是由于铜离子能使蛋白质变性 | |
| C. | 普通玻璃以纯碱、石灰石、石英砂为主要原料制得 | |
| D. | SO2气体通入氯水中可以增强氯水溶液的漂白性 |
20.化学与生活、生产密切相关,下列叙述正确的是( )
| A. | 为消除碘缺乏症,我国卫生部门规定食盐中必须加碘,其中碘元素以KI形式存在 | |
| B. | 空气污染日报中的空气污染指数的主要项目有可吸入颗粒物、二氧化硫、二氧化氮和二氧化碳 | |
| C. | 用含橙色的酸性重铬酸钾溶液的仪器检验酒驾,利用了乙醇的挥发性和还原性 | |
| D. | 为了获得更好的消毒效果,医用酒精的浓度通常为95% |
9.下列物质的熔、沸点高低顺序正确的是( )
| A. | 金刚石>晶体硅>碳化硅 | B. | HI>HBr>HCl>HF | ||
| C. | NaF>NaCl>NaBr | D. | NaCl>Hg>S |
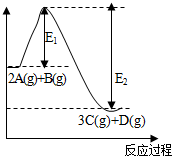 反应2A(g)+B(g)?3C(g)+D(g),△H=akJ/mol.反应过程中的能量变化如图所示.回答下列问题:
反应2A(g)+B(g)?3C(g)+D(g),△H=akJ/mol.反应过程中的能量变化如图所示.回答下列问题: