题目内容
中学化学常见的物质A、B、C、D之间存在如下转化关系:A+B→C+D+H2O.请按要求填空:
(1)若A为短周期元素组成的黑色固体单质,与B的浓溶液共热时,产生C、D两种气体,C、D两种气体均能使澄清石灰水变浑浊,则A与B反应的方程式是 ,已知具有刺激性气味的C气体和Cl2都能漂白某些有色物质,如果将两种气体等物质的量通入到品红溶液中的实验现象为 原因是 .如果将两种气体非等量通入到水中,为了验证哪种气体过量,某兴趣小组的同学准备了以下试剂:
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④苯酚溶液
⑤品红溶液 ⑥酸性高锰酸钾溶液
若Cl2过量:取适量溶液滴加至盛有 (选填一个序号)试剂的试管内,再加入 (选填一个序号)试剂,发生的现象是: ;若C过量:取适量溶液滴加至盛有 (选填一个序号)试剂的试管内,发生的现象是: .
(2)若A在水中的溶解度随温度的升高而降低;B为短周期非金属单质;C是漂白粉的有效成分,则C发生水解反应的离子方程式是 .
(3)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,受热易分解,分解后生成两种极易溶于水的气体.检验A中阳离子的方法是 (简述操作过程及结论).
(1)若A为短周期元素组成的黑色固体单质,与B的浓溶液共热时,产生C、D两种气体,C、D两种气体均能使澄清石灰水变浑浊,则A与B反应的方程式是
①氯化铁溶液 ②氯化亚铁溶液 ③硫氰化钾溶液 ④苯酚溶液
⑤品红溶液 ⑥酸性高锰酸钾溶液
若Cl2过量:取适量溶液滴加至盛有
(2)若A在水中的溶解度随温度的升高而降低;B为短周期非金属单质;C是漂白粉的有效成分,则C发生水解反应的离子方程式是
(3)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,受热易分解,分解后生成两种极易溶于水的气体.检验A中阳离子的方法是
考点:无机物的推断
专题:推断题
分析:(1)C、D两种气体均能使澄清石灰水变浑浊,能使澄清石灰水变浑浊的气体是二氧化碳和二氧化硫,所以C、D和二氧化碳和二氧化硫,A为短周期元素组成的黑色固体单质,所以A是C单质,加热条件下,碳和浓硫酸反应生成二氧化碳和二氧化硫、水,所以B是浓硫酸;具有刺激性气味的C气体为二氧化硫,则D是二氧化碳,二氧化硫与氯气能发生氧化还原反应,根据氯水和二氧化硫水溶液的性质差异答题;
(2)若A在水中的溶解度随温度的升高而降低是氢氧化钙,B为短周期非金属单质,D是漂白粉的成分之一,氢氧化钙和氯气反应生成氯化钙、次氯酸钙和水,所以B是氯气,C能发生水解反应,所以C是次氯酸钙,D是氯化钙;
(3)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,五核10电子的阳离子是铵根离子,受热易分解,分解后生成两种极易溶于水的气体,则A是氯化铵,单核18电子的阴离子是氯离子,氯离子的检验用硝酸酸化的硝酸银溶液,如果生成白色沉淀证明含有氯离子,否则没有氯离子.
(2)若A在水中的溶解度随温度的升高而降低是氢氧化钙,B为短周期非金属单质,D是漂白粉的成分之一,氢氧化钙和氯气反应生成氯化钙、次氯酸钙和水,所以B是氯气,C能发生水解反应,所以C是次氯酸钙,D是氯化钙;
(3)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,五核10电子的阳离子是铵根离子,受热易分解,分解后生成两种极易溶于水的气体,则A是氯化铵,单核18电子的阴离子是氯离子,氯离子的检验用硝酸酸化的硝酸银溶液,如果生成白色沉淀证明含有氯离子,否则没有氯离子.
解答:
解:(1)C、D两种气体均能使澄清石灰水变浑浊,能使澄清石灰水变浑浊的气体是二氧化碳和二氧化硫,所以C、D和二氧化碳和二氧化硫,A是碳,加热条件下,碳和浓硫酸反应生成二氧化碳、二氧化硫和水,反应方程式为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,根据上面的分析可知,C为二氧化硫,如果将二氧化硫和氯气两种气体等物质的量通入到品红溶液中则无现象,原因是Cl2+SO2+2H2O=4H++2Cl-+SO42-,失去漂白性,如果将两种气体非等量通入到水中,若Cl2过量:取适量溶液滴加至盛有 氯化亚铁溶液的试管内,再加入硫氰化钾溶液或苯酚溶液,发生的现象是:溶液呈现红色或紫色;若二氧化硫过量:取适量溶液滴加至盛有品红溶液或酸性高锰酸钾溶液的试管内,发生的现象是红色褪去或紫红色褪去,
故答案为:C+2H2SO4(浓)
CO2↑+2SO2↑+2H2O,无现象;Cl2+SO2+2H2O=4H++2Cl-+SO42-,失去漂白性;②;③(或④);溶液呈现红色(或紫色);⑤(或⑥);红色褪去(紫红色褪去);
(2)若A在水中的溶解度随温度的升高而降低是氢氧化钙,B为短周期非金属单质,D是漂白粉的成分之一,氢氧化钙和氯气反应生成氯化钙、次氯酸钙和水,所以B是氯气,C能发生水解反应,所以C是次氯酸钙,D是氯化钙,次氯酸根离子水解方程式为:ClO-+H2O?HClO+OH-;
故答案为:ClO-+H2O?HClO+OH-;
(3)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,五核10电子的阳离子是铵根离子,受热易分解,分解后生成两种极易溶于水的气体,则A是氯化铵,单核18电子的阴离子是氯离子,氯离子的检验方法是:取少量A于一洁净试管中,加蒸馏水溶解后,滴加硝酸银溶液,产生白色没淀,再滴加稀硝酸,振荡,沉淀不溶解,则A的阴离子为Cl-.
故答案为:取少量A于一洁净试管中,加蒸馏水溶解后,滴加硝酸银溶液,产生白色没淀,再滴加稀硝酸,振荡,沉淀不溶解,则A的阴离子为Cl-.
| ||
故答案为:C+2H2SO4(浓)
| ||
(2)若A在水中的溶解度随温度的升高而降低是氢氧化钙,B为短周期非金属单质,D是漂白粉的成分之一,氢氧化钙和氯气反应生成氯化钙、次氯酸钙和水,所以B是氯气,C能发生水解反应,所以C是次氯酸钙,D是氯化钙,次氯酸根离子水解方程式为:ClO-+H2O?HClO+OH-;
故答案为:ClO-+H2O?HClO+OH-;
(3)若A为五核10电子的阳离子与单核18电子的阴离子构成的无色晶体,五核10电子的阳离子是铵根离子,受热易分解,分解后生成两种极易溶于水的气体,则A是氯化铵,单核18电子的阴离子是氯离子,氯离子的检验方法是:取少量A于一洁净试管中,加蒸馏水溶解后,滴加硝酸银溶液,产生白色没淀,再滴加稀硝酸,振荡,沉淀不溶解,则A的阴离子为Cl-.
故答案为:取少量A于一洁净试管中,加蒸馏水溶解后,滴加硝酸银溶液,产生白色没淀,再滴加稀硝酸,振荡,沉淀不溶解,则A的阴离子为Cl-.
点评:本题以元素化合物的推断为载体考查了氧化还原反应、离子的检验等知识点,同时考查学生推断、分析、归纳总结能力,离子的检验是高考的热点,注意含有弱根离子的盐(弱酸弱碱盐除外)在水中以电离为主水解为次.

练习册系列答案
 全优点练单元计划系列答案
全优点练单元计划系列答案
相关题目
如表所示的五种元素中,W、X、Y、Z为短周期元素,这四种元素的原子最外层电子数之和为22.下列说法正确的是( )
| X | Y | ||
| W | Z | ||
| T |
| A、T元素的单质具有半导体的特性,T与Z元素可形成化合物TZ4 |
| B、X、Y、Z三种元素最低价氢化物的沸点依次升高 |
| C、由X、Y和氢三种元素形成的化合物中只有共价键 |
| D、物质WY2、W3X4、WZ4均有熔点高、硬度大的特性 |
以“创新?未来”为主题的第十四届上海国际车展在浦东新国际博览中心举行.车展期间,新一代电动汽车因其“技术含量高”“节能环保”而倍受关注.液态锂离子电池是一种被采用的车载电池,该电池的电极反应如下:正极6C+xLi++x e-═LixC6,负极LiNiO2-xe-═Li1-xNiO2+xLi+.则下列说法中正确的是( )
| A、放电时,电子从正极流向电源的负极 | |||
| B、放电时,Li+向负极移动 | |||
C、该电池的总反应为LiNiO2+6C
| |||
| D、充电时,阳极发生的电极反应为Li1-xNiO2+xLi++x e-═LiNiO2 |
下列装置的线路接通后,经过一段时间,溶液的pH值明显下降的是( )
A、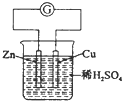 |
B、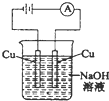 |
C、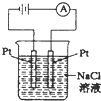 |
D、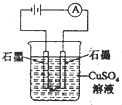 |
赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S,将赤铜矿与辉铜矿混合加热发生以下反应:Cu2S+2Cu2O
6Cu+SO2↑,下列说法中错误的是( )
| ||
| A、在Cu2O、Cu2S中Cu元素化合价都是+1价 |
| B、反应中Cu元素被氧化,S元素被还原 |
| C、Cu2S在反应中既是氧化剂,又是还原剂 |
| D、每生成6.4gCu,反应中转移0.1mol电子 |
 已知R-CH═CH2+HX
已知R-CH═CH2+HX .如图中的A、B分别是分子式为C3H7Cl的两种同分异构体,请根据图中所示物质转化关系和反应条件,判断并写出:
.如图中的A、B分别是分子式为C3H7Cl的两种同分异构体,请根据图中所示物质转化关系和反应条件,判断并写出: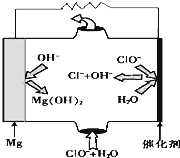 完成下列热化学方程式(化学方程式、电极反应式、表达式等)的书写:
完成下列热化学方程式(化学方程式、电极反应式、表达式等)的书写: