题目内容
下列说法正确的是( )
| A、用可溶性钡盐检验SO42-离子的存在时,先在待测溶液中加入盐酸,其作用是排除 SO42-以外的其它阴离子及Ag+的干扰 |
| B、在某待测液中滴加盐酸产生能使澄清石灰水变浑浊的气体,说明待测液中有CO32- |
| C、在某待测液中滴加氢氧化钠溶液并加热,产生无色有刺激性气味的气体,且该气体能使湿润的蓝色石蕊试纸变红,说明待测液中有NH4+ |
| D、在某待测液中滴加硝酸银溶液有白色沉淀产生,说明待测液中有Cl- |
考点:常见阴离子的检验,常见阳离子的检验
专题:物质检验鉴别题
分析:A、先排除其它离子的干扰,再根据能使钡盐产生白色沉淀的一定是硫酸根离子;
B、能使澄清石灰水变浑浊的气体不一定是二氧化碳,和盐酸反应产生二氧化碳气体的也不一定是碳酸根离子;
C、湿润红色石蕊试纸遇碱性物质变蓝;
D、能使银离子产生白色沉淀的离子有氯离子、硫酸根离子等.
B、能使澄清石灰水变浑浊的气体不一定是二氧化碳,和盐酸反应产生二氧化碳气体的也不一定是碳酸根离子;
C、湿润红色石蕊试纸遇碱性物质变蓝;
D、能使银离子产生白色沉淀的离子有氯离子、硫酸根离子等.
解答:
解:A、先在待测溶液中加入盐酸,排除SO42-以外的其它阴离子及Ag+的干扰,再用可溶性钡盐检验SO42-离子的存在是正确的做法,故A正确;
B、能使澄清石灰水变浑浊的气体有二氧化碳和二氧化硫,加盐酸有无色气体产生,该气体能使澄清石灰水变混浊,原溶液中不一定有CO32-,也可能含有HCO3-,SO32-等,故B错误;
C、湿润红色石蕊试纸遇碱性物质变蓝,加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+,故C错误;
D、能使银离子产生白色沉淀的离子有氯离子、硫酸根离子等,所以在某待测液中滴加硝酸酸化的硝酸银溶液有白色沉淀产生,待测液中不一定有Cl-,故D错误.
故选:A.
B、能使澄清石灰水变浑浊的气体有二氧化碳和二氧化硫,加盐酸有无色气体产生,该气体能使澄清石灰水变混浊,原溶液中不一定有CO32-,也可能含有HCO3-,SO32-等,故B错误;
C、湿润红色石蕊试纸遇碱性物质变蓝,加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH4+,故C错误;
D、能使银离子产生白色沉淀的离子有氯离子、硫酸根离子等,所以在某待测液中滴加硝酸酸化的硝酸银溶液有白色沉淀产生,待测液中不一定有Cl-,故D错误.
故选:A.
点评:本题考查离子的检验,题目难度不大,注意多积累离子的检验方法,做题时注意排除其它离子的干扰.

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
下列各情况,在其中Fe片腐蚀最快的是( )
A、 |
B、 |
C、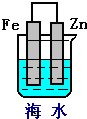 |
D、 |
物质的熔沸点能用键能大小解释的是( )
| A、H2O>H2S |
| B、O2>N2 |
| C、Na>K |
| D、SiO2>CO2 |
下列物质属于纯净物的是( )
| A、空气 | B、干冰 | C、煤 | D、石油 |
下表是第三周期部分元素的电离能[单位:eV(电子伏特)]数据.
根据以上数据分析,下列说法正确的是( )
| 元素 | I1/eV | I2/eV | I3/eV |
| 甲 | 5.7 | 47.4 | 71.8 |
| 乙 | 7.7 | 15.1 | 80.3 |
| 丙 | 13.0 | 23.9 | 40.0 |
| 丁 | 15.7 | 27.6 | 40.7 |
| A、甲的金属性比乙弱 |
| B、乙的化合价为+1价 |
| C、丙一定为非金属元素 |
| D、丁一定为金属元素 |
一种无色溶液中加入BaCl2溶液,生成不溶于稀HNO3的白色沉淀,则该溶液中含有的离子是( )
A、一定含有SO
| ||
B、一定含有CO
| ||
| C、可能有Ag+ | ||
D、一定有SO
|
 如图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列选项编号对应的曲线编号错误的是( )
如图中横坐标为加入反应物的物质的量,纵坐标为产生沉淀的物质的量.下列选项编号对应的曲线编号错误的是( )| A、向NaAlO2溶液中逐渐滴入HCl至过量 |
| B、向澄清石灰水中通入SO2至过量 |
| C、向含有盐酸的AlCl3溶液中滴入NaOH溶液至过量 |
| D、向含有等物质的量的Ca(OH)2、KOH的混合溶液中通入CO2至过量 |