��Ŀ����
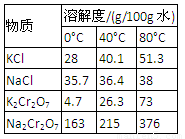
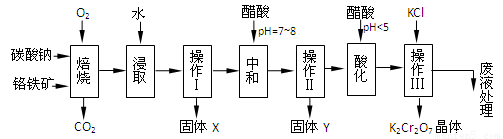
�����12�֣����������Ҫ�ɷֿɱ�ʾΪFeO��Cr2O3��������MgO��Al2O3��Fe2O3�����ʣ��������Ը�����Ϊԭ���Ʊ��ظ���أ�K2Cr2O7��������ͼ��
��֪����4FeO��Cr2O3+ 8Na2CO3+ 7O28Na2CrO4+ 2 Fe2O3 + 8CO2����
��Na2CO3 + Al2O32NaAlO2+ CO2������ Cr2O72��+ H2O
2CrO42�� + 2H+
��������ش��������⣺
1������X����Ҫ����_________����д��ѧʽ����Ҫ����ữ��������Һ��pH�Ƿ����4.5��Ӧ��ʹ��__________����д�������Լ����ƣ���
2���ữ�����ô��������ҺpH<5����Ŀ����_________________________________��
3���������жಽ��ɣ����K2Cr2O7����IJ��������ǣ�����KCl���塢����Ũ���� �����ˡ�_______�����
4���±���������ʵ��ܽ�����ݣ�����������Ӧ�Ļ�ѧ����ʽ�ǣ�Na2Cr2O7+2KCl �� K2Cr2O7��+2NaCl���÷�Ӧ����Һ���ܷ�����������_______________��
5������ƷY��Ҫ��������������������þ���������ܻ����P���������ʣ���ȷ����Y���������������ķ����dz�ȡn g��Ʒ���������______����д�Լ������ܽ⡢���ˡ���______����д�Լ������������ա���ȴ���������ø������m g ��������Ʒ��������������������Ϊ_________���ú�m��n�Ĵ���ʽ��ʾ����
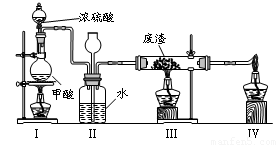
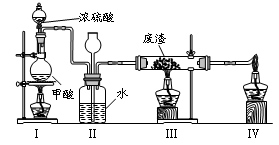
6�����۸��ж�����Cr3+���ȫ����ҵ������CrO3���������������ķ���֮һ�Ǹɷ��ⶾ����ú����ȫȼ�����ɵ�CO��ԭCrO3����ʵ������ģ����һ���̵�װ�����£�
CO�ɼ�����ˮ�Ƶã�ʵ�����ʱϨ��ƾ��Ƶ�˳����_________________________��
�����12�֣�
1��Fe2O3��MgO��2�֣���pH�ƻ���pH��ֽ��
2��ʹCrO42��ת��ΪCr2O72��
3����ȴ�ᾧ��ϴ�ӡ�
4��K2Cr2O7���ܽ�ȱ�Na2Cr2O7С��������������K2Cr2O7���ܽ����С����
5�� NaOH��Һ��ͨ�����������̼����2�֣���
6��III��I��IV
����:���������̿�����Ϊ��
1��ԭ�Ͼ�������Ҫ��������������Ӧ��
��4FeO��Cr2O3+ 8Na2CO3+7O28Na2CrO4 + 2 Fe2O3 + 8CO2����
��Na2CO3 + Al2O32NaAlO2+ CO2��
��ˮ��ȡ������CO2 �ݳ���Na2CrO4��NaAlO2 ����ˮ�������˳��IJ�����X��Ҫ��Fe2O3��MgO
2����������pH��7~8��Ŀ����ʹNaAlO2 ��Ϊ����Y��Al��OH��3
�ɷ�Ӧ�� Cr2O72��+ H2O2CrO42�� + 2H+ ��֪��������pH<5ʱ��CrO42��ת��ΪCr2O72��
3��4���ڴ��ữ�����Һ�м���KCl������ӦNa2Cr2O7+2KCl �� K2Cr2O7��+2NaCl���ɵõ�K2Cr2O7���壻�˷�Ӧֻ�����ܷ�����������е����ݿ�֪���ڽϵ��¶��£���������K2Cr2O7���ܽ����С�������Ը����������ܽ�ȵļ�С����ࡣ���Ի��K2Cr2O7����һ�������ڸ����µõ����Ũ����Һ�����������ǣ�����KCl���塢����Ũ������ȴ�ᾧ�����ˡ�ϴ�ӡ�����
5�������������������ԣ�һ����ʹ������ǿ����Һ����ͨ��CO2 ��������������������
6��CO��ʵ������ȡ����һ����HCOOH��ˮ��ʵ�����ʱӦע��ʵ�鰲ȫ�����ҷ�������������Ϩ��IIIװ���еĵƣ���Ϩ��I�еĵƣ�ֹͣͨCO�����Ϩ��IV�еĵƣ��Է���Ⱦ������

�����12�֣���ˮ�ϸ�����ͭ [Cu(C1O4)2 ��6H2O]��һ����ɫ���壬������ˮ��120��ʱ��ʼ�ֽ⡣ʵ����������ͭ�Ĵֲ�Ʒ�Ʊ�����������ͭ������������£�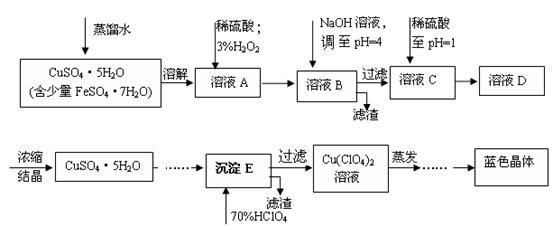
��֪��
| ���� | ��ҺpHֵ | |
| ��ʼ���� | ������ȫ | |
| Fe2+ | 7.6 | 9.6 |
| Fe3+ | 2.7 | 3.7 |
| Cu2+ | 5.2 | 6.4 |
��2������ҺC�м���ϡ�������pH=1��Ŀ����________________________________________��
��3��������������ҺC�е������Ƿ������������� ��
��4����������__________(��д����)��Ȼ����ȴ�ᾧ�����ˡ�ϴ�ӡ� ����д���������õ���������ɫ���塣
��5����Ϊ�˲ⶨ����ͭ�Ĵֲ�Ʒ�Ĵ��ȣ�ijͬѧ��������ͭ�Ĵֲ�Ʒ2.000g�� �� ������дʵ�鲽�裩���ˡ�ϴ�ӳ������ڿ��������գ����������ٸı�ʱ���Ƶ�����Ϊ0.58816 g��
��6��������Ʒ�Ĵ���Ϊ___________�������Ʒ��ʵ�ʴ���Ϊ93.2%����ⶨ��������Ϊ__________��


 8Na2CrO4 + 2 Fe2O3 + 8CO2����
8Na2CrO4 + 2 Fe2O3 + 8CO2���� 2CrO42��+ 2H+
2CrO42��+ 2H+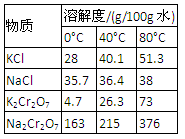
 8Na2CrO4
+ 2 Fe2O3 + 8CO2����
8Na2CrO4
+ 2 Fe2O3 + 8CO2���� 2CrO42�� + 2H+
2CrO42�� + 2H+