题目内容
某化学课外活动小组在实验室做了如下一系列实验:
(1)该小组设计了如图1所示的一套气体发生、收集和尾气吸收装置以探究装置的多功能性.

①甲同学认为装置Ⅰ可作为实验室制氧气的快速发生器,则装置Ⅰ的a仪器中可加入 或 ,装置Ⅱ从管口进气即可作为O2的收集装置.
②乙同学认为利用装置Ⅱ,可收集NO,试简述操作方法 :
(2)小组在整理实验室的化学试剂时,发现一盛有无色溶液的试剂瓶.标签破损(如图2),请你根据已掌握的知识,对该试剂可能是什么物质的溶液作出二种猜想,并设计实验验证,写出任一种的实验操作、现象和结论.
(3)该小组从ZnSO4、FeCl3的混合溶液中制取ZnSO4?7H2O过程如下:
a.在混合液中加入6mol?L-1 NaOH溶液,至pH=8为止.
b.过滤后得到沉淀,用蒸馏水多次洗涤沉淀.
c.向洗涤后的沉淀中加入2mol?L-1的硫酸,保持溶液的pH在4~6,加热煮沸,趁热过滤,滤液即为ZnSO4溶液
d.滤液中注入2mol?L-1的硫酸,使其pH保持为2
已知部分阳离子以氢氧化物的形式开始沉淀至完全沉淀时溶液的pH见表,回答下列问题:
①步骤a中用pH试纸控制溶液pH=8,使用pH试纸的操作是 ;步骤b中如何检验沉淀已经洗涤干净? .
②要制得ZnSO4?7H2O的步骤d还缺少的操作是,所用的主要硅酸盐仪器是 .
(1)该小组设计了如图1所示的一套气体发生、收集和尾气吸收装置以探究装置的多功能性.

①甲同学认为装置Ⅰ可作为实验室制氧气的快速发生器,则装置Ⅰ的a仪器中可加入
②乙同学认为利用装置Ⅱ,可收集NO,试简述操作方法
(2)小组在整理实验室的化学试剂时,发现一盛有无色溶液的试剂瓶.标签破损(如图2),请你根据已掌握的知识,对该试剂可能是什么物质的溶液作出二种猜想,并设计实验验证,写出任一种的实验操作、现象和结论.
| 猜想物质的化学式 | 检验所需要的试剂 | 操作、现象和结论 | |
| ① | |||
| ② |
a.在混合液中加入6mol?L-1 NaOH溶液,至pH=8为止.
b.过滤后得到沉淀,用蒸馏水多次洗涤沉淀.
c.向洗涤后的沉淀中加入2mol?L-1的硫酸,保持溶液的pH在4~6,加热煮沸,趁热过滤,滤液即为ZnSO4溶液
d.滤液中注入2mol?L-1的硫酸,使其pH保持为2
已知部分阳离子以氢氧化物的形式开始沉淀至完全沉淀时溶液的pH见表,回答下列问题:
| 沉淀物 | Fe(OH)3 | Zn(OH)2 |
| pH | 1.5~3.2 | 6.4~8.0 |
②要制得ZnSO4?7H2O的步骤d还缺少的操作是,所用的主要硅酸盐仪器是
考点:常见气体制备原理及装置选择,物质的检验和鉴别的实验方案设计,制备实验方案的设计
专题:实验设计题
分析:(1)①装置Ⅰ可作为实验室制氧气的快速发生器,是分液漏斗中a的液体加入烧瓶b中迅速发生反应生成氧气,可以用水滴入过氧化钠中,过氧化氢滴入固体二氧化锰中;
②一氧化氮气体易被氧气氧化,不能用排气法收集,难溶于水可以用排水法收集,利用装置Ⅲ装满水导气管短进长出收集;
(2)结合图可知,可能为硫酸钠、碳酸钠、亚硫酸钠等,检验硫酸根离子利用盐酸和氯化钡,检验碳酸根离子,利用盐酸、品红及石灰水,检验亚硫酸根离子利用盐酸和品红,以此来解答;
(3)①用PH试纸测PH时,试纸不能湿润;取最后一次洗涤液少量,滴加硝酸银溶液,若无白色沉淀,说明已经洗涤干净;
②加热蒸发需要用蒸发皿,酒精灯,玻璃棒.
②一氧化氮气体易被氧气氧化,不能用排气法收集,难溶于水可以用排水法收集,利用装置Ⅲ装满水导气管短进长出收集;
(2)结合图可知,可能为硫酸钠、碳酸钠、亚硫酸钠等,检验硫酸根离子利用盐酸和氯化钡,检验碳酸根离子,利用盐酸、品红及石灰水,检验亚硫酸根离子利用盐酸和品红,以此来解答;
(3)①用PH试纸测PH时,试纸不能湿润;取最后一次洗涤液少量,滴加硝酸银溶液,若无白色沉淀,说明已经洗涤干净;
②加热蒸发需要用蒸发皿,酒精灯,玻璃棒.
解答:
解:(1)①装置Ⅰ可作为实验室制氧气的快速发生器,是分液漏斗中a的液体加入烧瓶b中迅速发生反应生成氧气,可以用水滴入过氧化钠中,发生反应2Na2O2+2H2O=4NaOH+O2↑;过氧化氢滴入固体二氧化锰中反应生成氧气,2H2O2
2H2O+O2↑;
故答案为:H2O2;H2O;
②一氧化氮气体易被氧气氧化,不能用排气法收集,难溶于水可以用排水法收集,利用装置II装满水导气管短进长出收集;
故答案为:先将广口瓶中盛满水,从d管通入NO;
(2)结合图可知,可能为硫酸钠、碳酸钠、亚硫酸钠等,
若为Na2SO4,需要试剂为稀盐酸和BaCl2溶液,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入BaCl2溶液,如果生成白色沉淀,则原溶液是Na2SO4溶液;
若为Na2CO3,需要试剂为稀盐酸、品红试纸和澄清石灰水,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体不能使湿润的品红试纸变红,但能使澄清石灰水变浑浊.原溶液是Na2CO3溶液;
若为Na2SO3,需要试剂为稀盐酸、品红试纸,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体能使湿润的品红试纸变红,原溶液是Na2SO3溶液;
若为Na2SiO3,需要实际为稀盐酸,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生白色沉淀,则原溶液是Na2SiO3溶液,
故答案为:
;
(3)①用PH试纸测PH时,试纸不能湿润,则使用pH试纸的操作是取一片pH试纸置于洁净的玻璃片上,用玻璃棒蘸取溶液,点滴在pH试纸中央,待变色后,与标准比色卡对照;取最后一次洗涤液少量,滴加硝酸银溶液,若无白色沉淀,说明已经洗涤干净;
故答案为:取一片pH试纸置于洁净的玻璃片上,用玻璃棒蘸取溶液,点滴在pH试纸中央,待变色后,与标准比色卡对照;取最后一次洗涤液少量,滴加硝酸银溶液,若无白色沉淀,说明已经洗涤干净;
②加热蒸发需要用仪器蒸发皿,酒精灯,玻璃棒;
故答案为:蒸发皿,酒精灯,玻璃棒.
| ||
故答案为:H2O2;H2O;
②一氧化氮气体易被氧气氧化,不能用排气法收集,难溶于水可以用排水法收集,利用装置II装满水导气管短进长出收集;
故答案为:先将广口瓶中盛满水,从d管通入NO;
(2)结合图可知,可能为硫酸钠、碳酸钠、亚硫酸钠等,
若为Na2SO4,需要试剂为稀盐酸和BaCl2溶液,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入BaCl2溶液,如果生成白色沉淀,则原溶液是Na2SO4溶液;
若为Na2CO3,需要试剂为稀盐酸、品红试纸和澄清石灰水,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体不能使湿润的品红试纸变红,但能使澄清石灰水变浑浊.原溶液是Na2CO3溶液;
若为Na2SO3,需要试剂为稀盐酸、品红试纸,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体能使湿润的品红试纸变红,原溶液是Na2SO3溶液;
若为Na2SiO3,需要实际为稀盐酸,现象与结论为取少量该溶液于试管中,滴入稀盐酸,若产生白色沉淀,则原溶液是Na2SiO3溶液,
故答案为:
| 猜想的化学物质 | 检验需要的试剂 | 操作、现象和结论 | |
| 1 | Na2SO4 | 稀盐酸和BaCl2溶液 | 取少量该溶液于试管中,滴入稀盐酸,若无明显现象,再滴入BaCl2溶液,如果生成白色沉淀,则原溶液是Na2SO4溶液 |
| 2 | Na2CO3 | 稀盐酸、品红试纸和澄清石灰水 | 取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体不能使湿润的品红试纸变红,但能使澄清石灰水变浑浊.原溶液是Na2CO3溶液. |
| 3 | Na2SO3 | 稀盐酸、品红试纸 | 取少量该溶液于试管中,滴入稀盐酸,若产生的无色气体能使湿润的品红试纸变红,原溶液是Na2SO3溶液. |
| 4 | Na2SiO3 | 稀盐酸 | 取少量该溶液于试管中,滴入稀盐酸,若产生白色沉淀,则原溶液是Na2SiO3溶液. |
(3)①用PH试纸测PH时,试纸不能湿润,则使用pH试纸的操作是取一片pH试纸置于洁净的玻璃片上,用玻璃棒蘸取溶液,点滴在pH试纸中央,待变色后,与标准比色卡对照;取最后一次洗涤液少量,滴加硝酸银溶液,若无白色沉淀,说明已经洗涤干净;
故答案为:取一片pH试纸置于洁净的玻璃片上,用玻璃棒蘸取溶液,点滴在pH试纸中央,待变色后,与标准比色卡对照;取最后一次洗涤液少量,滴加硝酸银溶液,若无白色沉淀,说明已经洗涤干净;
②加热蒸发需要用仪器蒸发皿,酒精灯,玻璃棒;
故答案为:蒸发皿,酒精灯,玻璃棒.
点评:本题考查知识综合而全面,涉及气体的制备与收集、物质鉴别和检验方法的选择和应用等,能很好的考查出学生对所学知识的掌握和应用情况,注意试剂的选择、现象与结论的关系即可解答,具有一定的开放性,题目难度中等.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列物质:①乙烷②苯③乙烯④乙炔,其中不能能使KMnO4酸性溶液褪色的是( )
| A、①② | B、①③ | C、③④ | D、②③ |
下列叙述中,正确的是( )
| A、1 mol H2的质量只有在标准状况下才约为2 g |
| B、1 mol H2和O2的混合气体,在标准状况下的体积也是约为22.4L |
| C、在20℃时,1 mol的任何气体的体积总比22.4 L大 |
| D、标准状况下SO3的体积是22.4L时,则其物质的量约是1 mol,所含分子数约是6.02×1023 |
 可用图所示装置制取、净化、收集的气体是( )
可用图所示装置制取、净化、收集的气体是( )| A、铜和稀硝酸制一氧化氮 |
| B、用双氧水和MnO2制氧气 |
| C、石灰石和稀硫酸制CO2 |
| D、稀盐酸和MnO2制氯气 |
下列叙述正确的是( )
| A、某有机物燃烧后产物只有CO2和H2O,可推出的结论是有机物属于烃 |
| B、某有机物燃烧后产物只有CO2和H2O,可推出的结论是有机物属于烃的含氧衍生物 |
| C、某有机物燃烧后产物只有CO2和H2O,通过测定有机物、CO2和H2O的质量,可确定有机物是否含有氧 |
| D、甲烷在同系物中含碳量最高,因而是清洁能源 |
能用“Ba2++SO42-=BaSO4↓”表示的反应是( )
| A、H2SO4与Ba(OH)2反应 |
| B、K2SO4与Ba(OH)2反应 |
| C、CuSO4与Ba(OH)2反应 |
| D、H2SO4与BaCO3反应 |
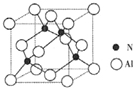 氮的化合物在无机化工领域有着重要的地位.请回答下列问题:
氮的化合物在无机化工领域有着重要的地位.请回答下列问题: