题目内容
 通过对模型、图形、图表的观察,能获取有关信息是化学学习的一种重要能力.按要求回答下列问题.
通过对模型、图形、图表的观察,能获取有关信息是化学学习的一种重要能力.按要求回答下列问题.(1)现有下列短周期元素性质的部分数据,其中X数值是表示不同元素的原子在分子内吸引电子的能力大小,若X值越大,其原子吸引电子能力越强,在所形成的分子中成为带负电荷一方:
| 元素编号/元素性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |
| X | 3.44 | 2.55 | 0.98 | 2.04 | 2.19 | 3.16 | 0.93 | 3.04 | 1.61 | |
| 常见化合价 | 最高价 | +4 | +1 | +3 | +1 | +3 | ||||
| 最低价 | -2 | -4 | -3 | -1 | -3 | |||||
(2)已知4种无机化合物在水中和液氨中的溶解度(g/100g溶剂)为:
| 物质/20℃时溶解度(g/100g溶剂) | AgNO3 | Ba(NO3)2 | AgCl | BaCl2 |
| 水中 | 216 | 9.02 | 1.9×10-14 | 35.8 |
| 液氨 | 86 | 97.2 | 0.8 | 0 |
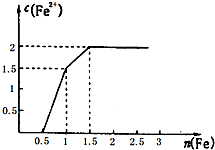
(3)某稀溶液中含有Fe(NO3)3、Cu(NO3)2、HNO3,向其中逐渐加入铁粉,溶液中Fe2+的浓度和加入铁粉的物质的量之间的关系如图所示.三种物质和铁发生反应的顺序为
考点:元素周期律和元素周期表的综合应用,物质的量浓度的相关计算,铁盐和亚铁盐的相互转变
专题:计算题,元素周期律与元素周期表专题
分析:(1)①只有-2价,没有正化合价,则①为O;④⑨都有最高价+3,处于ⅢA族,④吸引电子能力更强,则④为B、⑨为Al;⑤⑧都有最低价-3,处于ⅤA族,⑧吸引电子能力更强,故⑤为P、⑧为N;⑥有最低价-1,吸引电子能力比O若,故⑥为Cl;②有+4、-4价,吸引电子能力大于P,故②为C;③⑦都有+1价,处于ⅠA,吸引电子能力小于Al,且⑦吸引电子能力更弱,故③为Li、⑦为Na;
(2)在水中AgCl溶解度最小,故水溶液中硝酸银与氯化钡可以发生复分解反应;
氨水中氯化钡溶解度为0,故氨水中氯化银与硝酸钡发生复分解反应;
(3)稀溶液中各物质的氧化性顺序为HNO3>Fe (NO3) 3>Cu (NO3) 2,加入铁后会依次发生氧化还原反应:①Fe+4HNO3=Fe(NO3)3+NO↑+2H2O;②Fe+2Fe3+=3Fe2+;③Fe+Cu2+=Cu+Fe2+;由图象可知,加入0.5molFe时,硝酸恰好反应生成Fe(NO3)3,从0.5mol~1mol消耗的0.5molFe与溶液中铁离子恰好完全反应,从1.5mol~2mol消耗的0.5molFe与溶液中铜离子完全反应,据此计算.
(2)在水中AgCl溶解度最小,故水溶液中硝酸银与氯化钡可以发生复分解反应;
氨水中氯化钡溶解度为0,故氨水中氯化银与硝酸钡发生复分解反应;
(3)稀溶液中各物质的氧化性顺序为HNO3>Fe (NO3) 3>Cu (NO3) 2,加入铁后会依次发生氧化还原反应:①Fe+4HNO3=Fe(NO3)3+NO↑+2H2O;②Fe+2Fe3+=3Fe2+;③Fe+Cu2+=Cu+Fe2+;由图象可知,加入0.5molFe时,硝酸恰好反应生成Fe(NO3)3,从0.5mol~1mol消耗的0.5molFe与溶液中铁离子恰好完全反应,从1.5mol~2mol消耗的0.5molFe与溶液中铜离子完全反应,据此计算.
解答:
解:(1)①只有-2价,没有正化合价,则①为O;④⑨都有最高价+3,处于ⅢA族,④吸引电子能力更强,则④为B、⑨为Al;⑤⑧都有最低价-3,处于ⅤA族,⑧吸引电子能力更强,故⑤为P、⑧为N;⑥有最低价-1,吸引电子能力比O若,故⑥为Cl;②有+4、-4价,吸引电子能力大于P,故②为C;③⑦都有+1价,处于ⅠA,吸引电子能力小于Al,且⑦吸引电子能力更弱,故③为Li、⑦为Na,
故答案为:O;C;B;P;Cl;
(2)在水中AgCl溶解度最小,故水溶液中硝酸银与氯化钡可以发生复分解反应,反应方程式为:2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2,
氨水中氯化钡溶解度为0,故氨水中氯化银与硝酸钡发生复分解反应,反应方程式为:2AgCl+Ba(NO3)2=BaCl2↓+2AgNO3,
故答案为:2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2;2AgCl+Ba(NO3)2=BaCl2↓+2AgNO3;
(3)根据氧化性:HNO3>Fe3+>Cu2+,加入铁后会依次发生氧化还原反应,
①Fe+4HNO3═Fe(NO3)3+NO↑+2H2O,离子方程式为:Fe+4H++NO3-=Fe3++NO↑+2H2O,
②Fe+2Fe3+═3Fe2+;
③Fe+Cu2+═Cu+Fe2+;
从图象中可知铁为0.5mol时,无Fe2+生成,发生的反应①,消耗硝酸为2mol,生成Fe3+为0.5mol,
再加入0.5mol铁发生反应②,生成Fe2+物质的量为1.5mol,反应的Fe3+物质的量为1mol,其中原溶液中的Fe3+物质的量0.5mol,故原溶液有Fe3+物质的量为0.5mol,
从1.5mol~2mol消耗的0.5molFe与溶液中铜离子完全反应,故原溶液中Cu2+为0.5mol
故原溶液中Fe(NO3)3、Cu(NO3)2、HNO3分别为0.5mol、0.5mol、2mol,三者的浓度之比为0.5mol:0.5mol:2mol=1:1:4,
故答案为:HNO3、Fe(NO3)3、Cu(NO3)2;Fe+4H++NO3-=Fe3++NO↑+2H2O;1:1:4.
故答案为:O;C;B;P;Cl;
(2)在水中AgCl溶解度最小,故水溶液中硝酸银与氯化钡可以发生复分解反应,反应方程式为:2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2,
氨水中氯化钡溶解度为0,故氨水中氯化银与硝酸钡发生复分解反应,反应方程式为:2AgCl+Ba(NO3)2=BaCl2↓+2AgNO3,
故答案为:2AgNO3+BaCl2=2AgCl↓+Ba(NO3)2;2AgCl+Ba(NO3)2=BaCl2↓+2AgNO3;
(3)根据氧化性:HNO3>Fe3+>Cu2+,加入铁后会依次发生氧化还原反应,
①Fe+4HNO3═Fe(NO3)3+NO↑+2H2O,离子方程式为:Fe+4H++NO3-=Fe3++NO↑+2H2O,
②Fe+2Fe3+═3Fe2+;
③Fe+Cu2+═Cu+Fe2+;
从图象中可知铁为0.5mol时,无Fe2+生成,发生的反应①,消耗硝酸为2mol,生成Fe3+为0.5mol,
再加入0.5mol铁发生反应②,生成Fe2+物质的量为1.5mol,反应的Fe3+物质的量为1mol,其中原溶液中的Fe3+物质的量0.5mol,故原溶液有Fe3+物质的量为0.5mol,
从1.5mol~2mol消耗的0.5molFe与溶液中铜离子完全反应,故原溶液中Cu2+为0.5mol
故原溶液中Fe(NO3)3、Cu(NO3)2、HNO3分别为0.5mol、0.5mol、2mol,三者的浓度之比为0.5mol:0.5mol:2mol=1:1:4,
故答案为:HNO3、Fe(NO3)3、Cu(NO3)2;Fe+4H++NO3-=Fe3++NO↑+2H2O;1:1:4.
点评:本题考查较为综合,属于拼合型题目,涉及电负性的递变规律、沉淀转化、混合物计算等,(3)明确图象中每段发生的化学反应是解答本题的关键,侧重考查学生分析解决问题能力的考查,难度中等.

练习册系列答案
 A加金题 系列答案
A加金题 系列答案 全优测试卷系列答案
全优测试卷系列答案
相关题目
满足下列条件的同分异构体共有(不考虑立体异构)( )
①分子式为C5H10O3;
②等量的有机物与足量的NaHCO3溶液、Na反应时产生的气体在相同条件下的体积比为1:1.
①分子式为C5H10O3;
②等量的有机物与足量的NaHCO3溶液、Na反应时产生的气体在相同条件下的体积比为1:1.
| A、4种 | B、6种 |
| C、10种 | D、12种 |
同温同压下,A容器中氯化氢与B容器中氨气所含原子数相等,两容器体积之比为( )
| A、1:4 | B、2:1 |
| C、1:2 | D、4:1 |
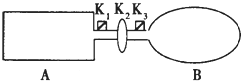 A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易传热的气球.关闭K2,将等量且少量的NO2通过K1、K3分别充人A、B中,反应起始时,A、B的体积均为V L.
A是由导热材料制成的密闭容器,B是一耐化学腐蚀且易传热的气球.关闭K2,将等量且少量的NO2通过K1、K3分别充人A、B中,反应起始时,A、B的体积均为V L.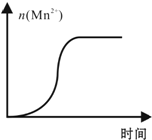 KMnO4酸性溶液与草酸(H2C2O4)溶液反应时,溶液紫色会逐渐褪去.某探究小组用测定此反应溶液紫色消失所需时间的方法,研究外界条件对反应速率的影响.该实验条件作如下限定:
KMnO4酸性溶液与草酸(H2C2O4)溶液反应时,溶液紫色会逐渐褪去.某探究小组用测定此反应溶液紫色消失所需时间的方法,研究外界条件对反应速率的影响.该实验条件作如下限定: