题目内容
Fe2O3、ZnO、CuO的固体混合粉末a g,在加热条件下用足量CO还原,得到金属混合物4.82g,将生成的CO2气体用足量的澄清石灰水吸收后,产生10.00g白色沉淀,则a的数值为
- A.14.82
- B.4.92
- C.6.42
- D.7.18
C
分析:根据反应方程式判断CO2中的O原子来源于CO和金属氧化物,CO2的物质的量等于金属氧化物中氧原子的物质的量,计算出氧化物中氧元素的质量,金属氧化物的质量等于金属的质量加氧化物中氧元素的质量.
解答:发生的有关反应为:Fe2O3+3CO 2Fe+3CO2,ZnO+CO
2Fe+3CO2,ZnO+CO Zn+CO2,CuO+CO
Zn+CO2,CuO+CO Cu+CO2,
Cu+CO2,
生成的CO2为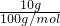 =0.1mol,从反应方程式可以看出,CO2中的O原子来源于CO和金属氧化物,CO2的物质的量等于金属氧化物中氧原子的物质的量,则氧化物中氧元素的物质的量为n(O)=0.1mol,故氧元素质量为0.1mol×16g/mol=1.6g,所以金属氧化物的质量为4.82gg+1.6g=6.42g,
=0.1mol,从反应方程式可以看出,CO2中的O原子来源于CO和金属氧化物,CO2的物质的量等于金属氧化物中氧原子的物质的量,则氧化物中氧元素的物质的量为n(O)=0.1mol,故氧元素质量为0.1mol×16g/mol=1.6g,所以金属氧化物的质量为4.82gg+1.6g=6.42g,
故选C.
点评:本题考查混合物的质量计算,题目难度中等,注意从元素质量守恒的角度分析,关键是确定CO2的物质的量等于金属氧化物中氧原子的物质的量.
分析:根据反应方程式判断CO2中的O原子来源于CO和金属氧化物,CO2的物质的量等于金属氧化物中氧原子的物质的量,计算出氧化物中氧元素的质量,金属氧化物的质量等于金属的质量加氧化物中氧元素的质量.
解答:发生的有关反应为:Fe2O3+3CO
 2Fe+3CO2,ZnO+CO
2Fe+3CO2,ZnO+CO Zn+CO2,CuO+CO
Zn+CO2,CuO+CO Cu+CO2,
Cu+CO2,生成的CO2为
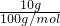 =0.1mol,从反应方程式可以看出,CO2中的O原子来源于CO和金属氧化物,CO2的物质的量等于金属氧化物中氧原子的物质的量,则氧化物中氧元素的物质的量为n(O)=0.1mol,故氧元素质量为0.1mol×16g/mol=1.6g,所以金属氧化物的质量为4.82gg+1.6g=6.42g,
=0.1mol,从反应方程式可以看出,CO2中的O原子来源于CO和金属氧化物,CO2的物质的量等于金属氧化物中氧原子的物质的量,则氧化物中氧元素的物质的量为n(O)=0.1mol,故氧元素质量为0.1mol×16g/mol=1.6g,所以金属氧化物的质量为4.82gg+1.6g=6.42g,故选C.
点评:本题考查混合物的质量计算,题目难度中等,注意从元素质量守恒的角度分析,关键是确定CO2的物质的量等于金属氧化物中氧原子的物质的量.

练习册系列答案
 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案
相关题目
Fe2O3、ZnO、CuO的固体混合粉末ag,在加热条件下用足量CO还原,得到金属混合物2.41g,将生成的CO2气体用足量的澄清石灰水吸收后,产生5.00g白色沉淀,则a的数值为( )
| A、7.41 | B、3.21 | C、2.46 | D、3.59 |