题目内容
下列说法中正确的是( )
| A、煤燃烧是化学能转化为光能的过程 |
| B、1 mol甲烷燃烧生成气态水和二氧化碳所放出的热量是甲烷的燃烧热 |
| C、HCl和NaOH反应的中和热△H=-57.3 kJ?mol-1,则H2SO4和Ca(OH)2反应的中和热△H=2×(-57.3)kJ?mol-1 |
| D、反应H2(g)+F2(g)═2HF(g);△H=-270 kJ?mol-1,说明在相同条件下,1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量 |
考点:反应热和焓变
专题:化学反应中的能量变化
分析:A、煤燃烧主要是把化学能转化为了热能和光能的过程;
B、燃烧热要求生成稳定的化合物;
C、中和热规定了产物水的物质的量为1mol;
D、反应物的总能量大于生成物的总能量为放热反应,△H<0.
B、燃烧热要求生成稳定的化合物;
C、中和热规定了产物水的物质的量为1mol;
D、反应物的总能量大于生成物的总能量为放热反应,△H<0.
解答:
解:A、煤燃烧主要是把化学能转化为了热能和光能的过程,故A错误;
B、101kp条件下,1 mol甲烷完全燃烧生成液态水和二氧化碳所放出的热量是甲烷的燃烧热,故B错误;
C、HCl和NaOH反应的中和热△H=-57.3 kJ?mol-1,则H2SO4和Ca(OH)2反应的中和热△H=-57.3kJ?mol-1,故C错误;
D、由热化学方程式可知该反应为放热反应,因此反应物的总能量(1 mol氢气与1 mol氟气的能量总和)大于生成物的总能量( 2mol氟化氢气体的能量),故D正确;
故选D.
B、101kp条件下,1 mol甲烷完全燃烧生成液态水和二氧化碳所放出的热量是甲烷的燃烧热,故B错误;
C、HCl和NaOH反应的中和热△H=-57.3 kJ?mol-1,则H2SO4和Ca(OH)2反应的中和热△H=-57.3kJ?mol-1,故C错误;
D、由热化学方程式可知该反应为放热反应,因此反应物的总能量(1 mol氢气与1 mol氟气的能量总和)大于生成物的总能量( 2mol氟化氢气体的能量),故D正确;
故选D.
点评:本题考查了热化学方程式的意义、吸热反应和放热反应、燃烧热、中和热的定义,综合性较强,注意中和热中和热规定了产物水的物质的量为1mol,与反应物的多少无关.

练习册系列答案
相关题目
pH值相同的下列溶液,其物质的量浓度最大的是( )
| A、HCl |
| B、H2SO4 |
| C、CH3COOH |
| D、H3PO4 |
下列物质属于芳香烃的是( )
| A、乙醇 | B、乙酸 | C、乙苯 | D、硝基苯 |
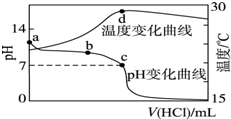 室温下,将1.000mol?L-1盐酸滴入20.00mL 1.000mol?L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )
室温下,将1.000mol?L-1盐酸滴入20.00mL 1.000mol?L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如图所示.下列有关说法正确的是( )| A、a点由水电离出的c(H+)<1.0×10-14mol/L |
| B、b点:n(NH4+)+n(NH3?H2O)>n(Cl-) |
| C、b点时加入的盐酸体积小于20.00mL,而c点时加入的盐酸体积大于20.00mL |
| D、d点后,温度略下降的主要原因是生成的NH4Cl水解吸热 |
下列各表述与示意图一致的是
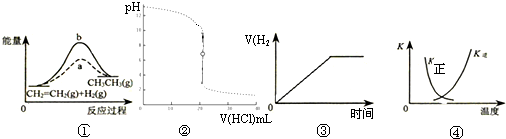

| A、图①中a、b曲线分别表示反应CH2=CH2(g)+H2(g)→CH3CH3(g)+Q使用和未使用催化剂时,反应过程中的能量变化 |
| B、图②表示25℃时,用0.1mol?L-1盐酸滴定20mL 0.1mol?L-1 NaOH溶液,溶液的pH随加入酸体积的变化 |
| C、图③表示锌粒与过量稀盐酸反应时,V(H2) 随时间的变化图 |
| D、图④中曲线表示反应2SO2(g)+O2(g)=2SO3(g)+Q 正、逆反应的平衡常数K随温度的变化 |
浓度是影响反应能否发生的因素之一.下列说法符合事实的是( )
| A、常温下,铝片可以溶解于足量浓硫酸,也可溶解于足量稀硫酸 |
| B、常温下,铜片与浓硝酸反应,不与稀硝酸反应 |
| C、常温下,浓的氢氧化钠溶液和极稀的氢氧化钠溶液均能溶解Al(OH)3 |
| D、加热条件下,MnO2能与浓盐酸反应生成氯气,与稀盐酸则不行 |
下列说法或表示法正确的是( )
| A、等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 |
| B、由C(石墨)→C(金刚石):△H=+119 kJ/mol可知,金刚石比石墨稳定 |
| C、已知2SO2(g)+O2(g)?2SO3(g)△H=196.64kJ/mol,在一定条件下向密闭容器中充人2molSO2和1molO2充分反应,最终放出的热量小于196.64kJ |
| D、在101 kPa时,2g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式可表示为2H2(g)+O2(g)=2H2O(l)△H=285.8 kJ/mol |
现有44g Mg、Al、Zn、Fe多种活泼金属粉末的混合物与1L含有一定质量的20%硫酸溶液恰好完全反应,得到无水盐140g,则下列说法正确的是( )
| A、电子转移为1mol |
| B、生成的气体体积(标准状况)为22.4 L |
| C、硫酸溶液的质量为540g |
| D、硫酸物质的量浓度为2mol/L |