��Ŀ����
11���������౻�㷺���������ߴ������ࡢ��������������ҽҩ��ҵ��ij�����ú�ú�̻ң���Ҫ�ɷ�ΪC��GeO2����������Al2O3��SiO2��Ϊԭ���Ʊ�GeO2����������ͼ��ʾ��
��֪��GeO2������ˮ��ϡ���ᣬ����ˮ��Ӧ����������Ϊ�����������������ǿ����Һ���������Σ�Ҳ����Ũ�������ɿ�����ˮ��GeCl4��GeCl4�ķе���83.1�棩��
��1����ˮ��ȡ������2Сʱ��Ŀ����Ϊ����ߺ������Ľ����ʣ�������X��������Ϊ���ò�����������̨��ţ�ǹܡ���ƿ��ʯ�������ƾ����ȱ�ٵIJ���������������ƿ���¶ȼơ������ܣ�
��2��д������ʱ�����������������Ʒ�����Ӧ�Ļ�ѧ����ʽ��2NaOH+GeO2$\frac{\underline{\;����\;}}{\;}$Na2GeO3+H2O��
��3�����ữ������Һ������Ũ��Ϊ5.3mol•L-1ʱ����������GeCl4��д���÷�Ӧ�Ļ�ѧ����ʽ��Na2GeO3+6HCl=2NaCl+3H2O+GeCl4������Һ���ữ��ʱ��Ȳ�������Һ��������ԵĻ��ǣ�ԭ����������H2GeO3����GeO2��GeO2•nH2O��������
��4��GeO2��Ʒ��ͨ����������SiO2��ȡ��Ʒw g�����������ԭ�ӵ����ʵ���Ϊn mol�������Ʒ��GeO2�����ʵ���Ϊ$\frac{w-30n}{45}$����$\frac{w}{45}$-$\frac{2}{3}$n��mol���ú�w��n�Ĵ���ʽ��ʾ����
���� GeO2������ˮ��ϡ���ᣬ����ˮ��Ӧ����������Ϊ���������������ú�̻ң���Ҫ�ɷ�ΪC��GeO2����������Al2O3��SiO2�����������ơ�̼���Ʊ��ղ���������̼�����ݷ�Ӧ���̿�֪��̼������������෴Ӧ���������ƺͶ�����̼������������������෴Ӧ���������ƺ�ˮ�����պ�IJ�������ơ�Al2O3��SiO2��ˮ��ȡ2Сʱ�������Һ�м����Ტ����PHֵ���������費�����ᣬ���ɵ�������ת���������������������˳�ȥ�������������Һ�м��������ữ�������������ᷴӦ����GeCl4��GeCl4�ķе�ͣ�ͨ������õ�GeCl4��GeCl4��ߴ�ˮ��Ӧ����GeO2•nH2O����һ�ֲ���ΪHCl��GeO2•nH2Oʧˮ�õ�GeO2���ݴ˷������
��1��ˮ��ȡ�������ʱ��ϳ�������ʹ�������к�����ᄀ�����ܽ⣻GeCl4�ķе�ͣ�ͨ������õ�GeCl4����������ʵ�������
��2��GeO2������ˮ��ϡ���ᣬ����ˮ��Ӧ����������Ϊ���������������֪�����������������Ʒ�Ӧ���������ƺ�ˮ��
��3��GeO2��һ��������ˮ��ƫ�����Ե��������������������������ʣ���H2GeO3�ܹ����Ȼ��ⷴӦ����������ΪGeCl4��NaCl��ˮ�������Ȳ������������������ӷ�Ӧ������������H2GeO3����GeO2��GeO2•nH2O����������H2GeO3����GeO2��GeO2•nH2O��ˮ���ܽ�Ȳ������Գ��ֻ�������
��4����wg��Ʒ�к�SiO2��GeO2�����ʵ����ֱ�Ϊx��y��������ԭ���غ�������غ���m=nM��ʽ���㣮
��� �⣺GeO2������ˮ��ϡ���ᣬ����ˮ��Ӧ����������Ϊ���������������ú�̻ң���Ҫ�ɷ�ΪC��GeO2����������Al2O3��SiO2�����������ơ�̼���Ʊ��ղ���������̼�����ݷ�Ӧ���̿�֪��̼������������෴Ӧ���������ƺͶ�����̼������������������෴Ӧ���������ƺ�ˮ�����պ�IJ�������ơ�Al2O3��SiO2��ˮ��ȡ2Сʱ�������Һ�м����Ტ����PHֵ���������費�����ᣬ���ɵ�������ת���������������������˳�ȥ�������������Һ�м��������ữ�������������ᷴӦ����GeCl4��GeCl4�ķе�ͣ�ͨ������õ�GeCl4��GeCl4��ߴ�ˮ��Ӧ����GeO2•nH2O����һ�ֲ���ΪHCl��GeO2•nH2Oʧˮ�õ�GeO2��
��1����ˮ��ȡ�����ﳤ��2Сʱ��Ŀ����Ϊ�˾�����ʹ���ջ�����еĺ����������ˮ���Ӷ���ߺ������Ľ����ʣ�GeCl4�ķе���83.1�棬��е�ϵͣ�����Һ�з����GeCl4������ͨ���������������ɣ�����Ҫ�õ�������������̨��ţ�ǹܡ���ƿ��ʯ�������ƾ��ƣ���Ҫ������ƿ���¶ȼơ������ܣ�
�ʴ�Ϊ��Ϊ����ߺ������Ľ����ʣ�����������ƿ���¶ȼơ������ܣ�
��2��GeO2������ˮ��ϡ���ᣬ����ˮ��Ӧ����������Ϊ���������������֪�����������������Ʒ�Ӧ���������ƺ�ˮ����Ӧ����ʽΪ��2NaOH+GeO2$\frac{\underline{\;����\;}}{\;}$Na2GeO3+H2O��
�ʴ�Ϊ��2NaOH+GeO2$\frac{\underline{\;����\;}}{\;}$Na2GeO3+H2O��
��3��GeO2��һ��������ˮ��ƫ�����Ե��������������������������ʣ���H2GeO3�ܹ����Ȼ��ⷴӦ����������ΪGeCl4��NaCl��ˮ����Ӧ�Ļ�ѧ����ʽΪ��Na2GeO3+6HCl=2NaCl+3H2O+GeCl4������Һ���ữ��ʱ��Ȳ�����Na2GeO3�������ӷ�Ӧ������������H2GeO3����GeO2��GeO2•nH2O����������H2GeO3����GeO2��GeO2•nH2O����ˮ���ܽ�Ƚ�С��������Һ��������ԵĻ��ǣ�
�ʴ�Ϊ��Na2GeO3+6HCl=2NaCl+3H2O+GeCl4��������H2GeO3����GeO2��GeO2•nH2O��������
��4����wg��Ʒ�к�SiO2��GeO2�����ʵ����ֱ�Ϊx��y�����O�����ʵ���Ϊn mol��������ԭ���غ�ɵã�2x+2y=n �٣����������غ�ɵã�60x+105y=w�ڣ�
���٢ڿɵ�y=$\frac{w-30n}{45}$����$\frac{w}{45}$-$\frac{2}{3}$n����
�ʴ�Ϊ��$\frac{w-30n}{45}$����$\frac{w}{45}$-$\frac{2}{3}$n����
���� ����ͨ����GeO2���Ʊ����̣������������Ʊ���������Ʒ�������Ŀ�Ѷ��еȣ���������д��ѧ����ʽ��֪ʶ��϶࣬���ؼ��Ǹ����Ʊ�������ȷ�жϷ�Ӧ������Ȼ�����������غ㶨����д������ʽ���ɣ���������������ѧ���ķ������������������Ӧ����ѧ֪ʶ���ʵ�������������

 ��Ӣ���㿨ϵ�д�
��Ӣ���㿨ϵ�д�����һ��
���϶���
| ���� | �۵�/�� | �е�/�� | �ܶ�/g•cm-3 | �ܽ��� |
| �Ҷ����� C2H6O2�� | -11.5 | 198 | 1.11 | ������ˮ���Ҵ� |
| ��������C3H8O3�� | 17.9 | 290 | 1.26 | �ܸ�ˮ���ƾ�������Ȼ��� |
A������ B����ȡ�� C�����ܽ⡢�ᾧ�����ˡ��ķ��� D����Һ��
��1����������Ȼ��ƺʹ���Ļ�����з�����������Ӧ��C��
��2�����Ҷ����ͱ�������������ѷ�����A��
��3�������л��ܼ�CCl4ʱ��Ҳ���ȡ����ķ���������ʵ��װ��ͼ�еĴ���֮���У�
���¶ȼ��¶˵�ˮ�����ܲ�����Һ��
�������ܽ���ˮ�ķ���ߵ�
�ۼ����ձ�δ����ʯ����
��ͼ������������ʱ��ʹ��ˮ�ܼ����ȵĺô������Ⱦ��ȣ����ڿ����¶ȣ�


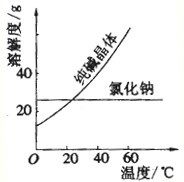
��֪ZnSO4���ܽ�������ʾ��
| �¶�/�� | 0 | 10 | 20 | 30 | 40 | 60 | 80 | 100 |
| �ܽ��/g | 41.6 | 47.5 | 53.8 | 61.3 | 70.5 | 75.4 | 71.1 | 60.5 |
��2�����������Ҫ�ɷ�ΪPbSO4��X�Ļ�ѧʽΪZnO��Zn��OH��2��
��3���ܽ�����м����ϡ������������Ʊ�ZnSO4������ZnSO4ˮ�⣮
��4���ᾧ�IJ���Ϊ����Ũ������ȴ�ᾧ��
��5���þƾ�����ϴ�ӵ�ԭ���Ǽ�������п�������ʧ�������
| A�� | H+��Fe2+��NO3-��SO42- | B�� | Al3+��Na+��SO42-��HCO3- | ||
| C�� | Na+��Ca2+��Cl-��SO42- | D�� | Fe3+��K+��SCN-��Cl- |


