题目内容
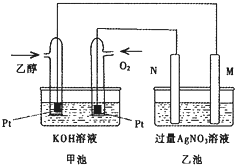 如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:(1)M电极的材料是
(2)在此过程中,乙池中某一电极析出金属银4.32g时,甲池中理论上消耗氧气为
考点:原电池和电解池的工作原理
专题:电化学专题
分析:(1)碱性乙醇燃料电池中通入乙醇的一极为原电池的负极,通入氧气的一极为原电池的正极,乙池为电解池,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,N连接原电池的正极,应为电解池的阳极,则应为石墨材料,M为电解池的阴极,为铁电极,据此解答即可;
(2)结合电子的转移的物质的量的判断进行计算.
(2)结合电子的转移的物质的量的判断进行计算.
解答:
解:(1)碱性乙醇燃料电池中通入乙醇的一极为原电池的负极,负极上乙醇失电子发生氧化反应,电极反应式为C2H5OH-12e-+16OH-=2CO32-+11H2O,通入氧气的一极为原电池的正极,电极反应式为:4OH--4e-═2H2O+O2↑,乙池为电解池,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,N连接原电池的正极,应为电解池的阳极,则应为石墨材料,N为阳极,电极反应式是4OH--4e-=O2↑+2H2O,M为阴极,电极材料是Fe,
故答案为:铁;阴极;4OH--4e-═2H2O+O2↑;C2H5OH-12e-+16OH-=2CO32-+11H2O;
(2)n(Ag)=
=0.04mol,根据Ag++e-=Ag可知转移电子为0.04mol,甲池中通入氧气的一极为正极,反应式为2O2+8H++8e-=4H2O,则消耗n(O2)=
×0.04mol=0.01mol,V(O2)=0.01mol×22.4L/mol=0.224L,故答案为:0.224.
故答案为:铁;阴极;4OH--4e-═2H2O+O2↑;C2H5OH-12e-+16OH-=2CO32-+11H2O;
(2)n(Ag)=
| 4.32g |
| 108g/mol |
| 1 |
| 4 |
点评:本题考查了原电池原理和电解池原理,明确原电池和电解池电极上发生反应的类型即可分析解答本题,题目难度中等.

练习册系列答案
相关题目
已知氧化性Fe3+>Cu2+,向FeCl3、CuCl2的混合溶液中加入铁粉,充分反应后仍有固体存在,则下列判断不正确的是( )
| A、溶液中一定含有Fe2+ |
| B、溶液中一定含Cu2+ |
| C、剩余固体中一定含铜 |
| D、加入KSCN溶液一定不变红色 |
保护地下钢管不受腐蚀,可使它连接( )
| A、铜板 | B、石墨 |
| C、直流电源负极 | D、直流电源正极 |
下列事实不能用电化学理论解释的是( )
| A、轮船水线以下的船壳上装一定数量的锌块 |
| B、铁可以在氯气中燃烧 |
| C、纯锌与稀硫酸反应时,滴入少量硫酸铜溶液后速率加快 |
| D、镀锌的铁比镀锡的铁耐用 |
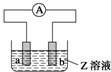 如图中a、b分别是原电池的两极,接通电路后发现a极板质量增加,b极板溶解,
如图中a、b分别是原电池的两极,接通电路后发现a极板质量增加,b极板溶解,符合这一情况的是( )
| a极板 | b极板 | a电极 | Z溶液 | |
| A | 锌 | 石墨 | 负极 | CuSO4 |
| B | 石墨 | 石墨 | 负极 | NaOH |
| C | 银 | 铁 | 正极 | AgNO3 |
| D | 铜 | 石墨 | 正极 | CuCl2 |
| A、A | B、B | C、C | D、D |
下列描述违背化学原理的是( )
| A、“冰,水为之,而寒于水”说明相同质量的水和冰,水的能量高 |
| B、反应A(g)+3B(g)?2C(g)达平衡后,温度不变,增大压强,平衡正向移动,平衡常数K值增大 |
| C、SO2的催化氧化是一个放热的反应,升高温度,反应速率加快 |
| D、电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑ |
45mL某气体,可能含有CO2、O2、NH3将其通过浓硫酸,气体体积无变化,通过足量的Na2O2后,体积变为30mL,则该气体的组成为( )
| A、CO2为30mL,O2为15mL |
| B、NH3为30mL,O2为15mL |
| C、CO2为15mL,O2为30mL |
| D、CO2 为30mL,O2为15mL |
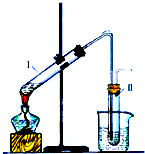 如图是实验室制取溴乙烷的装置示意图,烧杯中装有自来水,试管I和试管II中均事先装有少量蒸馏水.请回答下列问题:
如图是实验室制取溴乙烷的装置示意图,烧杯中装有自来水,试管I和试管II中均事先装有少量蒸馏水.请回答下列问题: