题目内容
下列有关说法正确的是( )
| A、将Al2(SO4)3溶液蒸干得到Al2(SO4)3固体 |
| B、用广泛pH试纸测得某溶液pH为11.3 |
| C、向纯水通入少量HCl气体,水的电离程度减小,Kw减小 |
| D、向0.1 mol?L-1 CH3COOH溶液中加少量水,溶液中所有离子的浓度都减小 |
考点:盐类水解的应用,弱电解质在水溶液中的电离平衡,水的电离,试纸的使用
专题:基本概念与基本理论
分析:A.硫酸没有挥发性;
B.pH试纸测定溶液pH为整数;
C.酸或碱抑制水电离,水的离子积常数只与温度有关;
D.加水稀释促进醋酸电离,溶液中氢氧根离子浓度增大.
B.pH试纸测定溶液pH为整数;
C.酸或碱抑制水电离,水的离子积常数只与温度有关;
D.加水稀释促进醋酸电离,溶液中氢氧根离子浓度增大.
解答:
解:A.硫酸没有挥发性,所以将Al2(SO4)3溶液蒸干得到Al2(SO4)3固体,故A正确;
B.pH试纸测定溶液pH为整数,所以用广泛pH试纸不可能测得某溶液pH为11.3,故B错误;
C.酸或碱抑制水电离,水的离子积常数只与温度有关,温度不变,水的离子积常数不变,故C错误;
D.加水稀释促进醋酸电离,溶液中氢离子浓度减小,温度不变,水的离子积常数不变,则溶液中氢氧根离子浓度增大,故D错误;
故选A.
B.pH试纸测定溶液pH为整数,所以用广泛pH试纸不可能测得某溶液pH为11.3,故B错误;
C.酸或碱抑制水电离,水的离子积常数只与温度有关,温度不变,水的离子积常数不变,故C错误;
D.加水稀释促进醋酸电离,溶液中氢离子浓度减小,温度不变,水的离子积常数不变,则溶液中氢氧根离子浓度增大,故D错误;
故选A.
点评:本题考查较综合,涉及pH试纸测定pH值、盐类水解、弱电解质的电离等知识点,根据盐类水解特点、弱电解质电离特点等知识点分析解答,易错选项是D,注意:水的离子积常数只与温度有关,与溶液酸碱性及浓度无关,为易错点.

练习册系列答案
 普通高中同步练习册系列答案
普通高中同步练习册系列答案 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案
相关题目
下列各组离子一定能在无色溶液中大量共存的是( )
| A、Na+、CO32-、NO3-、AlO2- | ||
| B、K+、H+、CrO42-、SO32- | ||
C、Al3+、Ba2+、HCO
| ||
| D、Fe3+、Mg2+、SCN-、Cl- |
下列关于稀硫酸的叙述正确的是( )
| A、能作气体干燥剂 |
| B、其中硫元素的化合价是+6价 |
| C、具有脱水性 |
| D、属于一元强酸 |
下列说法正确的是( )
| A、强电解质溶液一定比弱电解质溶液的导电性强 |
| B、强电解质的水溶液中不存在电解质分子 |
| C、强电解质都是离子化合物,弱电解质都是共价化合物 |
| D、不同的弱电解质只要物质的量浓度相同,电离程度也就相同 |
将标准状况下3.36L CO2缓慢通入1L 0.2mol?L-1的NaOH溶液中,气体被充分吸收,下列关系不正确的是( )
| A、c(Na+)+c(H+)=c(OH-)+c(HCO3-)+2c(CO32-) |
| B、3c(Na+)=4[c (H2CO3)+c(HCO3-)+c(CO32-)] |
| C、c(Na+)>c(CO32-)>c(HCO3-)>c(OH-)>c(H+) |
| D、3c(OH-)+2 c(CO32-)=c(HCO3-)+4c(H2CO3)+3c(H+) |
标准状况下,两个容积相等的贮气瓶,一个装有O2,另一个装有O3,两瓶气体具有相同的( )
| A、质量 | B、原子总数 |
| C、密度 | D、分子数 |
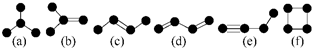 如图所示是4个碳原子相互结合的方式.小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合.则下列说法中正确的是( )
如图所示是4个碳原子相互结合的方式.小球表示碳原子,小棍表示化学键,假如碳原子上其余的化学键都是与氢结合.则下列说法中正确的是( )| A、一个有机物a分子中含有8个氢原子 |
| B、有机物b、c、f互为同分异构体 |
| C、有机物d、e的1H核磁共振谱中,特征峰的数目相同 |
| D、有机物b、c、e中4个碳原子可处于同一平面 |
下列试剂加入少量溴水充分振荡后,上层几乎无色的是( )
| A、己烷 | B、溴苯 | C、乙醇 | D、甲苯 |