题目内容
18.已知氯、溴、碘三种元素原子的最外层电子数相同.溴元素有两种稳定的核素,分别是79Br和81Br,回答下列问题:(1)写出氯离子结构示意图
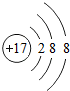 ;
;(2)写出与Cl-具有相同电子层结构(核外电子排布相同)的一种离子:
 ;
;(3)4.04g由 ${\;}_{20}^{40}$Ca和 ${\;}_{35}^{81}$Br组成的溴化钙中所含质子数为1.8NA.
分析 (1)氯离子为氯原子得到1个电子形成的微粒,核内质子数为17,核外电子数为18,核外分3个电子层,结合核外电子排布规律书写;
(2)Cl-具有相同电子层结构,即核外电子数为18,核外有3个电子层,第一层上有2个电子,第二层上有8个电子,第三层上有8个电子,如硫离子符合条件;
(3)根据由 ${\;}_{20}^{40}$Ca和 ${\;}_{35}^{81}$Br组成的溴化钙中式量为202,1molCaBr2中含质子数为90NA计算.
解答 解:(1)氯离子的核内质子数为17,核外电子数为18,核外有3个电子层,第一层上有2个电子,第二层上有8个电子,第三层上有8个电子,其结构示意图为: ,
,
故答案为: ;
;
(2)S2-是硫原子得到2个电子得到的,其核外有18个电子,有3个电子层,与氯离子电子层排布相同,其结构示意图为: ,
,
故答案为: ;
;
(3)4.04g由 ${\;}_{20}^{40}$Ca和 ${\;}_{35}^{81}$Br组成的溴化钙的物质的量为$\frac{4.04g}{202g/mol}$=0.02mol,1molCaBr2中含质子数为90NA,则4.04g由 ${\;}_{20}^{40}$Ca和 ${\;}_{35}^{81}$Br组成的溴化钙中所含质子数为0.02mol×90NA=1.8NA,
故答案为:1.8NA.
点评 本题考查常用化学用语的书写,掌握原子的核外电子排布、微粒符号的意义是正确解答本题的关键,本题难度不大.

练习册系列答案
相关题目
8.下列反应的离子方程式正确的是( )
| A. | 往Na[Al(OH)4]溶液中通入过量CO22[Al(OH)4]-+CO2=2Al(OH)3↓+CO32-+H2O | |
| B. | Na2SiO3溶液与稀醋酸混合SiO32-+2H+=H2SiO3↓ | |
| C. | 钠与CuSO4溶液反应2Na+Cu2+=Cu+2Na+ | |
| D. | 往Na2SO3溶液中滴加双氧水 H2O2+SO32-=SO42-+H2O |
9.用NA表示阿伏加德罗常数的值.下列说法中正确的是( )
| A. | 2.4g金属镁变成镁离子时失去的电子数为0.1NA | |
| B. | 标准状况下,11.2L CCl4所含的分子数为0.5NA | |
| C. | 0.5mol/L AlCl3溶液中Cl-的数目为1.5NA | |
| D. | 17g氨气中含有的电子数为10NA |
6.钛(Ti)在生产生活中应用十分广泛,以TiO2制取Ti的主要反应如下:
①TiO2+2Cl2+2C$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO; ②TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$2MgCl2+Ti
有关说法错误的是( )
①TiO2+2Cl2+2C$\frac{\underline{\;高温\;}}{\;}$TiCl4+2CO; ②TiCl4+2Mg$\frac{\underline{\;高温\;}}{\;}$2MgCl2+Ti
有关说法错误的是( )
| A. | 反应①是置换反应 | B. | ①②均属于氧化还原反应 | ||
| C. | 每消耗1mol TiO2会生成56g CO | D. | 反应②中镁元素化合价升高 |
13.以下分散系,不会出现丁达尔现象的是( )
| A. | 鸡蛋清溶液 | B. | 淀粉溶液 | C. | 食盐水 | D. | 雾 |
3.“如果改变影响平衡的条件之一,平衡将向着能够减弱这种改变的方向移动”总结出这条经验规律的科学家是( )
| A. | 门捷列夫 | B. | 盖斯 | C. | 勒夏特列 | D. | 范德华 |
7. 实验室保存下列试剂时应使用如图装置的是( )
实验室保存下列试剂时应使用如图装置的是( )
 实验室保存下列试剂时应使用如图装置的是( )
实验室保存下列试剂时应使用如图装置的是( )| A. | 硝酸银固体 | B. | 烧碱溶液 | C. | 浓硝酸 | D. | 氢氟酸 |
12.下列实验设计不能达到实验目的是( )
| 选项 | 实验设计 | 实验目的 |
| A | 过氧化钠与水反应 | 制备少量干燥的氧气 |
| B | 取铁在氧气中充分燃烧后的固体产物溶于稀硫酸,加KSCN溶液 | 检验铁的燃烧产物中含+3价铁 |
| C | 分别取大小相近的钠粒、钾粒投入水中,观察反应的剧烈程度 | 比较钠、钾的还原性强弱 |
| D | 将CO2气体通入Na2SiO3溶液中 | 比较C、Si元素非金属性的强弱 |
| A. | A | B. | B | C. | C | D. | D |