题目内容
7.下列物质属于有机物的是( )| A. | CH4 | B. | CO2 | C. | NaHCO3 | D. | CH3COOH |
分析 有机物是指含有碳元素的化合物.无机物是指不含有碳元素的化合物.一氧化碳、二氧化碳、碳酸盐等物质中虽然含有碳元素,但是这些物质的性质和无机物相似,把它们归入无机物.
解答 解:A.CH4是含有碳元素的化合物,属于有机物,故A正确;
B.CO2虽然含有碳元素,但是CO2的性质和无机物相似,属于无机物,故B错误;
C.NaHCO3虽然含有碳元素,但是CO2的性质和无机物相似,属于无机物,故C错误;
D.CH3COOH是含有碳元素的化合物,属于有机物,故D正确.
故选AD.
点评 本题考查有机物和无机物的区别,难度不大,掌握有机物与无机物的概念、特征等是正确解答此类题的关键.

练习册系列答案
相关题目
18.下列变化属于化学变化的是( )
| A. | 蒸馏法分离酒精与水 | B. | 食物腐烂 | ||
| C. | 过滤除去水中的泥沙 | D. | 分液法分离四氯化碳与水 |
15.一定体积的KMnO4溶液恰好能氧化一定质量的KHC2O4•H2C2O4•2H2O.若用0.1000mol/L的NaOH溶液中和相同质量的KHC2O4•H2C2O4•2H2O,所需NaOH溶液的体积恰好为KMnO4溶液的6倍,则KMnO4溶液的浓度(mol/L)为( )
提示:①H2C2O4是二元弱酸
②10[KHC2O4•H2C2O4]+8KMnO4+17H2SO4═8MnSO4+9K2SO4+40CO2↑+32H2O.
提示:①H2C2O4是二元弱酸
②10[KHC2O4•H2C2O4]+8KMnO4+17H2SO4═8MnSO4+9K2SO4+40CO2↑+32H2O.
| A. | 0.0800 | B. | 0.1200 | C. | 0.1600 | D. | 0.2400 |
16.下列反应的离子方程式,正确的是( )
| A. | Fe溶于稀盐酸:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 用小苏打治疗胃酸过多:CO32-+2H+═CO2↑+H2O | |
| C. | 用FeCl3溶液腐蚀印刷电路板上铜箔:Fe3++Cu═Fe2++Cu2+ | |
| D. | 铝与浓氢氧化钠溶液反应:2Al+2OH-+2H2O═2AlO2-+3H2↑ |

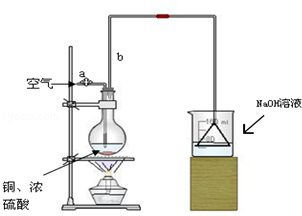 某学校课外活动小组针对教材中铜与浓硫酸反应,提出了“能够与铜反应的硫酸的最低浓度是多少?”的探究课题,并设计了如下方案进行实验:实验试剂:18mol/L硫酸20mL,纯铜粉足量,足量2mol/LNaOH溶液.
某学校课外活动小组针对教材中铜与浓硫酸反应,提出了“能够与铜反应的硫酸的最低浓度是多少?”的探究课题,并设计了如下方案进行实验:实验试剂:18mol/L硫酸20mL,纯铜粉足量,足量2mol/LNaOH溶液.