��Ŀ����
15��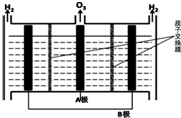 NO������⻯ѧ�������ƻ������㣮����NO�ж��ַ�������������ش��������⣺
NO������⻯ѧ�������ƻ������㣮����NO�ж��ַ�������������ش��������⣺�����ô�������β���е�NO��COת���CO2��N2����ѧ����ʽ���£�
2NO��g��+2CO��g�� $\stackrel{����}{?}$ 2CO2��g��+N2��g����H=-748kJ/mol
Ϊ�˲ⶨij���������µķ�Ӧ���ʣ���һ���¶��£���ij�����ܱ������г�������ʵ�����NO��CO����������Ӧ�������崫������ò�ͬʱ��NOŨ�������
| ʱ�䣨s�� | 0 | 1 | 2 | 3 | 4 | �� |
| c��NO��/mol•L-1 | 1.00��10-3 | 4.00��10-4 | 1.70��10-4 | 1.00��10-4 | 1.00��10-4 | �� |
��2���ﵽƽ��ʱ�����д�ʩ�����NOת���ʵ���BD��������ĸ��ţ�
A��ѡ�ø���Ч�Ĵ���B�����ͷ�Ӧ��ϵ���¶�
C���������ʹ������ѹǿ����D������COʹ������ѹǿ����
��3����֪N2��g��+O2��g��=2NO��g����H=+180kJ/mol����CO��ȼ����Ϊ284kJ/mol��
����Ҳ�����ڴ���NO��
��4��O3����NO���ˮϴ�ɲ���HNO3��O2��ÿ����1mol��HNO3ת��3mol���ӣ�
��5��O3���ɵ��ϡ�����Ƶã�ԭ����ͼ��ͼ������ΪB���A����B���������������Ե缫���ĵ缫��ӦʽΪ3H2O-6e-=O3+6H+��
���� ��1�����ݱ������������ǰ2s�ڵ�ƽ����Ӧ���ʦԣ�NO��=��1.00��10-3-1.70��10-4 ����2=4.15��10-4mol/��L•s�������ݻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ��ԣ�N2��=1/2�ԣ�NO��=2.08��10-4 mol/��L•s�����ɱ������ݿ�����3s��c��NO���������ƽ�⣬��ʱc��CO��=1.00��10-4mol•L-1��c��CO2��=1.00��10-3mol•L-1 -1.00��10-4mol•L-1=9.00��10-4mol•L-1��c��N2��=1/2c��CO2��=4.50��10-4mol•L-1������K=c��CO2��2��c��N2��/��c��NO��2��c��CO��2��=3.65��106��
��2���ﵽƽ��ʱ��Ҫ���NOת���ʣ����ı�����Ҫʹƽ�������ƶ���
A��ѡ�ø���Ч�Ĵ�����ƽ�ⲻ�ƶ�����A����
B�����ͷ�Ӧ��ϵ���¶ȣ��÷�ӦΪ���ȷ�Ӧ�������ƶ�����B��ȷ��
C���������ʹ������ѹǿ����ƽ�ⲻ�ƶ�����C����
D������COʹ������ѹǿ�����൱������COŨ�ȣ�ƽ�������ƶ���NOת������ߣ���D��ȷ��
��3������֪���̢�2NO��g��+2CO��g��=2CO2��g��+N2��g����H=-748kJ/mol����N2��g��+O2��g��=2NO��g����H=+180kJ/mol�����ݸ�˹���ɢ١�2+�ڡ�2��CO��ȼ���ȵ��Ȼ�ѧ����ʽΪCO��g��+1/2O2��g��=CO2��g����H=��-748kJ/mol����2+��+180kJ/mol����2=-284 kJ/mol��
��4��O3����NO���ˮϴ�ɲ���HNO3��O2��ת�Ƶ�����=���ϼ���������NOת��ΪHNO3 �����ϼ�����3��ÿ����1mol��HNO3ת��3mol����
��5��������֪ͼ��A����������O3��B����������H2��˵��A��������������ӦΪ������B��������ԭ��ӦΪ���������������Ե缫���ĵ缫��ӦʽΪ3H2O-6e-=O3+6H+
��� ���1�����ݱ������������ǰ2s�ڵ�ƽ����Ӧ���ʦԣ�NO��=��1.00��10-3-1.70��10-4 ����2=4.15��10-4mol/��L•s�������ݻ�ѧ��Ӧ����֮�ȵ��ڻ�ѧ������֮�ȣ��ԣ�N2��=1/2�ԣ�NO��=2.08��10-4 mol/��L•s�����ɱ������ݿ�����3s��c��NO���������ƽ�⣬��ʱc��CO��=1.00��10-4mol•L-1��c��CO2��=1.00��10-3mol•L-1 -1.00��10-4mol•L-1=9.00��10-4mol•L-1��c��N2��=1/2c��CO2��=4.50��10-4mol•L-1������K=c��CO2��2��c��N2��/��c��NO��2��c��CO��2��=3.65��106��
�ʴ�Ϊ��2.08��10-4 mol/��L•s����3.65��106��
��2���ﵽƽ��ʱ��Ҫ���NOת���ʣ����ı�����Ҫʹƽ�������ƶ���
A��ѡ�ø���Ч�Ĵ�����ƽ�ⲻ�ƶ�����A����
B�����ͷ�Ӧ��ϵ���¶ȣ��÷�ӦΪ���ȷ�Ӧ�������ƶ�����B��ȷ��
C���������ʹ������ѹǿ����ƽ�ⲻ�ƶ�����C����
D������COʹ������ѹǿ�����൱������COŨ�ȣ�ƽ�������ƶ���NOת������ߣ���D��ȷ��
�ʴ�Ϊ��BD��
��3������֪���̢�2NO��g��+2CO��g��=2CO2��g��+N2��g����H=-748kJ/mol����N2��g��+O2��g��=2NO��g����H=+180kJ/mol�����ݸ�˹���ɢ١�2+�ڡ�2��CO��ȼ���ȵ��Ȼ�ѧ����ʽΪCO��g��+1/2O2��g��=CO2��g����H=��-748kJ/mol����2+��+180kJ/mol����2=-284 kJ/mol��
�ʴ�Ϊ��284 kJ/mol���H=-284kJ/mol��
��4��O3����NO���ˮϴ�ɲ���HNO3��O2��ת�Ƶ�����=���ϼ���������NOת��ΪHNO3 �����ϼ�����3��ÿ����1mol��HNO3ת��3mol���ӣ��ʴ�Ϊ��3��
��5��������֪ͼ��A����������O3��B����������H2��˵��A��������������ӦΪ������B��������ԭ��ӦΪ���������������Ե缫���ĵ缫��ӦʽΪ3H2O-6e-=O3+6H+���ʴ�Ϊ��B��3H2O-6e-=O3+6H+��
���� ���⿼���˷�Ӧ���ʡ�ƽ�ⳣ����ת���ʵļ��㣬��Ӧ�����仯�ķ����жϺ��Ȼ�ѧ����ʽ����д����ѧƽ���Ӱ�����ط���Ӧ�ã�ƽ�ⳣ�����㣬�缫����ʽ����д�ȣ����ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�

 �ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�
�ϴ�̸�������������νӽ̳��Ͼ���ѧ������ϵ�д�| A�� | ������백ˮ�У�H++OH-�TH2O | |
| B�� | ̼�������Һ����������������Һ��ϣ�HCO3-+OH-�TCO32-+H2O | |
| C�� | ����������Һ��ͨ�������������SO2+OH-�THSO3- | |
| D�� | ̼����ܽ���ϡ�����У�CO32-+2H+�TCO2��+H2O |
CrO42-$��_{ת��}^{H+}$Cr2O72-$��_{��ԭ}^{Fe_{2}+}$Cr3+$��_{����}^{OH-}$Cr��OH��3��
��֪ת�������еķ�ӦΪ��2CrO42-��aq��+2H+��aq���TCr2O72-��aq��+H2O��1����ת����������Һ�и�Ԫ�غ���Ϊ28.6g/L��CrO42-��10/11ת��ΪCr2O72-������˵������ȷ���ǣ�������
| A�� | ת�������У�����c��H+����ƽ��������Ӧ�����ƶ���CrO42-��ת������� | |
| B�� | ������Ksp[Cr��OH��3]=1��10-32��Ҫʹ�������ˮ��c��Cr3+������1��10-5mol/L��Ӧ����Һ��pH=5 | |
| C�� | �����̷���FeSO4•7H2O����M=278������ԭ��������1L��ˮ��������Ҫ917.4g | |
| D�� | ������ת����Ӧ��ƽ�ⳣ��K=104����ת����������Һ��pH=1 |
| A�� | ��ˮ�е����̪��Һ����Һ��죺NH3•H2O=NH4++OH- | |
| B�� | 90��ʱ����ô�ˮ��c��H+��•c��OH-��=3.8��10-13��H2O��l��?H+��aq��+OH-��aq����H��0 | |
| C�� | ������Һ��ͨ��CO2����Һ����ǣ�2C6H5ONa+CO2+H2O��2C6H5OH+Na2CO3 | |
| D�� | FeCl3��Һ��ͨ��SO2����Һ��ɫ��ȥ��2Fe3++SO2 +2H2O=2Fe2++SO42-+4H+ |
| ѡ�� | �������� | �������� | Ԥ����е����� | 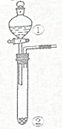 |
| A | ϡ���� | Ũ̼������Һ | ������������ | |
| B | Ũ���� | ��ɰֽ��ĥ�������� | ������������ɫ���� | |
| C | �Ȼ�������Һ | �������ƹ��� | ��������ͺ��ɫ���� | |
| D | ����������Һ | ��������ĩ | ������ɫ���� |
| A�� | A | B�� | B | C�� | C | D�� | D |
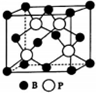 �����ס�����ͬ��Ԫ�أ�����Ԫ�ص��ʼ��仯������ũҩ�����ʵȷ�������ҪӦ�ã�
�����ס�����ͬ��Ԫ�أ�����Ԫ�ص��ʼ��仯������ũҩ�����ʵȷ�������ҪӦ�ã�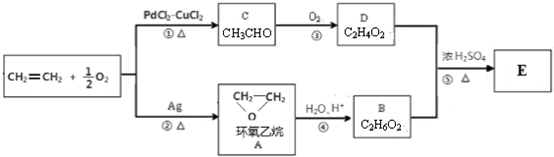
 ��
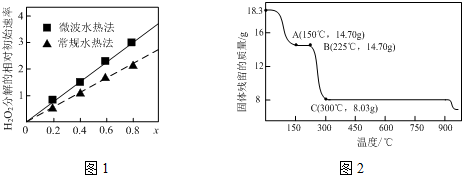
��
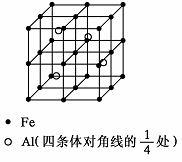 �������ڹ���Ԫ��Fe��Ti����C��H��N��O�γɶ��ֻ����
�������ڹ���Ԫ��Fe��Ti����C��H��N��O�γɶ��ֻ����