��Ŀ����
2��ij��ѧ��ȤС���ڼ������������ö������̺�Ũ���ᷴӦ����ȡ���ռ���������1����Ҫ��ȡ���������������Ӧʹ��������ͨ��װ�б���ʳ��ˮ��Ũ�����ϴ��ƿ��
��2��ijͬѧ������MnO2��KCl��ĩ����ˣ�����û����ķ����Ͳ������£��벹��������������ʢ�л�Ϸ�ĩ���ձ��м���������ˮ�ܽ⣻�ڽ������õĻ������ˣ��ò������ò���������©�������������ձ�����ϴ�ӡ���������õ�MnO2�����ڢڲ���������Һ�������ᾧ����������ƣ��õ�KCl���壮
���� ��1������������Ũ�����ڼ��������·�Ӧ�����Ȼ��̡�ˮ��������Ũ�����ӷ��������Ʊ��������к����Ȼ��⡢ˮ�����������������Ȼ���ˮ���ԡ�Ũ�������ˮ��ѡ����ʵij��Ӽ���
��2���������̲�����ˮ���Ȼ���������ˮ�����Կ�ѡ����˷���������ߣ����ݹ���ʵ���õ����������
���Ȼ�����Һ�з�������Ȼ��صIJ���Ϊ�����ᾧ���ݴ˽��
��� �⣺��1��Ũ�����лӷ��ԣ�Ũ���ᡢˮ�ڼ���ʱ��������壬���������к����Ȼ��⡢ˮ�������Ȼ��⼫������ˮ���ұ���ʳ��ˮ�к��������ӣ������������ܽ⣬���Ա���ʳ��ˮ�������������Ȼ������壻Ũ��������ˮ�ԣ������������dz�ˮ������
�ʴ�Ϊ������ʳ��ˮ��Ũ���
��2���������̲�����ˮ���Ȼ���������ˮ�����Կ�ѡ����˷���������ߣ������õ��IJ��������У�©�������������ձ�����ȱ�ٵ�����Ϊ��©����
���Ȼ�����Һ�з�������Ȼ��صIJ���Ϊ�����ᾧ��
�ʴ�Ϊ��©���������ᾧ��
���� ���⿼����������ʵ�����Ʊ����������ʷ����ᴿ�ķ�������ȷ�Ʊ�ԭ�����ˡ������ᾧԭ���ǽ���ؼ�����Ŀ�ѶȲ���

��ϰ��ϵ�д�
 ��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
��Ǭ����������ҵ���ּ����ӱ����������ϵ�д�
�����Ŀ
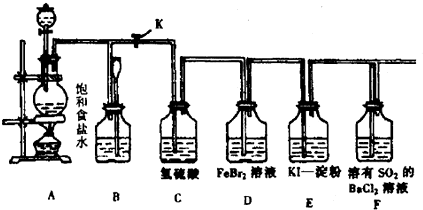
17����ͼ��ʵ�����Ʊ�����������һϵ�����ʵ���װ�ã��г��豸��A�м���װ����ʡ�ԣ���

��1���Ʊ�����ѡ�õ�ҩƷΪ���������̺�Ũ���ᣬ��ط�Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;����\;}}{\;}$MnCl2+Cl2��+2H2O��
��2��װ��B�б���ʳ��ˮ�������dz�ȥCl2�е�HCl��ͬʱװ��B���ǰ�ȫƿ�����ʵ�����ʱC���Ƿ�����������д����������ʱB�е�����B�г���©����Һ���������γ�ˮ����
��3��װ��F�ձ���ʢ�ŵ��Լ���NaOH��Һ�����з�����Ӧ�����ӷ���ʽ��2OH-+Cl2=Cl-+ClO-+H2O��
��4��װ��C��ʵ��Ŀ������֤�����Ƿ����Ư���ԣ�Ϊ��C�Т����η���D��
��5�����װ��D��E��Ŀ���DZȽ�Cl2��Br2��I2��������ǿ��������D�л���ͨ����������ʱ�����Կ�����ɫ��Һ��Ϊ����ɫ��˵��Cl2�������Դ���Br2����������װ��D��������Һ����װ��E�У����۲쵽��������E����Һ��Ϊ���㣬�²㣨CCl4�㣩Ϊ�Ϻ�ɫ���������ܣ���ܡ����ܡ���˵��Br2��������ǿ��I2��ԭ���ǹ�����Cl2Ҳ�ɽ�I-����ΪI2��

��1���Ʊ�����ѡ�õ�ҩƷΪ���������̺�Ũ���ᣬ��ط�Ӧ�Ļ�ѧ����ʽΪ��MnO2+4HCl��Ũ��$\frac{\underline{\;����\;}}{\;}$MnCl2+Cl2��+2H2O��
��2��װ��B�б���ʳ��ˮ�������dz�ȥCl2�е�HCl��ͬʱװ��B���ǰ�ȫƿ�����ʵ�����ʱC���Ƿ�����������д����������ʱB�е�����B�г���©����Һ���������γ�ˮ����
��3��װ��F�ձ���ʢ�ŵ��Լ���NaOH��Һ�����з�����Ӧ�����ӷ���ʽ��2OH-+Cl2=Cl-+ClO-+H2O��
��4��װ��C��ʵ��Ŀ������֤�����Ƿ����Ư���ԣ�Ϊ��C�Т����η���D��
| ѡ�� | �� | �� | �� |
| A | �������ɫ���� | ��ʯ�� | ʪ�����ɫ���� |
| B | �������ɫ���� | �轺 | ʪ�����ɫ���� |
| C | ʪ�����ɫ���� | Ũ���� | �������ɫ���� |
| D | ʪ�����ɫ���� | ��ˮ�Ȼ��� | �������ɫ���� |
14����������ۺ����ü������ڽ�Լ��Դ���������ڱ���������ʵ�������÷����ɵ�ص�ͭñ��Zn��Cu�ܺ���ԼΪ99%������ͭ���Ʊ�ZnO�IJ���ʵ�������ͼ��
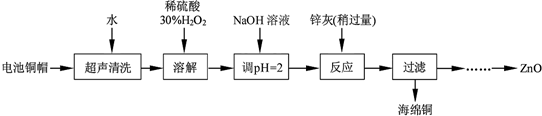
��1��Ϊȷ������п�ң���Ҫ�ɷ�ΪZn��ZnO������Ϊ�����������������ʵ������ⶨ��ȥH2O2����Һ��Cu2+�ĺ�����ʵ�����Ϊ��ȷ��ȡһ������ĺ���Cu2+����Һ�ڴ�����ƿ�У�������ˮϡ�ͣ�����pH=3��4���������KI����Na2S2O3����Һ�ζ����յ㣮���������е����ӷ���ʽ���£�2Cu2++4I-�T2CuI����ɫ����+I2��I2+2S2O32-�T2I-+S4O62-
��Na2S2O3����ҺӦװ�ڼ�ʽ������ʽ���ʽ���ζ����ڣ�
�ڵζ�ѡ�õ�ָʾ��Ϊ������Һ���ζ��յ�۲쵽������Ϊ�μ����һ�Σ���ɫ����ɫ�����ɫ���Ұ�����ڲ��䣮
�����ζ�ǰ��Һ��H2O2û�г��������ⶨ��Cu2+�ĺ�������ƫ�ߣ��ƫ�ߡ���ƫ�͡������䡱����
��2����֪pH��11ʱZn��OH��2������NaOH��Һ����[Zn��OH��4]2-���±��г��˼����������������������pH��Χ����ʼ������pH����������Ũ��Ϊ1.0mol•L-1���㣩��
ʵ���п�ѡ�õ��Լ���30% H2O2��1.0mol•L-1HNO3��1.0mol•L-1 NaOH��
�ɳ�ȥͭ����Һ�Ʊ�ZnO��ʵ�鲽������Ϊ��
�ټ�H2O2������Fe2+��
�ڼ�����������Һ������PH��4���ң�
�۹��ˣ�
�ܼ�����������Һ������PH��8.9-11֮�䣻
�ݹ��ˡ�ϴ�ӡ�����
��900�����գ�

��1��Ϊȷ������п�ң���Ҫ�ɷ�ΪZn��ZnO������Ϊ�����������������ʵ������ⶨ��ȥH2O2����Һ��Cu2+�ĺ�����ʵ�����Ϊ��ȷ��ȡһ������ĺ���Cu2+����Һ�ڴ�����ƿ�У�������ˮϡ�ͣ�����pH=3��4���������KI����Na2S2O3����Һ�ζ����յ㣮���������е����ӷ���ʽ���£�2Cu2++4I-�T2CuI����ɫ����+I2��I2+2S2O32-�T2I-+S4O62-
��Na2S2O3����ҺӦװ�ڼ�ʽ������ʽ���ʽ���ζ����ڣ�
�ڵζ�ѡ�õ�ָʾ��Ϊ������Һ���ζ��յ�۲쵽������Ϊ�μ����һ�Σ���ɫ����ɫ�����ɫ���Ұ�����ڲ��䣮
�����ζ�ǰ��Һ��H2O2û�г��������ⶨ��Cu2+�ĺ�������ƫ�ߣ��ƫ�ߡ���ƫ�͡������䡱����
��2����֪pH��11ʱZn��OH��2������NaOH��Һ����[Zn��OH��4]2-���±��г��˼����������������������pH��Χ����ʼ������pH����������Ũ��Ϊ1.0mol•L-1���㣩��
ʵ���п�ѡ�õ��Լ���30% H2O2��1.0mol•L-1HNO3��1.0mol•L-1 NaOH��
| ��ʼ������pH | ��ȫ������pH | |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Zn2+ | 5.9 | 8.9 |
�ټ�H2O2������Fe2+��
�ڼ�����������Һ������PH��4���ң�
�۹��ˣ�
�ܼ�����������Һ������PH��8.9-11֮�䣻
�ݹ��ˡ�ϴ�ӡ�����
��900�����գ�
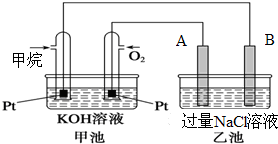 ��ͼ��ʾ�Ǽ���ȼ�ϵ�ع���ʱ��װ�ã��ҳ��е������缫һ����ʯī�缫��һ����ͭ�缫������ʱA��B�����缫�������������٣���ش��������⣺
��ͼ��ʾ�Ǽ���ȼ�ϵ�ع���ʱ��װ�ã��ҳ��е������缫һ����ʯī�缫��һ����ͭ�缫������ʱA��B�����缫�������������٣���ش��������⣺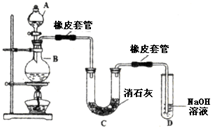 ��仯ѧ���������о����̿���Ҫ�ɷ���MnO2���Ĺ����У�������Ũ�����ϼ��ȣ�������һ�ֻ���ɫ���̼�����ζ������--������ijѧ��ʹ����һԭ�������ͼ��ʾ��ʵ��װ�ã����������Ƶõ������볱ʪ����ʯ�ҷ�Ӧ��ȡ����Ư�ۣ�����һ�����ȷ�Ӧ�����ݴ˻ش��������⣺
��仯ѧ���������о����̿���Ҫ�ɷ���MnO2���Ĺ����У�������Ũ�����ϼ��ȣ�������һ�ֻ���ɫ���̼�����ζ������--������ijѧ��ʹ����һԭ�������ͼ��ʾ��ʵ��װ�ã����������Ƶõ������볱ʪ����ʯ�ҷ�Ӧ��ȡ����Ư�ۣ�����һ�����ȷ�Ӧ�����ݴ˻ش��������⣺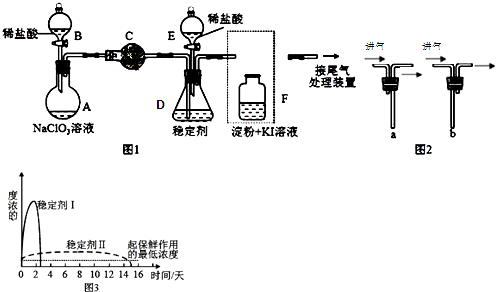
 ����������ԭ��Ӧ��2Ag+��aq��+Cu��s��=Cu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ��
����������ԭ��Ӧ��2Ag+��aq��+Cu��s��=Cu2+��aq��+2Ag��s����Ƶ�ԭ�����ͼ��ʾ��