题目内容
15.X、Y为两种主族元素,其原子的最外层电子数分别为1和6,则X、Y两种元素形成的化合物( )| A. | 一定是离子化合物 | |
| B. | 一定是共价化合物 | |
| C. | 一定形成X2Y型化合物 | |
| D. | 可能含有离子键、极性键、非极性键中的一种或两种 |
分析 X、Y为两种主族元素,其原子的最外层电子数分别为1和6,分别为ⅠA、ⅥA族元素,X可为H、Li、Na等,Y为O、S等,则X、Y两种元素的化合价分别为+1和-2价,以此解答该题.
解答 解:X、Y为两种主族元素,其原子的最外层电子数分别为1和6,则X、Y两种元素的化合价分别为+1和-2价,可形成X2Y型化合物,也可形成X2Y2型化合物,如过氧化氢,可以是离子化合氧化钠或者过氧化钠,如为水,含有极性键,如为过氧化钠,含有离子键和非极性键,
故选D.
点评 本题考查原子结构与性质关系,为高频考点,侧重考查学生的分析能力,注意把握原子的核外电子排布以及元素周期率知识,把握常见物质的结构和性质,难度不大.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
16.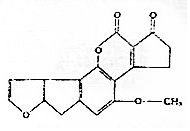 黄曲霉素AFTB1,其结构简式如图所示.它是污染粮食的真菌霉素,人类的P53特殊基因在黄曲霉素的作用下会发生突变,有引发肝癌的可能性.下列说法正确的是( )
黄曲霉素AFTB1,其结构简式如图所示.它是污染粮食的真菌霉素,人类的P53特殊基因在黄曲霉素的作用下会发生突变,有引发肝癌的可能性.下列说法正确的是( )
 黄曲霉素AFTB1,其结构简式如图所示.它是污染粮食的真菌霉素,人类的P53特殊基因在黄曲霉素的作用下会发生突变,有引发肝癌的可能性.下列说法正确的是( )
黄曲霉素AFTB1,其结构简式如图所示.它是污染粮食的真菌霉素,人类的P53特殊基因在黄曲霉素的作用下会发生突变,有引发肝癌的可能性.下列说法正确的是( )| A. | 黄曲霉素分子中所有的原子均共面 | |
| B. | 黄曲霉素分子中含有2个手性碳原子 | |
| C. | 黄曲霉素可以发生取代,加成,氧化反应 | |
| D. | 1mol黄曲霉素最多能与7molH2发生加成反应 |
6.下列反应中硝酸既表现出了强氧化性又表现了酸性的是( )
| A. | 氧化铁与硝酸反应 | B. | 氢氧化铜与硝酸反应 | ||
| C. | 木炭粉与浓硝酸反应 | D. | 铜与硝酸反应 |
3.与100mL0.1mol/LNa2SO4溶液中Na+离子浓度相同的是( )
| A. | 10mL1mol/LNa2SO4溶液 | B. | 50mL0.2mol/LNaCl溶液 | ||
| C. | 10mL0.2mol/LNa2SO4溶溶液 | D. | 200mL0.1mol/LNaNO3溶液 |
10.下列有关物质性质的比较顺序中,不正确的是( )
| A. | 热稳定性:HF<HCl<HBr<HI | B. | 微粒半径:K+>Na+>Mg2+>Al3+ | ||
| C. | 酸性:HClO4>H2SO4>H3PO4>H2SiO3 | D. | 最外层电子数Li<Mg<Si<Ar |
20.卢瑟福提出原子的行星模型的实验依据是( )
| A. | α粒子散射实验 | B. | 铀盐晶体实验 | C. | X-射线管实验 | D. | 14C放射性实验 |
7.在3Cl2+6KOH→KClO3+5KCl+3H2O的反应中,被氧化的氯元素与被还原的氯元素的质量之比为( )
| A. | 2:1 | B. | 5:1 | C. | 1:1 | D. | 1:5 |
5.下列气体均能用浓H2SO4干燥,并在常温下能共存的是( )
| A. | HCl和H2S | B. | SO2和CO2 | C. | H2和F2 | D. | NH3和HCl |