题目内容
14.随着人类对原子结构的不断认识,科学家和他们提出的原子结构模型对应的是( )| A. | 道尔顿-葡萄干面包模型 | B. | 卢瑟福-行星模型 | ||
| C. | 汤姆逊-电子轨道模型 | D. | 居里夫人-量子力学模型 |
分析 A.英国科学家道尔顿提出了原子论;
B.卢瑟福提出原子结构行星模型;
C.汤姆孙提出的葡萄干面包原子模型;
D.玻尔原子模型:电子的轨道是量子化,原子的能量是量子化.
解答 解:A.1808年,英国科学家道尔顿提出了原子论,故A错误;
B.1911年卢瑟福提出原子结构行星模型,故B正确;
C.1904年汤姆孙提出的葡萄干面包原子模型,故C错误;
D.玻尔原子模型:电子的轨道是量子化,原子的能量是量子化,所以他提出能量量子化,故D错误;
故选B.
点评 本题主要考查了化学史,难度不大,平时注意知识的积累.

练习册系列答案
 激活思维智能训练课时导学练系列答案
激活思维智能训练课时导学练系列答案
相关题目
5.向容积恒为5L的密闭容器中加入5mol SO2、2.5mol O2和0.5mol SO3,在500℃的温度和催化剂作用下发生反应:2SO2+O2$?_{△}^{催化剂}$2SO3经过amin后SO3的物质的量稳定于4.5mol而不变.下列叙述错误的是( )
| A. | SO3的物质的量为4.5mol的状态为平衡状态 | |
| B. | O2的平均反应速率为0.4amol•(L•min)-1 | |
| C. | SO2和O2的反应百分率相等 | |
| D. | 达到化学平衡状态时容器内压强减小 |
2.某化学小组用如图所示装置制取氯气,下列说法不正确的是( )
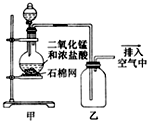

| A. | 该装置图中至少存在两处明显错误 | |
| B. | 烧瓶中的MnO2可换成KMnO4 | |
| C. | 在乙后连一盛有饱和食盐水的烧杯可进行尾气处理 | |
| D. | 在集气瓶的导管口处放一片湿润的淀粉碘化钾试纸可以证明是否有氯气逸出 |
9.元素X的单质及X与Y形成的化合物能按如图所示的关系发生转化.则X为( )


| A. | 当n=1时,X可能是C | B. | 当n=1时,X可能是Al | ||
| C. | 当n=2时,X可能是S | D. | 当n=2时,X可能是Na |
19.一定温度下,测定某溶液中只含NH4+、Cl-、H+、OH-四种离子,下列说法一定正确的是( )
| A. | 溶液中四种粒子之间满足:c(Cl-)>c(H+)>c(NH4+)>c(OH-) | |
| B. | 若溶液中粒子间满足:c(NH4+)>c(Cl-)>c(OH-)>c(H+),则溶液中溶质为:NH3•H2O和NH4Cl | |
| C. | 若溶液中粒子间满足:c(Cl-)>c(NH4+)>c(H+)>c(OH-),则溶液中溶质只有NH4Cl | |
| D. | 若溶液中c(NH4+)=c(Cl-),则该溶液pH等于7. |
6.常温下,下列各组离子在指定溶液中能大量共存的是( )
| A. | c(SO32-)=0.5 mol•L-1的溶液中:ClO-、Na+、Cl-、CO32- | |
| B. | pH=1的溶液中:NH4+、Na+、SO42-、Fe3+ | |
| C. | 强碱性溶液中:Na+、AlO2-、NO3-、HCO3- | |
| D. | 水电离产生的c(H+)=1×10-14mol•L-1的溶液中:HCO3-、NH4+、Cl-、Ca2+ |
3.以下物质分离提纯(括号里为杂质)所用试剂正确的是( )
| A. | 乙酸乙酯(乙酸):水 | |
| B. | 溴苯(溴):NaOH溶液 | |
| C. | 苯(苯酚):浓溴水 | |
| D. | 苯(甲苯):酸性高锰酸钾溶液、NaOH溶液 |
4.X、Y、Z是3种短周期元素,其中X、Z位于同一主族.X原子的最外层电子数是其电子层数的3倍.X原子的核外电子数比Y原子少1.下列说法正确的是( )
| A. | 原子半径由大到小的顺序为Z>X>Y | |
| B. | Z元素的氢化物是一种强酸 | |
| C. | 元素非金属性由强到弱的顺序为X>Y>Z | |
| D. | 3种元素的气态氢化物中,Y的气态氢化物还原性最强 |