题目内容
10.实验室配制少量银氨溶液的方法是:用文字表达2%硝酸银溶液逐滴加入2%的稀氨水,至生成的沉淀恰好溶解可得到银氨溶液,发生的离子反应方程式为Ag++NH3•H2O═AgOH↓+NH4+、AgOH+2NH3•H2O═Ag(NH3)2++OH-+2H2O,向银氨溶液中滴加少量的乙醛,水浴加热片刻即可在试管内壁形成银镜,离子方程式为:CH3CHO+2Ag(NH3)2++2OH-$→_{△}^{水浴}$CH3COO-+NH4++2Ag↓+3NH3+H2O.分析 硝酸银溶液中加氨水,至生成的沉淀恰好溶解可得到银氨溶液,银氨溶液中滴加少量的乙醛,发生银镜反应生成Ag、氨气、水和乙酸铵,以此来解答.
解答 解:实验室配制少量银氨溶液的方法是:用文字表达为2%硝酸银溶液逐滴加入2%的稀氨水,至生成的沉淀恰好溶解可得到银氨溶液,发生的离子反应方程式为Ag++NH3•H2O═AgOH↓+NH4+、AgOH+2 NH3•H2O═Ag(NH3)2++OH-+2H2O,向银氨溶液中滴加少量的乙醛,水浴加热片刻即可在试管内壁形成银镜,离子方程式为CH3CHO+2 Ag(NH3)2++2 OH-$→_{△}^{水浴}$ CH3COO-+NH4++2Ag↓+3NH3+H2O,
故答案为:2%硝酸银溶液逐滴加入2%的稀氨水,至生成的沉淀恰好溶解可得到银氨溶液;Ag++NH3•H2O═AgOH↓+NH4+、AgOH+2 NH3•H2O═Ag(NH3)2++OH-+2H2O;CH3CHO+2 Ag(NH3)2++2 OH-$→_{△}^{水浴}$ CH3COO-+NH4++2Ag↓+3NH3+H2O.
点评 本题考查离子反应方程式的书写及有机物的结构与性质,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
20.下列A、B、C、D、E、F为几种常见仪器的部分结构(有的仪器被放大)
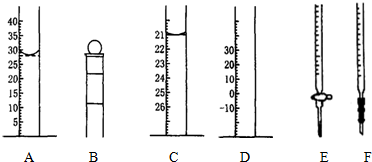
(1)A图中液面所示溶液的体积为28.0mL
(2)仪器E的名称是酸式滴定管
(3)Na2S2O3(硫代硫酸钠),俗称大苏打.把Na2S2O3•5H2O固体溶于水,得到无色溶液,该溶液显碱性,用离子反应方程式解释溶液显碱性的原因:S2O32?+5H2O?HS2O3?+0H?.化工生产中常常依据反应2S2O32-+I2=S4O62-+2I-,用I2的标准溶液测定大苏打产品的纯度.步骤如下:
①称取5.5g Na2S2O3•5H2O产品,用仪器B(从上述A、B、C、D、E、F中选填)配制成100.00mL溶液.
②用仪器F(从上述A、B、C、D、E、F中选填)量取10.00mL溶液于锥形瓶中,以淀粉溶液为指示剂.
③用浓度为0.0500mol/L的I2标准溶液进行滴定,判断达到滴定终点的现象是锥形瓶中的溶液由无色溶液变成蓝色,且半分钟不褪色.
④重复滴定3次,数据记录于表.计算所配制的Na2S2O3溶液的物质的量浓度为(保留4位小数)0.2000mol/L
⑤滴定时若用Na2S2O3溶液润洗锥形瓶,则测得大苏打产品的浓度偏高(填偏高、偏低、不变).

(1)A图中液面所示溶液的体积为28.0mL
(2)仪器E的名称是酸式滴定管
(3)Na2S2O3(硫代硫酸钠),俗称大苏打.把Na2S2O3•5H2O固体溶于水,得到无色溶液,该溶液显碱性,用离子反应方程式解释溶液显碱性的原因:S2O32?+5H2O?HS2O3?+0H?.化工生产中常常依据反应2S2O32-+I2=S4O62-+2I-,用I2的标准溶液测定大苏打产品的纯度.步骤如下:
①称取5.5g Na2S2O3•5H2O产品,用仪器B(从上述A、B、C、D、E、F中选填)配制成100.00mL溶液.
②用仪器F(从上述A、B、C、D、E、F中选填)量取10.00mL溶液于锥形瓶中,以淀粉溶液为指示剂.
③用浓度为0.0500mol/L的I2标准溶液进行滴定,判断达到滴定终点的现象是锥形瓶中的溶液由无色溶液变成蓝色,且半分钟不褪色.
④重复滴定3次,数据记录于表.计算所配制的Na2S2O3溶液的物质的量浓度为(保留4位小数)0.2000mol/L
| 编号 | 1 | 2 | 3 | 4 |
| Na2S2O3溶液的体积/mL | 10.00 | 10.00 | 10.00 | 10.00 |
| 消耗I2标准溶液的体积/mL | 19.99 | 19.98 | 20.01 | 20.02 |
1.下列说法中,错误的是( )
| A. | 蔗糖、淀粉、纤维素水解的最终产物都是葡萄糖 | |
| B. | 误服重金属盐,立即服用牛奶或豆浆可解毒 | |
| C. | 油脂、乙酸乙酯都属于酯类,但不是同系物 | |
| D. | 室温下,在水中的溶解度:甘油>苯酚>1-氯丁烷 |
5.已知X、Y、Z、W是原子序数依次增大的短周期主族元素,X最外层电子数是次外层电子数的2倍,Y和W同主族,且W的原子序数是Y的2倍,Z的焰色反应为黄色.下列说法不正确的是( )
| A. | 原子半径大小顺序:r(Z)>r(W)>r(Y) | |
| B. | Y的简单气态氢化物的热稳定性比W的强 | |
| C. | Z和Y形成的原子个数比为1:1和2:1的化合物中化学键类型相同 | |
| D. | X的最高价氧化物对应水化物的酸性比W的弱 |
15.研究发现,NO在人体的血管系统内具有传送信号的功能,因而有“信使分子”的誉称.下列有关NO的说法正确的是( )
| A. | NO不属于大气污染物 | B. | NO能溶于水 | ||
| C. | NO易与空气中的氧气化合 | D. | NO可用排空气法收集 |
19.下列关于硅酸的叙述,错误的是( )
| A. | 硅酸是一种很弱的酸 | |
| B. | 硅酸可由二氧化硅与水反应制得 | |
| C. | 硅酸不稳定,加热脱水会生成二氧化硅 | |
| D. | 硅酸可以由可溶性硅酸盐与盐酸反应制得 |
20.下列关系不正确的是( )
| A. | 离子半径:Cl->F->Na+>Al3+ | B. | 非金属性:Cl>S>P>Si | ||
| C. | 酸性:H2SiO3>H2CO3>H3PO4 | D. | 热稳定性:PH3<H2S<HCl<HF |
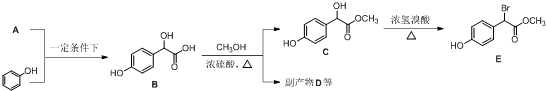
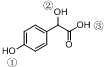 中①、②、③3个-OH的酸性由强到弱的顺为③>①>②;写出B与过量Na2CO3溶液反应的化学方程式
中①、②、③3个-OH的酸性由强到弱的顺为③>①>②;写出B与过量Na2CO3溶液反应的化学方程式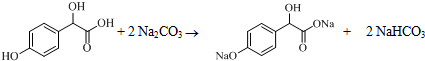 .
.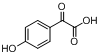 $→_{△}^{浓H_{2}SO_{4}}$
$→_{△}^{浓H_{2}SO_{4}}$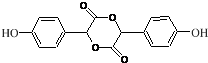 +2H2O.
+2H2O.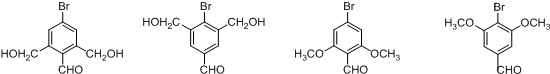 (不考虑立体异构).
(不考虑立体异构).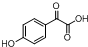 的合成路线图.
的合成路线图.