题目内容
13.下列电离方程式中,正确的是( )| A. | HCl=H+1+Cl-1 | B. | (NH4)2SO4=(NH4)2-+SO42- | ||
| C. | FeCl2=Fe3++Cl- | D. | K2S=2 K++S2- |
分析 A.氯化氢完全电离生成离子的电荷标注错误;
B.硫酸铵电离生成2个铵根离子,铵根离子带正电荷;
C.氯化亚铁电离生成亚铁离子和两个氯离子;
D.硫化钾完全电离生成两个钾离子和硫离子;
解答 解:A.氯化氢完全电离生成离子,电离方程式为:HCl=H++Cl-,故A错误;
B.硫酸铵电离生成2个铵根离子,电离方程式为:(NH4)2SO4=2NH4++SO42-,故B错误;
C.氯化亚铁电离生成亚铁离子和两个氯离子,电离方程式为:FeCl2=Fe2++2Cl-,故C错误;
D.硫化钾完全电离生成两个钾离子和硫离子,电离方程式为K2S=2 K++S2-,故D正确;
故选D.
点评 本题考查了电离方程式的书写,掌握电离方程式的书写方法并能灵活运用是正确解答此类题的关键,题目难度不大.

练习册系列答案
 开心蛙状元测试卷系列答案
开心蛙状元测试卷系列答案
相关题目
3.根据有机化合物的命名原则,下列命名正确的是( )
| A. | 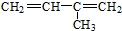 3-甲基-1,3-丁二烯 3-甲基-1,3-丁二烯 | B. | 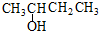 2-羟基丁烷 2-羟基丁烷 | ||
| C. | CH3CH(C2H5)CH2CH2CH3 2-乙基戊烷 | D. | CH3CH(NH2)CH2COOH 3-氨基丁酸 |
4.NA表示阿伏加德罗常数的值,下列说法正确的是( )
| A. | 5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA | |
| B. | 1 mol Na2O2与足量H2O充分反应,转移的电子数为2NA | |
| C. | 7.8gNa2O2中含有的阴离子数等于0.1NA | |
| D. | 标况下,2.24LH2O所含分子数为0.1NA |
1.根据反应:
①I2+SO2+2H2O═H2SO4+2HI
②2FeCl3+2HI═2FeCl2+I2+2HCl
③2FeCl2+Cl2═2FeCl3
可知:I-、Fe2+、Cl-、SO2的还原性由强到弱的顺序是( )
①I2+SO2+2H2O═H2SO4+2HI
②2FeCl3+2HI═2FeCl2+I2+2HCl
③2FeCl2+Cl2═2FeCl3
可知:I-、Fe2+、Cl-、SO2的还原性由强到弱的顺序是( )
| A. | SO2>I->Fe2+>Cl- | B. | Cl->Fe2+>SO2>I- | C. | Fe2+>I->Cl->SO2 | D. | I->Fe2+>Cl->SO2 |
8.现有一瓶物质甲和乙的混合物,已知甲和乙的某些性质如表所示.据此,将甲和乙分离的最佳方法是( )
| 物质 | 熔点(℃) | 沸点(℃) | 密度 (g•cm-3) | 二者溶解性关系 |
| 甲 | -98 | 57.5 | 1.93 | 互不相溶 |
| 乙 | -84 | 77 | 0.90 |
| A. | 蒸馏 | B. | 蒸发 | C. | 过滤 | D. | 分液 |
5.在相同的温度和压强下,二氧化碳和笑气(化学式为N2O)的体积相同,则下列它们一定相同的是( )
①分子数;②原子数; ③密度;④质量;⑤物质的量.
①分子数;②原子数; ③密度;④质量;⑤物质的量.
| A. | 只有①⑤ | B. | 只有①②④⑤ | C. | 只有②③④⑤ | D. | ③②④⑤① |
2.在实验室中,下列做法不正确的是( )
| A. | 在演示实验和分组实验中,要力求利用最少的实验用品,获得最佳的实验效果,最大限度的减少废弃物 | |
| B. | 稀释浓硫酸时,应沿烧杯壁向浓硫酸中缓缓加水,并用玻璃棒不断搅拌 | |
| C. | 取用液体药品时,要把瓶塞反放在桌面上,标签朝向手心,放回原处时标签向外 | |
| D. | 不能用手接触实验室里的药品,不要凑到容器口闻气体的气味 |
 ,
, .
.