题目内容
(10分) “低碳循环”引起各国的高度重视,已知煤、甲烷等可以与水蒸气反应生成以CO和H2为主的合成气,合成气有广泛应用。试回答下列问题:
(1)高炉炼铁是CO气体的重要用途之一,其基本反应为:FeO(s)+CO(g) Fe(s)+CO2(g) ΔH>0。已知在1 100 ℃时,该反应的化学平衡常数K=0.263。
Fe(s)+CO2(g) ΔH>0。已知在1 100 ℃时,该反应的化学平衡常数K=0.263。
①温度升高,化学平衡移动后达到新的平衡,此时平衡常数K值 (填“增大”、“减小”或“不变”);
②1 100 ℃时测得高炉中,c(CO2)=0.025 mol·L-1,c(CO)=0.1 mol·L-1,则在这种情况下,该反应向 进行(填“左”或“右”),判断依据是 。
(2)目前工业上也可用CO2来生产燃料甲醇,有关反应为:
CO2(g)+3H2(g)  CH3OH(g)+H2O(g) ΔH=-49.0KJ/mol,现向体积为1L的密闭容器中充入1mol CO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
CH3OH(g)+H2O(g) ΔH=-49.0KJ/mol,现向体积为1L的密闭容器中充入1mol CO2和3molH2,反应过程中测得CO2和CH3OH(g)的浓度随时间的变化如图所示。
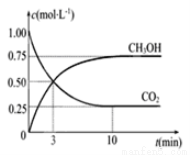
①从反应开始到平衡,氢气的平均反应速率V(H2)=------------。
②反应达到平衡后,下列措施能使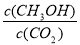 增大的是-------(填符号)
增大的是-------(填符号)
A.升高温度 B.再充入H2 C.再充入CO2 D.将H2O(g)从体系中分离 E.充入He(g)
(1)①增大,②右,因为c(CO2)/c(CO)=0.25<0.263 (2)① 0.225mol/(L·min) ②B D
【解析】
试题分析:①由于该反应的正反应是吸热反应,所以温度升高,化学平衡正向移动,达到新的平衡时平衡常数K值增大;②1 100 ℃时测得高炉中,c(CO2)=0.025 mol·L-1,c(CO)=0.1 mol·L-1,则Q= c(CO2)÷c(CO)=0.025 mol·L-1÷0.1 mol·L-1=0.25<0.263=K,所以在这种情况下,该反应向正反应方向移动;(2) ①根据图像可知:从反应开始到平衡,V(CO2)=0.75mol/L÷10min=0.075mol/(L·min),V(H2)=3V(CO2)= 0.225mol/(L·min);②反应达到平衡后,下列措施能使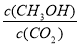 增大, A.升高温度,平衡逆向移动,错误; B.再充入H2使平衡正向移动,正确;C.再充入CO2 平衡正向移动,但是Δc(CO2) 大于Δc(CH3OH), 比值减小,错误;D.将H2O(g)从体系中分离,平衡正向移动,比值增大,正确;E.充入He(g),平衡不移动,比值不改变,错误。
增大, A.升高温度,平衡逆向移动,错误; B.再充入H2使平衡正向移动,正确;C.再充入CO2 平衡正向移动,但是Δc(CO2) 大于Δc(CH3OH), 比值减小,错误;D.将H2O(g)从体系中分离,平衡正向移动,比值增大,正确;E.充入He(g),平衡不移动,比值不改变,错误。
考点:考查化学速率的计算、化学反应进行的方向及判断依据、影响平衡移动的因素的知识。

 2OH- +Cl2↑ +H2↑
2OH- +Cl2↑ +H2↑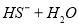
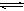
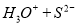
 2Z(g)
2Z(g) PCl 3(g)+Cl2(g) ① 2HI(g)
PCl 3(g)+Cl2(g) ① 2HI(g)