题目内容
20.实验室盛装NaOH溶液的试剂瓶不能用玻璃塞,以防止发生反应:(离子方程式)SiO2+2OH-=SiO32-+H2O.分析 二氧化硅是酸性氧化物,能和强碱溶液反应,二氧化硅能和氢氧化钠反应生成硅酸钠和水,玻璃中含有二氧化硅,二氧化硅和氢氧化钠溶液生成可溶性的硅酸钠具有粘性,据此分析解答.
解答 解:实验室盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,其原因是在常温下,氢氧化钠与玻璃中的二氧化硅缓慢地发生反应,生成具有粘性的Na2SiO3,反应为SiO2+2NaOH=Na2SiO3+H2O,离子反应为:SiO2+2OH-=SiO32-+2H2O,
故答案为:SiO2+2OH-=SiO32-+2H2O.
点评 本题以化学试剂的存放为载体考查了二氧化硅的性质,注意二氧化硅是酸性氧化物,和强酸不反应,但能和氢氟酸反应,题目难度不大.

练习册系列答案
相关题目
20.元素X、Y、Z、W、Q、M在元素周期表的相对位置如表所示,其中Z元素是目前发现的非金属性最强的元素,下列说法正确的是( )
| X | Y | Z | |
| W | Q | M |
| A. | 对应氢化物的沸点Y>Q是因为Y的非金属性比Q强 | |
| B. | XM4的比例模型为  其二氢取代物有两种 其二氢取代物有两种 | |
| C. | W的氧化物,常温下可以和Z、M的氢化物反应 | |
| D. | Z的单质能将Y的单质从其氢化物中置换出来 |
1.下列有关说法正确的是( )
| A. | HClO是弱酸,所以NaClO是弱电解质 | |
| B. | Cl2具有很强的氧化性,在化学反应中只能作氧化剂 | |
| C. | 1.12 L Cl2含有1.7NA个质子(NA 表示阿伏加德罗常数) | |
| D. | 过量的铁粉与氯气反应生成FeCl3 |
8.使相同物质的量浓度的NaCl、MgCl2、AlCl3溶液中的Cl-离子完全沉淀时,若所用相同浓度的AgNO3溶液的体积比为2:2:1,则上述三种溶液的体积比是( )
| A. | 9:3:1 | B. | 3:2:1 | C. | 6:3:1 | D. | 9:4:1 |
15.某K2CO3样品中含有Na2CO3、KNO3和Ba(NO3)2三种杂质的一种或两种,现将13.8g样品加入足量水,样品全部溶解,再加入过量的CaCl2溶液得到9克沉淀,对样品所含杂质的正确判断是( )
| A. | 肯定有KNO3,一定没有Na2CO3 | B. | 肯定没有Ba(NO3)2和KNO3 | ||
| C. | 肯定没有Ba(NO3)2,可能有Na2CO3 | D. | 肯定没有Ba(NO3)2,肯定有Na2CO3 |
12.下列有关实验的说法正确的是( )
| A. | 将SO2通入溴水中,溴水褪色证明SO2具有漂白性 | |
| B. | 将含有少量HCl的Cl2通入水中以除去HCl杂质 | |
| C. | 将乙烯通入酸性KMnO4溶液中,溶液褪色证明乙烯具有还原性 | |
| D. | 将蔗糖溶液和少量稀H2SO4混合加热后,加入新制的Cu(OH)2检验蔗糖是否水解 |
9.下列诗句描述的过程包含化学变化的是( )
| A. | 千锤万凿出深山 | B. | 雪融山顶响流泉 | C. | 吹尽狂沙始到金 | D. | 蜡炬成灰泪始干 |
10.下列各组物质,不能按右图(“→”表示反应一步完成)关系转化的是( )
| 选项 | a | b | c | 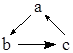 |
| A | Al | Al2O3 | Al (OH)3 | |
| B | SiO2 | Na2SiO3 | H2SiO3 | |
| C | AlCl3 | Na[Al(OH)4] | Al(OH)3 | |
| D | CaO | Ca(OH)2 | CaCO3 |
| A. | A | B. | B | C. | C | D. | D |
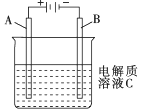 (1)肼(N2H4)又称联氨,是一种可燃性液体,可用作燃料.肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,反应生成一种可以参与大气循环的气体.该电池放电时,负极的电极反应式是:N2H4+4OH--4e-=4H2O+N2↑.
(1)肼(N2H4)又称联氨,是一种可燃性液体,可用作燃料.肼-空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液,反应生成一种可以参与大气循环的气体.该电池放电时,负极的电极反应式是:N2H4+4OH--4e-=4H2O+N2↑.