题目内容
13.短周期元素A、B、C的原子序数之和为37,A、B在同一周期,A+、C-具有相同的核外电子层结构.下列推测不正确的是( )| A. | 同周期元素中C的氢化物稳定性最强 | |
| B. | 同周期元素中A的金属性最强 | |
| C. | 原子半径:A>B,离子半径:A+>C- | |
| D. | A、B、C的简单离子中,会破坏水的电离平衡的是C |
分析 A+与C-具有相同的核外电子层结构,可推知C在A、B的上一个周期,又因为A、B、C原子序数之和为37,A、B在同一周期,若A、B处于长周期,则A、B元素的质子数之和大于37,故A、B、C处于短周期,则A为Na、C为F、可知B的质子数=37-11-9=17,则B为Cl,结合元素周期律的递变规律解答该题.
解答 解:A+与C-具有相同的核外电子层结构,可推知C在A、B的上一个周期,又因为A、B、C原子序数之和为37,A、B在同一周期,若A、B处于长周期,则A、B元素的质子数之和大于37,故A、B、C处于短周期,则A为Na、C为F、可知B的质子数=37-11-9=17,则B为Cl,
A.同主族自上而下非金属性减弱,非金属性越强,氢化物越稳定,故同主族中HF最稳定,故A正确;
B.A为Na,由同周期元素从左到右元素的金属性逐渐减弱,可知同周期元素中Na的金属性最强,故B正确;
C.同周期随原子序数递增原子半径减小,故原子半径Na>Cl,电子层结构相同,核电核数越大离子半径越小,则离子半径应为:F->Na+,故C错误;
D.A、B、C的简单离子中F-形成的酸为弱酸,能够水解,会破坏水的电离平衡,故D正确,
故选:C.
点评 本题考查元素的推断和元素周期律,为高频考点,题目难度中等,注意把握元素的推断的角度以及元素周期律的递变规律.

练习册系列答案
相关题目
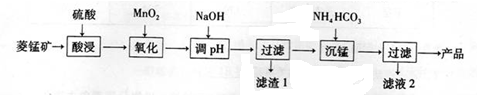
5.辉铜矿是一种重要的铜矿石,主要含有硫化亚铜(Cu2S),还有Fe2O3、SiO2及一些不溶性杂质.一种以辉铜矿石为原料制备硝酸铜晶体的工艺流程如图:
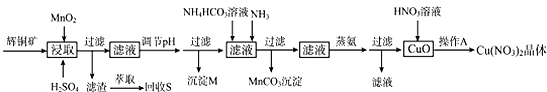
已知:部分金属阳离子生成氢氧化物沉淀的pH范围如表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
回答下列问题
(1)浸取后得到的浸出液中含有CuSO4、MnSO4.写出浸取时产生CuSO4、MnSO4反应的化学方程式2MnO2+Cu2S+4H2SO4=S↓+2CuSO4+2MnSO4+4H2O.
(2)调节pH的目的是铁离子转化成氢氧化铁完全沉淀,pH的调节范围为3.2≤pH<4.4.
(3)生成MnCO3沉淀的离子方程式为Mn2++NH3+HCO3-=MnCO3↓+NH4+.
(4)操作A为蒸发浓缩、冷却结晶.
(5)由辉铜矿制取铜的反应过程可以表示为:
2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ/mol
2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ/mol
则由Cu2S与O2加热反应生成Cu的热化学方程式为Cu2S(s)+02(g)═2Cu(s)+SO2(g)△H=-217.4kJ.mol-l.
(6)若用含85% Cu2S(Mr=160)的辉铜矿来制备无水Cu(NO3)2,假设浸取率为95%,调节pH时损Cu 3%,蒸氨过程中有5%未转化为CuO,其它过程中无损耗,则1.6kg这样的辉铜矿最多能制备14.9mol无水Cu(NO3)2.(计算结果精确到小数点后1位)

已知:部分金属阳离子生成氢氧化物沉淀的pH范围如表所示(开始沉淀的pH按金属离子浓度为1.0mol/L计算)
| 离子 | 开始沉淀的pH | 完全沉淀的pH |
| Fe3+ | 1.1 | 3.2 |
| Mn2+ | 8.3 | 9.8 |
| Cu2+ | 4.4 | 6.4 |
(1)浸取后得到的浸出液中含有CuSO4、MnSO4.写出浸取时产生CuSO4、MnSO4反应的化学方程式2MnO2+Cu2S+4H2SO4=S↓+2CuSO4+2MnSO4+4H2O.
(2)调节pH的目的是铁离子转化成氢氧化铁完全沉淀,pH的调节范围为3.2≤pH<4.4.
(3)生成MnCO3沉淀的离子方程式为Mn2++NH3+HCO3-=MnCO3↓+NH4+.
(4)操作A为蒸发浓缩、冷却结晶.
(5)由辉铜矿制取铜的反应过程可以表示为:
2Cu2S(s)+3O2(g)═2Cu2O(s)+2SO2(g)△H=-768.2kJ/mol
2Cu2O(s)+Cu2S(s)═6Cu(s)+SO2(g)△H=+116.0kJ/mol
则由Cu2S与O2加热反应生成Cu的热化学方程式为Cu2S(s)+02(g)═2Cu(s)+SO2(g)△H=-217.4kJ.mol-l.
(6)若用含85% Cu2S(Mr=160)的辉铜矿来制备无水Cu(NO3)2,假设浸取率为95%,调节pH时损Cu 3%,蒸氨过程中有5%未转化为CuO,其它过程中无损耗,则1.6kg这样的辉铜矿最多能制备14.9mol无水Cu(NO3)2.(计算结果精确到小数点后1位)
2.在一个恒定容积的密闭容器中,发生化学反应2M(g)?N(g)+P(g),若N、P的起始浓度为0,反应物M的浓度随反应时间的变化情况如下表:
根据上述数据,完成下列填空:
(1)在实验I中,50min时,N的浓度为0.25mol•L-1,0~50min内,以P的浓度改变表示的反应速率为0.005mol/(L.min).
(2)在实验Ⅱ中,若10~20min内,v(N)=0.10mol•L-1,则c2=0.7mol•L-1.
(3)对比两个实验,推测实验Ⅱ中M的初始浓度c1=1.0mol•L-1,反应经20minM的浓度不再变化,可推测实验Ⅱ中还隐含的条件是实验Ⅱ使用催化剂.
(4)上述实验中,反应达到限度后,M的转化率是50%.
| 实验序号 | 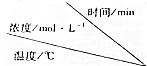 | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| Ⅰ | 800 | 1.0 | 0.80 | 0.67 | 0.57 | 0.50 | 0.50 | 0.50 |
| Ⅱ | 800 | c1 | c2 | 0.50 | 0.50 | 0.50 | 0.50 | 0.50 |
(1)在实验I中,50min时,N的浓度为0.25mol•L-1,0~50min内,以P的浓度改变表示的反应速率为0.005mol/(L.min).
(2)在实验Ⅱ中,若10~20min内,v(N)=0.10mol•L-1,则c2=0.7mol•L-1.
(3)对比两个实验,推测实验Ⅱ中M的初始浓度c1=1.0mol•L-1,反应经20minM的浓度不再变化,可推测实验Ⅱ中还隐含的条件是实验Ⅱ使用催化剂.
(4)上述实验中,反应达到限度后,M的转化率是50%.
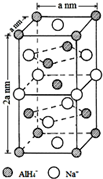 氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示.
氢化铝钠(NaAlH4)是一种新型轻质储氢材料,掺入少量Ti的NaAlH4在150℃时释氢,在170℃、15.2MPa条件下又重复吸氢.NaAlH4可由AlCl3和NaH在适当条件下合成.NaAlH4的晶胞结构如图所示. .
.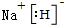 .
. (标明配位键).
(标明配位键).