题目内容
13. 氮族元素的单质及其化合物在农药、化肥等方面有重要应用.我们可以利用物质结构与性质的相关知识去认识和利用它们,
氮族元素的单质及其化合物在农药、化肥等方面有重要应用.我们可以利用物质结构与性质的相关知识去认识和利用它们,(1)基态磷原子的电子排布式为1s22s22p63s23p3;等物质的量的NH3和N2混合气体中σ键与π键的数目之比为2:1.
(2)N、P、As原子的第一电离能由大到小的顺序为N>P>As.
(3)光化学烟雾易在PM2.5尘粒的催化作用下形成,光化学烟雾中含有NOx、
O3、CH2=CHCHO、HCOOH等二次污染物.下列说法正确的是ABD.
A.N2O与CO2互为等电子体,其结构式为N=N=O
B.O3的沸点大于O2
C.N2O结构式可表示为N=N=O,中心氮原子的杂化轨道类型为sp2、sp3
D.HCOOH在水中溶解度大的原因与氢键有关
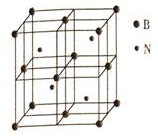
(4)六方氮化硼在高温高压下可转化为立方氮化硼,其晶胞结构如图所示,晶胞边长为dcm,该晶胞中含有4个氮原子、4个硼原子.
(5)N与砷(As)是同族元素,B与鎵(Ga)是同族元素,立方砷化镓晶体与立方氮化硼晶体结构类似,两种晶体中熔点较高的是氮化硼;立方砷化镓晶体的晶胞边长为apm(1pm=10-12m),则其密度为$\frac{5.8×1{0}^{32}}{{a}^{3}{N}_{A}}$g•cm-3 (用含a的式子表示,设NA为阿伏加德罗常数的值).
分析 (1)基态N原子价电子排布式为2s22p3,根据洪特规则、泡利原理画出价电子轨道排布图;NH3分子含有3个σ键,N2分子结构式为N≡N,三键含有1个σ键、2个π键;
(2)元素的非金属性越强,其得电子能力越强,失电子能力越弱,则第一电离能越大;
(3)A.原子总数相等、价电子总数相等的微粒互为等电子体,等电子体结构相似;
B.均形成分子晶体,相对分子质量越大,分子间作用力越强,沸点越高;
C.CH2=CHCHO分子中碳原子均形成3个σ键,没有孤对电子,杂化轨道数目为3;
D.HCOOH在水中与水分子之间形成氢键;
(4)晶胞中N原子数目为4,B原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4;
(5)立方砷化镓晶体与立方氮化硼晶体结构类似,均属于原子晶体,原子半径越小,共价键越强,晶体熔点越高;根据均摊法计算晶胞中As、Ga原子数目,表示出晶胞质量,根据ρ=$\frac{m}{V}$计算晶胞密度.
解答 解:(1)磷属于15好元素,根据构造原理基态磷原子的电子排布式为1s22s22p63s23p3,1molNH3含有3molσ键,1molN2含有1molσ键和2molπ键,混合气体中σ键与π键的数目之比为2:1,故答案为:1s22s22p63s23p3;
(2)同一主族元素中,元素的金属性随着原子序数的增大而增强,失电子能力增强,也就是越容易失电子,电离能越小,则第一电离能随着原子序数的增大而减小,所以这几种元素第一电离能大小顺序是N>P>As,故答案为:N>P>As;
(3)A.N2O与CO2分子均含有3个原子、价电子数均为16,二者互为等电子体,N2O的结构式为N=N=O,故A正确;
B.O3、O2均形成分子晶体,O3的相对分子质量越大,分子间作用力更强,故O3的沸点大于O2,故B正确;
C.CH2=CHCHO分子中碳原子均形成3个σ键,没有孤对电子,杂化轨道数目为3,碳原子采取sp2杂化,故C错误;
D.HCOOH在水中与水分子之间形成氢键,故HCOOH在水中溶解度大,故D正确,
故答案为:ABD;
(4)晶胞中N原子数目为4,B原子数目为8×$\frac{1}{8}$+6×$\frac{1}{2}$=4,故答案为:4;4;
(5)立方砷化镓晶体与立方氮化硼晶体结构类似,均属于原子晶体,原子半径N<As、B<Ga,故氮化硼中共价键更强,氮化硼的晶体熔点更高,晶胞中As、Ga原子数目均为4,晶胞质量为4×$\frac{145}{{N}_{A}}$g,晶胞密度为4×$\frac{145}{{N}_{A}}$g÷(a×10-10 cm)3=$\frac{5.8×1{0}^{32}}{{a}^{3}{N}_{A}}$g.cm-3,
故答案为:氮化硼;$\frac{5.8×1{0}^{32}}{{a}^{3}{N}_{A}}$.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、化学键、杂化方式、晶体类型与性质、晶胞计算等,注意对基础知识的理解掌握.

Y原子最外层电子数为次外层的3倍,X原子最外层电子数为Y原子最外层电子数的一半.下列说法正确的是
( )
| A. | 原子序数:W>X>Y>Z | B. | 原子半径:W>X>Y>Z | ||
| C. | 最高价氧化物对应的碱的碱性:W<X | D. | 最简单氧化物的稳定性:Y>Z |
| A. | 用氯化铁溶液腐蚀铜板:Cu+Fe3+═Cu2++Fe2+ | |
| B. | 碘水中通入适量的SO2:I2+SO2+2H2O═2I-+SO42-+4H+ | |
| C. | 硝酸银溶液中滴加过量氨水:Ag++NH3•H2O═AgOH↓+NH4+ | |
| D. | 0.5mol/LNaHSO4与0.5mol/LBa(OH)2混合至溶液呈中性:Ba2++OH-+SO42-+H+═BaSO4↓+H2O |
| A. | 50℃时,测定某NaNO2溶液的pH=8,则溶液中c(Na+)-c(NO2-)=9.9×10-7mol•L-1 | |||||||||
| B. | NaHSO3水溶液中存在关系:c(H2SO3)+c(H+)=c(OH-)+c(SO32-)+c(HSO3-) | |||||||||
| C. | 一定温度下,利用pH计测定不同浓度醋酸溶液的pH值,得到如下数据:
| |||||||||
| D. | 已知25℃时,有关弱电解质的电离平衡常数:HCN:Ka=4.9×10-10;H2CO3:Ka1=4.3×10-7Ka2=5.6×10-11.则CO2通入NaCN溶液中反应的化学方程式为:2NaCN+H2O+CO2=2HCN+Na2CO3 |

 ;D元素在元素周期表中的位置为第四周期第Ⅷ族
;D元素在元素周期表中的位置为第四周期第Ⅷ族