题目内容
下列叙述正确的是( )
| A、白铁(镀锌)的表面一量破损,铁腐蚀加快 |
| B、原电池中电子向负极流动 |
| C、马口铁(镀锡)的表面一旦破损,铁腐蚀加快 |
| D、用铝质铆钉接铁板,铁易被腐蚀 |
考点:金属的电化学腐蚀与防护,原电池和电解池的工作原理
专题:电化学专题
分析:A、白铁(镀锌)的表面一量破损,构成原电池,锌做负极;
B、原电池中负极失电子;
C、马口铁(镀锡)的表面一旦破损,构成原电池,铁做负极;
D、用铝质铆钉接铁板,构成原电池,铝做负极.
B、原电池中负极失电子;
C、马口铁(镀锡)的表面一旦破损,构成原电池,铁做负极;
D、用铝质铆钉接铁板,构成原电池,铝做负极.
解答:
解:A、白铁(镀锌)的表面一量破损,构成原电池,锌做负极,铁做正极,铁被保护,腐蚀减慢,故A错误;
B、原电池中负极失电子,故电子从负极流出,故B错误;
C、马口铁(镀锡)的表面一旦破损,构成原电池,铁做负极,铁的腐蚀加快,故C正确;
D、用铝质铆钉接铁板,构成原电池,铝做负极,铁被保护,铁的腐蚀减慢,故D错误.
故选C.
B、原电池中负极失电子,故电子从负极流出,故B错误;
C、马口铁(镀锡)的表面一旦破损,构成原电池,铁做负极,铁的腐蚀加快,故C正确;
D、用铝质铆钉接铁板,构成原电池,铝做负极,铁被保护,铁的腐蚀减慢,故D错误.
故选C.
点评:本题考查原电池的工作原理,应明白原电池的负极易被腐蚀,正极被保护,难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
在25℃时,某稀溶液中由水电离产生的c(OH-)水=10-11mol/L.下列有关该溶液的叙述正确的是( )
| A、该溶液一定呈酸性 |
| B、该溶液中的c(H+)肯定等于10-3mol/L |
| C、该溶液的pH可能为3,可能为11 |
| D、该溶液一定呈碱性 |
下列实验操作或记录的数据合理的是( )
| A、在中和反应反应热的测定实验中,用温度计轻轻搅拌混合液充分反应后再读数 |
| B、酸碱中和滴定前滴定管和锥形瓶先用滴定液润洗:2~3次 |
| C、配制硫酸亚铁溶液时,将FeSO4固体溶解在稀硫酸中并加人少量铁,再加水进行有关操作 |
| D、某学生用广泛pH试纸测得某稀盐酸的pH为2.3 |
某有机物结构简式如图,下列有关它的说法正确的是( )
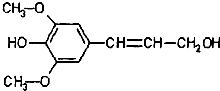

| A、分子式是C11H14O4,属于芳香烃 |
| B、分子中所有碳原子不可能在同一平面 |
| C、不能与Na反应放出H2 |
| D、能发生的反应类型有氧化、取代、加成 |
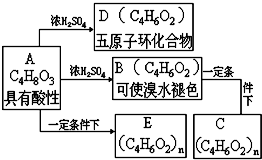 化合物C和E都是医用功能高分子材料,且组成中元素质量分数相同,均可由化合物A(C4H8O3)制得,如图所示.B和D互为同分异构体.
化合物C和E都是医用功能高分子材料,且组成中元素质量分数相同,均可由化合物A(C4H8O3)制得,如图所示.B和D互为同分异构体.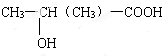 .
.