题目内容
17.X、Y和Z是三种元素,其常见化合价均为+2价 X2++Z=X+Z2+;Y+Z2+=Y2++Z.这三种离子的氧化性强弱顺序为:X2+>Z2+>Y2+.分析 依据氧化还原反应中氧化剂的氧化性大于氧化产物,还原剂的还原性大于还原产物分析判断.
解答 解:反应X2++Z=X+Z2+中氧化剂X2+的氧化性大于氧化产物Z2+,即氧化性X2+>Z2+;反应Y+Z2+=Y2++Z中氧化剂Z2+的氧化性大于氧化产物Y2+,即氧化性Z2+>Y2+表现的氧化性大小为:X2+>Z2+>Y2+,故答案为:X2+>Z2+>Y2+.
点评 本题考查了氧化还原反应的强弱规律的应用,正确理解和判断氧化剂、氧化产物是解本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
7.X、Y都是短周期元素,X原子最外层只有一个电子,Y元素的最高正价与最低负价的代数和为6,X和Y两元素形成的化合物为R,则下列关于R的叙述正确的是( )
| A. | R一定是共价化合物 | |
| B. | R一定是离子化合物 | |
| C. | R可能是共价化合物,也可能是离子化合物 | |
| D. | R常温下一定是固态物质 |
8.不能用分液漏斗分离的是( )
| A. | 汽油和水 | B. | 苯和盐酸 | C. | 酒精和水 | D. | 水和四氯化碳 |
12.对实验Ⅰ~Ⅳ的叙述正确的是( )
| A. | 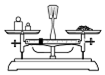 如图实验:用托盘天平称量一定质量的氯化钠固体 | |
| B. | 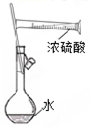 如图实验:配制一定物质的量浓度的硫酸 | |
| C. | 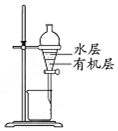 如图实验:用苯萃取溴水中的溴后进行分液 | |
| D. | 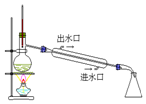 如图实验:用于蒸馏,分离四氯化碳和溴 |
2.按溶液、浊液、胶体的顺序排列正确的是( )
| A. | 食盐水、牛奶、豆浆 | B. | 碘酒、泥水、血液 | ||
| C. | 白糖水、食盐水、茶叶水 | D. | Ca(OH)2悬浊液、澄清石灰水、石灰浆 |
9.如表所示,对陈述Ⅰ、Ⅱ的正确性及两者间是否具有因果关系的判断都正确的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ | 判断 |
| A | NaHCO3可用于治疗胃病 | NaHCO3可与盐酸反应 | Ⅰ对,Ⅱ对,无 |
| B | 向滴有酚酞的水溶液中加入Na2O2变红色 | Na2O2与水反应生成氢氧化钠 | Ⅰ对,Ⅱ错,无 |
| C | 金属钠具有强还原性 | 高压钠灯发出透雾性强的黄光 | Ⅰ对,Ⅱ对,有 |
| D | Na2O2可为航天员供氧 | Na2O2能与CO2和H2O反应生成O2 | Ⅰ对,Ⅱ对,有 |
| A. | A | B. | B | C. | C | D. | D |
6.化学反应 A2(g)+B2(g)?2AB(g)的能量变化如图所示,下列叙述中正确的是( )
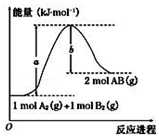

| A. | 每生成 2 个分子 AB 吸收(a-b) kJ 热量 | |
| B. | 该反应热△H=+(a-b)kJ•mol-1 | |
| C. | 逆反应的活化能高于正反应的活化能 | |
| D. | 断裂1mol A-A 和 1mol B-B 键,放出 a kJ 能量 |
4.误服重金属盐可以立即采取的最合适的急救措施是( )
| A. | 大量喝水 | B. | 服用维生素C | C. | 喝适量牛奶 | D. | 喝食用醋 |