题目内容
 小苏打长期放置在空气中会变质(部分转变为Na2CO3),某研究小组测定某小苏打样品中NaHCO3的质量分数,设计如下实验方案:
小苏打长期放置在空气中会变质(部分转变为Na2CO3),某研究小组测定某小苏打样品中NaHCO3的质量分数,设计如下实验方案:Ⅰ.热分解法
利用图1装置,充分加热小苏打样品.
(1)仪器a的名称为
(2)在实验过程中,需要测量的实验数据有:
①仪器a的质量; ②
Ⅱ.测量气体的体积法
利用图2装置,测定反应生成气体的体积.
(1)组装好仪器后,首先进行的操作为
(2)导管g的作用为
(3)为了减少实验误差,B、C中最好利用
(4)待反应结束,气体冷却至室温后,利用图2所示装置读取气体体积时,应注意的事项有:①
(5)若所取样品的质量为mg,反应前测定滴管C的读数为V1mL,反应结束后滴管C的读数为V2mL,则测定样品中NaHCO3和Na2CO3的物质的量之和为
Ⅲ.其他方案讨论
测定该小苏打样品中的NaHCO3的质量分数,还可采用的方案有
A.x g样品与足量稀盐酸充分反应,加热,蒸干、灼烧.得到固体y g
B.x g样品与足量稀硫酸充分反应,逸出气体用碱石灰吸收,碱石灰增重y g
C.x g样品与足量Ba(OH)2溶液充分反应、过滤、洗涤、烘干,得到固体y g.
考点:探究物质的组成或测量物质的含量,化学方程式的有关计算,探究碳酸钠与碳酸氢钠的性质
专题:实验设计题
分析:Ⅰ(1)该仪器名称是坩埚;
(2)采用热分解法测定碳酸氢钠质量分数时要测定坩埚质量、加热前坩埚和样品质量、加热后坩埚和残留物的质量;
Ⅱ(1)连接后仪器后在实验前要检查装置气密性;
(2)g的作用有平衡气压、减少误差的作用;
(3)二氧化碳能溶于水,但难溶于饱和碳酸氢钠溶液,从而减少误差;
(4)读数时,B、C两管液面相平、视线与液面最低处相平;
(5)CO2气体体积=(V1-V2)mL,则n(CO2)=
,根据C原子守恒计算NaHCO3和Na2CO3的物质的量之和;
Ⅲ(6)A.最终得到固体成分是NaCl,根据Na原子守恒计算碳酸氢钠;
B.碱石灰能吸收水蒸气和二氧化碳气体;
C.最终得到固体为碳酸钡,根据C原子守恒计算碳酸氢钠.
(2)采用热分解法测定碳酸氢钠质量分数时要测定坩埚质量、加热前坩埚和样品质量、加热后坩埚和残留物的质量;
Ⅱ(1)连接后仪器后在实验前要检查装置气密性;
(2)g的作用有平衡气压、减少误差的作用;
(3)二氧化碳能溶于水,但难溶于饱和碳酸氢钠溶液,从而减少误差;
(4)读数时,B、C两管液面相平、视线与液面最低处相平;
(5)CO2气体体积=(V1-V2)mL,则n(CO2)=
| (V1-V2)×10-3L |
| 22.4L/mol |
Ⅲ(6)A.最终得到固体成分是NaCl,根据Na原子守恒计算碳酸氢钠;
B.碱石灰能吸收水蒸气和二氧化碳气体;
C.最终得到固体为碳酸钡,根据C原子守恒计算碳酸氢钠.
解答:
解:Ⅰ(1)该仪器名称是坩埚,故答案为:坩埚;
(2)采用热分解法测定碳酸氢钠质量分数时要测定坩埚质量、加热前坩埚和样品质量、加热后坩埚和残留物的质量,利用质量差进行计算,所以②加热前,仪器a和样品的总质量;③加热冷却后,仪器a和残留物的总质量,
故答案为:②加热前,仪器a和样品的总质量;③加热冷却后,仪器a和残留物的总质量;
Ⅱ(1)连接后仪器后在实验前要检查装置气密性,否则可能导致实验失败,故答案为:检查装置的气密性;
(2)①平衡分液漏斗与锥形瓶内的气压,使液体顺利流下,否则稀硫酸不易流下;②滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的体积误差,而使测量更准确,
故答案为:①平衡分液漏斗与锥形瓶内的气压,使液体顺利流下;②滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的体积误差;
(3)二氧化碳能溶于水,但难溶于饱和碳酸氢钠溶液,从而减少误差,所以可以用饱和碳酸氢钠代替水,故答案为:饱和NaHCO3;
(4)读数时,B、C两管液面相平、视线与液面最低处相平,否则易产生误差,导致计算结果有误差,故答案为:读数时应上下移动C管,使B、C两管液面相平;视线与液面最低处相平;
(5)CO2气体体积=(V1-V2)mL,则n(CO2)=
,根据C原子守恒得n(NaHCO3)+n(Na2CO3)=n(CO2)=
=
mol,故答案为:
mol;
Ⅲ(6)A.最终得到固体成分是NaCl,根据Na原子守恒计算碳酸氢钠质量,从而计算碳酸氢钠质量分数,故正确;
B.碱石灰能吸收水蒸气和二氧化碳气体,所以碱金属增加的质量不仅仅是二氧化碳,所以无法计算碳酸氢钠质量,导致无法计算碳酸氢钠质量分数,故错误;
C.最终得到固体为碳酸钡,根据C原子守恒计算碳酸氢钠质量,从而计算碳酸氢钠质量分数,故正确;
故选AC.
(2)采用热分解法测定碳酸氢钠质量分数时要测定坩埚质量、加热前坩埚和样品质量、加热后坩埚和残留物的质量,利用质量差进行计算,所以②加热前,仪器a和样品的总质量;③加热冷却后,仪器a和残留物的总质量,
故答案为:②加热前,仪器a和样品的总质量;③加热冷却后,仪器a和残留物的总质量;
Ⅱ(1)连接后仪器后在实验前要检查装置气密性,否则可能导致实验失败,故答案为:检查装置的气密性;
(2)①平衡分液漏斗与锥形瓶内的气压,使液体顺利流下,否则稀硫酸不易流下;②滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的体积误差,而使测量更准确,
故答案为:①平衡分液漏斗与锥形瓶内的气压,使液体顺利流下;②滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的体积误差;
(3)二氧化碳能溶于水,但难溶于饱和碳酸氢钠溶液,从而减少误差,所以可以用饱和碳酸氢钠代替水,故答案为:饱和NaHCO3;
(4)读数时,B、C两管液面相平、视线与液面最低处相平,否则易产生误差,导致计算结果有误差,故答案为:读数时应上下移动C管,使B、C两管液面相平;视线与液面最低处相平;
(5)CO2气体体积=(V1-V2)mL,则n(CO2)=
| (V1-V2)×10-3L |
| 22.4L/mol |
| (V1-V2)×10-3L |
| 22.4L/mol |
| V1-V2 |
| 22400 |
| V1-V2 |
| 22400 |
Ⅲ(6)A.最终得到固体成分是NaCl,根据Na原子守恒计算碳酸氢钠质量,从而计算碳酸氢钠质量分数,故正确;
B.碱石灰能吸收水蒸气和二氧化碳气体,所以碱金属增加的质量不仅仅是二氧化碳,所以无法计算碳酸氢钠质量,导致无法计算碳酸氢钠质量分数,故错误;
C.最终得到固体为碳酸钡,根据C原子守恒计算碳酸氢钠质量,从而计算碳酸氢钠质量分数,故正确;
故选AC.
点评:本题采用多种方法测定碳酸氢钠质量分数,同时考查学生基本实验操作、实验分析、计算能力、对比能力等,明确实验原理是解本题关键,注意滴定管刻度遵循“上小下大”原则,难点是分析导管g的作用,题目难度中等.

练习册系列答案
相关题目
二甲醚(CH3OCH3)可由一氧化碳和物质X在一定的条件下制得.反应的化学方程式为2CO+4X
CH3OCH3+H2O,则X的化学式为( )
| ||
| A、C2H5OH |
| B、H2O2 |
| C、C2H4 |
| D、H2 |
对于氯化铁溶液和氢氧化铁胶体,以下说法正确的是( )
| A、分散质粒子直径都在1nm~100nm之间 |
| B、分散质微粒都能透过半透膜 |
| C、加热蒸干并灼烧后都有氧化铁生成 |
| D、分散系中分散质微粒前者带电荷、后者不带电荷 |
鉴别K2CO3和KHCO3两种白色固体,有4位同学为鉴别它们,分别设计了下列四种不同的方法,其中可行的是( )
| A、分别加入1 mol?L-1的盐酸溶液,看有无气泡产生 |
| B、分别取样在试管中加热,将可能产生的气体通入澄清石灰水,观察有无白色浑浊 |
| C、分别取样配成溶液,滴加Ca(OH)2溶液,观察有无白色沉淀 |
| D、分别配成溶液,用洁净铂丝蘸取溶液在酒精灯火焰上灼烧,观察火焰的颜色(可使用蓝色钴玻璃) |
化合物X的分子式为C5H11Cl,用NaOH醇溶液处理X,可得到具有分子式为C5H10的两种产物Y、Z.Y、Z经催化加氢都可得到2-甲基丁烷.则X的结构简式为( )
| A、CH3CH2CH2CH2Cl |
| B、(CH3)2CHCH2CH2Cl |
| C、(CH3)2CClCH2CH3 |
| D、(CH3)3CCH2Cl |
有a L乙炔和乙烯的混合气体,在催化剂存在下与足量的H2发生加成反应,消耗H2 1.25a L,乙烯和乙炔的体积比为( )
| A、1:1 | B、2:1 |
| C、3:1 | D、4:1 |
因发生电极反应,直接破坏了该电极附近水的电离平衡的是( )
| A、电解氯化铜溶液时的阴极 |
| B、铜铁原电池的负极(硫酸溶液为电解质) |
| C、电解食盐水时的阴极 |
| D、铁片上镀锌时的阴极 |
电解无水氯化镁所得的镁蒸气冷却后即为固体镁.下列气体中,镁蒸气可以在其氛围中冷却的是( )
| A、H2 |
| B、CO2 |
| C、空气 |
| D、O2 |
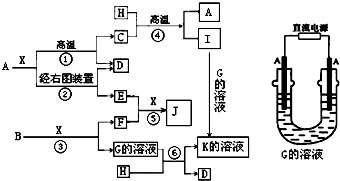 如图表示各物质之间的转化关系,已知A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液.请按要求填空:
如图表示各物质之间的转化关系,已知A、D、F、H均为单质,X常温下为无色液体,B为淡黄色固体,J溶于酸得到黄色溶液.请按要求填空: