题目内容
在含有FeCl3、FeCl2、AlCl3、NaCl的混合溶液中,加入足量的Na2O2固体,搅拌充分反应后,再加入过量盐酸,溶液中离子数目无变化的是( )
| A、Na+ |
| B、Al3+ |
| C、Fe2+ |
| D、Fe3+ |
考点:离子方程式的有关计算
专题:
分析:过氧化钠和水反应生成氢氧化钠和氧气,过氧化钠具有强氧化性,亚铁离子具有还原性,易被氧化为三价铁,铵盐易和强碱反应.
解答:
解:因为加入的过氧化钠具有强氧化性,所以二价铁会被氧化为三价铁,两者变化均较大,过氧化钠和水反应生成氢氧化钠和氧气,钠离子增加,反应生成NaOH与NH4+结合微热会产生挥发性的氨气,所以铵根减少,铝离子加过量过氧化钠时生成偏铝酸钠,再加过量盐酸又反应生成铝离子,即Al3+数目无变化.
故选B.
故选B.
点评:本题考查物质性质的有关知识,可以根据所学知识进行回答,难度不大,注意亚铁离子被氧化为三价铁离子是解题的易错点.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
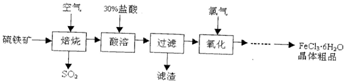
用铝土矿(主要成分为Al2O3,含Fe2O3杂质)为原料冶炼铝的工艺流程如下:下列叙述正确的是( )


| A、试剂X可以是盐酸 |
| B、反应①过滤后所得沉淀为氢氧化铁 |
| C、图中所示转化反应都不是氧化还原反应 |
| D、操作②中发生的化学方程式为NaAlO2+2H2O+CO2=Al(OH)3↓+NaHCO3 |
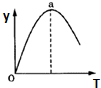 工业制氢气的一个重要反应是:CO(g)+H2O(g)?CO2(g)+H2(g)
工业制氢气的一个重要反应是:CO(g)+H2O(g)?CO2(g)+H2(g)