题目内容
材料是人类赖以生存和发展的重要物质基础.
(1)生产硅酸盐水泥和普通玻璃都需要用到的主要原料是 (填名称).
(2)石英玻璃化学稳定性强、膨胀系数小,是一种特种玻璃,石英玻璃的主要成分是
(填化学式);有机玻璃(聚甲基丙烯酸甲酯)实际上不是硅酸盐材料,而是一种 .(选填“橡胶”或“纤维”或“塑料”).
(3)玻璃钢具有耐腐蚀、质量轻、强度高的性能,它属于 材料(填“合金”或“复合”).
(4)上海世博会期间将用可降解的“玉米塑料”替代一次性饭盒、并可被用来制作世博会证件及胸卡,目的是为了防止产生 污染.
(1)生产硅酸盐水泥和普通玻璃都需要用到的主要原料是
(2)石英玻璃化学稳定性强、膨胀系数小,是一种特种玻璃,石英玻璃的主要成分是
(3)玻璃钢具有耐腐蚀、质量轻、强度高的性能,它属于
(4)上海世博会期间将用可降解的“玉米塑料”替代一次性饭盒、并可被用来制作世博会证件及胸卡,目的是为了防止产生
考点:硅酸盐工业,常见的生活环境的污染及治理,硅和二氧化硅,水泥的主要化学成分、生产原料及其用途,玻璃的主要化学成分、生产原料及其用途
专题:
分析:(1)根据制备水泥和玻璃的原料分析;
(2)石英玻璃的主要成分是SiO2;聚甲基丙烯酸甲酯属于塑料;
(3)复合材料是由两种或两种以上不同性质的材料,通过物理或化学的方法,在宏观上组成具有新性能的材料;
(4)聚乙烯等材料塑料难以降解,形成白色污染,用可降解材料代替塑料壳减少白色污染.
(2)石英玻璃的主要成分是SiO2;聚甲基丙烯酸甲酯属于塑料;
(3)复合材料是由两种或两种以上不同性质的材料,通过物理或化学的方法,在宏观上组成具有新性能的材料;
(4)聚乙烯等材料塑料难以降解,形成白色污染,用可降解材料代替塑料壳减少白色污染.
解答:
解:(1)制备水泥的原料是粘土、石灰石;制备玻璃的原料是纯碱、石灰石、石英,所以都用到CaCO3,故答案为:石灰石;
(2)石英玻璃化学稳定性强、膨胀系数小,是一种特种玻璃,主要成分为SiO2,聚甲基丙烯酸甲酯是合成高分子化合物属于塑料,故答案为:SiO2;塑料;
(3)玻璃钢是将玻璃纤维和高分子材料复合而成的复合材料,故答案为:复合;
(4)对难降解的塑料垃圾(多指塑料袋)环境污染称为白色污染,用可降解的“玉米塑料”替代一次性饭盒、并可被用来制作世博会的证件及胸卡,可以防止产生白色污染,故答案为:白色.
(2)石英玻璃化学稳定性强、膨胀系数小,是一种特种玻璃,主要成分为SiO2,聚甲基丙烯酸甲酯是合成高分子化合物属于塑料,故答案为:SiO2;塑料;
(3)玻璃钢是将玻璃纤维和高分子材料复合而成的复合材料,故答案为:复合;
(4)对难降解的塑料垃圾(多指塑料袋)环境污染称为白色污染,用可降解的“玉米塑料”替代一次性饭盒、并可被用来制作世博会的证件及胸卡,可以防止产生白色污染,故答案为:白色.
点评:本题考查了几种常见的材料,侧重性质及其应用,为高频考点,侧重于化学与生产、化学材料与环境保护的考查,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
如图是同学们经常使用的某品牌修正液包装标签.小明仔细阅读后,结合自己的生活经验和所学知识得出了修正液的某些性质,小明的推测中合理的是.( )


| A、修正液的成分对纸张具有强腐蚀性 |
| B、修正液中不含有化学物质 |
| C、修正液是一种胶体,均一、稳定 |
| D、修正液的溶剂易挥发、易燃 |
1998年7月8日,全国科学技术名称审定委员会公布了101-109号元素的中文定名.而早在1996年2月,德国达姆施塔特重离子研究所就合成出当时最重的人造元素,它是由
Zn撞入一个
Pb的原子核,并立即释放一个中子而产生的一种新元素的原子.该元素的原子序数是( )
70 30 |
208 82 |
| A、111 | B、112 |
| C、113 | D、114 |
下在无土栽培中,需配制一定组成的植物营养液.已知某植物营养液的配方为0.3molKCl、0.2molK2SO4、0.1molZnSO4和1LH2O.若用KCl、K2SO4、ZnCl2和1LH2O为原料配得相同组成的营养液,所需三种盐的物质的量分别是( )
| A、0.1mol、0.2mol、0.1mol |
| B、0.2mol、0.3mol、0.2mol |
| C、0.1mol、0.5mol、0.2mol |
| D、0.1mol、0.3mol、0.1mol |
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)?CO2(g)+H2(g),反应过程中测定的部分数据见下表
已知表中t1>t2,下列说法不正确的是( )
| 反应时间/min | n(CO)/mol | H2O/mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | 0.20 |
A、反应在t1 min内的平均速率为v(H2)=
| ||
| B、保持其他条件不变,起始时间容器中充入0.60molCO和1.20molH2O,到达平衡时,n(CO2)=0.40mol | ||
| C、保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大 | ||
| D、温度升至800℃时,若上述反应平衡常数为0.64,则正反应为吸热反应 |
铁镍蓄电池又称爱迪生电池,其充、放电按下式进行:Fe+Ni2O3+3H2O
Fe(OH)2+2Ni(OH)2,下列有关该电池的说法不正确的是( )
| 放电 |
| 充电 |
| A、电池的电解液为碱性溶液,正极为Ni2O3、负极为Fe |
| B、电池放电时,负极反应为Fe+2OH--2e-=Fe(OH)2 |
| C、电池充电过程中,阴极附近溶液的pH降低 |
| D、电池充电时,阳极反应为2Ni(OH)2+2OH--2e-=Ni2O3+3H2O |
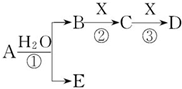 A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去):
A、B、C、D、E是短周期元素组成的中学常见的物质,它们的转化关系如图所示(部分产物和反应条件略去):