题目内容
工业制硝酸的其中一步反应为氨的氧化,反应方程式为:4NH3(g)+5O2(g)?4NO(g)+6H2O(g)△H=-1025kJ/mol氧化过程中还伴随有N2O、N2等物质生成.有关该反应的说法正确的是( )
| A、反应处于平衡状态时,c(NH3)?c(O2)=c(NO)?c(H2O) |
| B、反应达到平衡后,ν正(NH3)=ν逆(H2O) |
| C、其它条件不变,温度越高,氨的转化率越高 |
| D、寻找合适的催化剂是加快反应速率并提高NO产率的有效措施 |
考点:化学平衡建立的过程,化学平衡的影响因素
专题:化学平衡专题
分析:A、化学反应达到平衡状态时,正逆反应速率相等,各物质的浓度不变,由此衍生的一些物理量也不变.
B、反应达到平衡后,不同物质的反应速率之比等于其计量数之比为正反应速率之比.
C、升高温度,平衡向吸热方向移动.
D、催化剂能加快反应速率.
B、反应达到平衡后,不同物质的反应速率之比等于其计量数之比为正反应速率之比.
C、升高温度,平衡向吸热方向移动.
D、催化剂能加快反应速率.
解答:
解:A、反应处于平衡状态时,体系中各组分的浓度不变,与c(NH3)?c(O2)和c(NO)?c(H2O)是否相等无关,故A错误;
B、反应达到平衡后,各组分的浓度保持不变,则一定有3v正(NH3)=2v逆(H2O),故B错误;
C、该反应正反应方向是放热反应,升高温度平衡向逆反应方向移动,温度越高,氨的转化率越低,故C错误;
D、合适的催化剂能加快反应速率,所以能提高氨气的产率,故D正确.
故选D.
B、反应达到平衡后,各组分的浓度保持不变,则一定有3v正(NH3)=2v逆(H2O),故B错误;
C、该反应正反应方向是放热反应,升高温度平衡向逆反应方向移动,温度越高,氨的转化率越低,故C错误;
D、合适的催化剂能加快反应速率,所以能提高氨气的产率,故D正确.
故选D.
点评:本题考查了化学平衡状态的判断及外界条件对化学平衡的影响,难度不大,注意催化剂能改变化学反应速率但不影响化学平衡的移动.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
进行化学实验,必须注意安全,下列说法不正确的是(填写标号)( )
| A、不慎将酸溅到眼中,应立即用水冲洗,边洗边眨眼睛 |
| B、不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 |
| C、如果苯酚浓液沾到皮肤上,应立即用酒精洗 |
| D、配制硫酸溶液时,可先在量筒内加入一定体积的水,再在搅拌下慢慢加入浓硫酸 |
用水稀释0.1摩/升氨水时,溶液中随着水量的增加而减小的是( )
A、
| ||
B、
| ||
| C、[H+]和[OH-]的乘积 | ||
| D、OH-的物质的量 |
气态电中性基态原子的原子核外电子排布发生如下变化,吸收能量最多的是( )
| A、1s22s22p63s23p2→1s22s22p63s23p1 |
| B、1s22s22p2→1s22s22p1 |
| C、1s22s22p4→1s22s22p3 |
| D、1s22s22p3→1s22s22p2 |


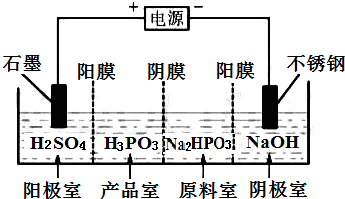 亚磷酸(H3PO3)与足量的NaOH溶液反应生成Na2HPO3.
亚磷酸(H3PO3)与足量的NaOH溶液反应生成Na2HPO3.