题目内容
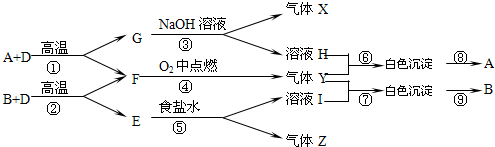
已知A、B、E是固体化合物,D、G是固体单质,X、Z、F为可燃性气体,F、X的火焰呈淡蓝色,他们之间有如下转化关系:
(1)写出A、B、Z的名称:A ,B ,Z
(2)Y的结构式为: ,A的晶体结构类型: ,溶液H的保存要求 .
(3)按要求写出反应方程式:①的化学方程式: .⑥离子方程式: .

(1)写出A、B、Z的名称:A
(2)Y的结构式为:
(3)按要求写出反应方程式:①的化学方程式:
考点:无机物的推断
专题:推断题
分析:化合物A与单质D反应得到单质G与气体F,单质G与NaOH溶液反应得到气体X,X、F为可燃性气体,X、F的火焰呈淡蓝色,则X为H2,F为CO,A为SiO2,G为碳,由转化关系可知,H为Na2SiO3,Y为CO2,反应⑥得到白色沉淀为H2SiO3,可溶性气体Z由化合物E与食盐水得到,考虑为Z为乙炔,E为碳化钙,I为Ca(OH)2,反应⑦的白色沉淀为CaCO3,B为CaO,据此解答.
解答:
解:化合物A与单质D反应得到单质G与气体F,单质G与NaOH溶液反应得到气体X,X、F为可燃性气体,X、F的火焰呈淡蓝色,则X为H2,F为CO,A为SiO2,G为碳,由转化关系可知,H为Na2SiO3,Y为CO2,反应⑥得到白色沉淀为H2SiO3,可溶性气体Z由化合物E与食盐水得到,考虑为Z为乙炔,E为碳化钙,I为Ca(OH)2,反应⑦的白色沉淀为CaCO3,B为CaO,
(1)由上述分析可知,A为二氧化硅,B为氧化钙,Z为乙炔,
故答案为:二氧化硅;氧化钙;乙炔;
(2)Y为CO2,结构式为:O=C=O,二氧化硅属于原子晶体,Na2SiO3溶液应保存在带橡胶塞的细口试剂瓶中,
故答案为:O=C=O;原子晶体;带橡胶塞的细口试剂瓶;
(3)反应①的化学方程式:SiO2+2C
Si+2CO↑,
反应⑥离子方程式:SiO32-+CO2+H2O═H2SiO3↓+CO32-,
故答案为:SiO2+2C
Si+2CO↑;SiO32-+CO2+H2O═H2SiO3↓+CO32-.
(1)由上述分析可知,A为二氧化硅,B为氧化钙,Z为乙炔,
故答案为:二氧化硅;氧化钙;乙炔;
(2)Y为CO2,结构式为:O=C=O,二氧化硅属于原子晶体,Na2SiO3溶液应保存在带橡胶塞的细口试剂瓶中,
故答案为:O=C=O;原子晶体;带橡胶塞的细口试剂瓶;
(3)反应①的化学方程式:SiO2+2C
| ||
反应⑥离子方程式:SiO32-+CO2+H2O═H2SiO3↓+CO32-,
故答案为:SiO2+2C
| ||
点评:本题考查无机物推断,难度中等,需要学生熟练掌握元素化合物知识,确定气体Z为乙炔是难点,中学涉及比较少,

练习册系列答案
相关题目
设nA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、1mol甲醇中含有4nA个C-H键 |
| B、常温常压下,18g H2O含有10nA电子 |
| C、标准状况下,22.4L盐酸中含有nA个HCl分子 |
| D、64 g铜片与足量稀HNO3反应生成nA个NO分子 |
对于平衡体系mA(g)+nB(g)?pC(g)+qD(g);△H<0.下列结论中正确的是( )
| A、若温度不变,将容器的体积增大1倍,此时A的浓度变为原来的0.48倍,则m+n>p+q | ||
| B、若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m:n | ||
| C、若m+n=p+q,则往含有a mol气体的平衡体系中再加入b mol B,达到新平衡时,气体的总物质的量等于(a+b) | ||
D、温度不变时,若压强增大至原来的2倍,达到新平衡时,总体积一定是原体积的
|
等质量的下列物质,所含分子数最多的是( )
| A、KCl |
| B、CH3COOH |
| C、SiO2 |
| D、P4 |