题目内容
16.下列实验装置图正确的是( )| A. | 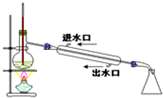 工业乙醇的蒸馏 | B. | 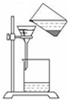 苯甲酸趁热过滤 | ||
| C. | 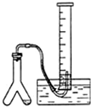 制少量乙炔并测体积 | D. | 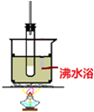 实验室制硝基苯 |
分析 A.蒸馏时温度计测定馏分的温度,冷却水的方向下进上出;
B.过滤时用玻璃棒引流;
C.乙炔不溶于水,可利用排水法测定其体积;
D.制备硝基苯,需要水浴加热.
解答 解:A.蒸馏时温度计测定馏分的温度,冷却水的方向下进上出,则图中温度计的位置、冷却水方向均不合理,故A错误;
B.过滤时用玻璃棒引流,图中缺少玻璃棒,故B错误;
C.乙炔不溶于水,可利用排水法测定其体积,则图中装置可制少量乙炔并测体积,故C正确;
D.制备硝基苯,需要水浴加热,但不是沸水浴,故D错误;
故选C.
点评 本题考查化学实验方案的评价,为高频考点,把握混合物分离提纯、有机物制备及实验操作为解答的关键,侧重分析与实验能力的考查,注意实验评价性分析,题目难度不大.

练习册系列答案
相关题目
20.下列物质属于纯净物的是( )
| A. | 乙烷 | B. | 汽油 | C. | 柴油 | D. | 天然气 |
11.化学与生活、社会密切相关.下列说法正确的是( )
| A. | 维生素C能将食物中的Fe3+转化为易吸收的Fe2+,是因为维C有氧化性 | |
| B. | SO2、NO2等在大气中达到一定浓度造成大气污染.溶液的稳定性决定了污染的长期性 | |
| C. | 燃料电池能有效提高能源的利用率是因为通过原电池装置将热能直接转化成了电能 | |
| D. | 绿色化学的核心是应用化学原理对环境污染进行有效治理 |
1.下列装置或操作能达到实验目的是( )
| A. |  量取8.5mL稀硫酸 | B. | 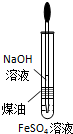 制备Fe(OH)2 | ||
| C. | 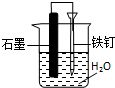 防止铁钉生锈 | D. | 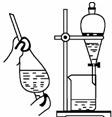 用酒精萃取水中的溴 |
5.已知Ba(OH)2•8H2O与NH4Cl(s)反应的焓变为△H1,Ba(OH)2•8H2O分解的热焓变为△H2,Ba(OH)2与NH4Cl(s)反应的热焓变△H3<0.则( )
| A. | △H1<0 | B. | △H1>△H2 | C. | △H2═△H1+△H3 | D. | △H2>|△H3| |
6.如表是A、B、C、D、E五种有机物的有关信息:
回答下列问题:
(1)A~E中,属于烃的是AB(填字母).
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br.
(3)有机物B具有的性质是②③(填序号).
①无色无味的液体; ②有毒; ③不溶于水; ④密度比水大; ⑤能使酸性KMnO4溶液和溴水褪色
(4)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是:CH3COOH+NaHCO3═CH3COONa+H2O+CO2↑(用化学方程式说明).
| A | ①能使溴的四氯化碳溶液褪色 ②比例模型如图 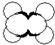 ③能与水在一定条件下反应生成C |
| B | ①由C、H两种元素组成 ②球棍模型如图 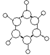 |
| C | ①由C、H、O三种元素组成 ②能与Na反应 ③与E反应生成相对分子质量为88的酯 |
| D | ①相对分子质量比C少2 ②能由C催化氧化得到 |
| E | ①由C、H、O三种元素组成 ②其水溶液能使紫色石蕊试液变红 |
(1)A~E中,属于烃的是AB(填字母).
(2)A能使溴的四氯化碳溶液褪色,发生反应的化学方程式为CH2=CH2+Br2→CH2BrCH2Br.
(3)有机物B具有的性质是②③(填序号).
①无色无味的液体; ②有毒; ③不溶于水; ④密度比水大; ⑤能使酸性KMnO4溶液和溴水褪色
(4)E的水溶液能使紫色石蕊试液变红,说明E的水溶液显酸性,现设计一个实验来比较E与碳酸酸性的强弱,则该实验的原理是:CH3COOH+NaHCO3═CH3COONa+H2O+CO2↑(用化学方程式说明).
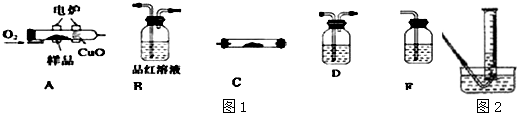
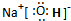 ,所含有的化学键有离子键、共价键;它属于离子化合物(填“离子”或“共价”).
,所含有的化学键有离子键、共价键;它属于离子化合物(填“离子”或“共价”).