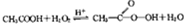题目内容
6.氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室制备少量Mg(ClO3)2•6H2O的流程如图1: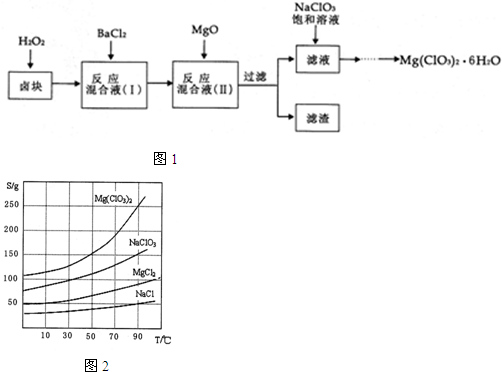
已知:①卤块主要成分为MgCl2•6H2O,含有MgSO4、FeCl2等杂质.②四种化合物的溶解度(S)随温度(T)变化曲线如图所示.
回答下列问题:
(1)加速卤块在H2O2溶液中溶解的措施有:将卤块粉碎或加热等(写出一条即可).
(2)加入MgO的作用是调节溶液的pH,使Fe3+沉淀完全;滤渣的主要成分为BaSO4和Fe(OH)3.
(3)向滤液中加入NaClO3饱和溶液后,发生反应的化学方程式为MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,再进一步制取Mg(ClO3)2•6H2O的实验步骤依次为①蒸发结晶;②趁热过滤;③冷却结晶;④过滤、洗涤.
(4)产品中Mg(ClO3)2•6H2O含量的测定:
步骤1:准确称量3.50g产品配成100mL溶液.
步骤2:取10.00mL于锥形瓶中,加入10.00mL稀硫酸和20.00mL 1.000mol•L-1的FeSO4溶液,微热.
步骤3:冷却至室温,用0.1000mol•L-1 K2Cr2O7溶液滴定剩余的Fe2+至终点,此过程中反应的离子方程式为:Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O.
步骤4:将步骤2、3重复两次,计算得平均消耗K2Cr2O7溶液15.00mL.
①写出步骤2中发生反应的离子方程式(还原产物为Cl-):ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O;
②产品中Mg(ClO3)2•6H2O的质量分数为(保留一位小数)78.3%.
分析 卤块的成分有MgCl2•6H2O、MgSO4、FeCl2,加入双氧水之后,亚铁离子可以被氧化为三价铁离子,再向混合物中加入氯化钡溶液,可以将硫酸根离子转化为硫酸钡沉淀,加入氧化镁,调节pH,可以促进铁离子的水解,将铁离子转化为氢氧化铁而除去,过滤,得到的滤液是氯化镁,可以根据溶解度受温度的影响情况来获得要制取的物质,
(1)温度、固体颗粒大小、物质的浓度等会影响反应速率;
(2)MgO的作用是调节溶液的pH,使杂质Fe3+形成沉淀完全除去,根据示意图可知滤渣的主要成分为BaSO4和Fe(OH)3;
(3)滤液中含有氯化镁,加入NaClO3饱和溶液后,生成Mg(ClO3)2和氯化钠,利用NaCl、Mg(ClO3)2的溶解度与温度的关系,将溶液蒸发浓缩结晶、趁热过滤、冷却结晶,最后过滤、洗涤,得到Mg(ClO3)2•6H2O;
(4)①氯酸根离子具有氧化性,可以将亚铁离子氧化为正三价;
②根据ClO3-~6Fe2+,Cr2O72-~6Fe2+,根据各个质物之间的关系式可计算百分含量.
解答 解:(1)影响化学反应速率的因素有:升高温度、将固体粉碎成细小的颗粒、增加物质的浓度等,因此加速卤块在KMnO4溶液中溶解的措施有:将卤块粉碎或加热等;
故答案为:将卤块粉碎或加热等;
(2)金属氧化物MgO能与酸反应产生盐和水.所以加入MgO的作用是调节溶液的pH,使杂质Fe3+形成沉淀完全除去,根据示意图可知滤渣的主要成分为BaSO4和Fe(OH)3,
故答案为:调节溶液的pH,使Fe3+沉淀完全;BaSO4和Fe(OH)3;
(3)滤液中含有氯化镁,加入NaClO3饱和溶液后,生成Mg(ClO3)2和氯化钠,氯化钠溶解度小,析出,反应为:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,利用NaCl、Mg(ClO3)2的溶解度与温度的关系将溶液蒸发浓缩、趁热过滤、冷却结晶,最后过滤、洗涤,就得到Mg(ClO3)2•6H2O;
故答案为:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓;趁热过滤;冷却结晶;
(4)①氯酸根离子具有氧化性,可以将亚铁离子氧化为正三价,化学方程式为:ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O;
故答案为:ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O;
②根据化学方程式:ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O以及Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,可以得出:ClO3-~6Fe2+,Cr2O72-~6Fe2+,用0.100mol•L-1 K2Cr2O7溶液滴定至终点过程可以得出剩余的亚铁离子的物质的量为:0.100mol•L-1×0.015L×6=0.009mol,和氯酸根离子反应的亚铁离子的物质的量为:20×10-3L×1.000mol•L-1-0.009mol=0.011mol,氯酸根离子的物质的量为:$\frac{1}{6}$×0.011mol,产品中Mg(ClO3)2•6H2O的质量分数:($\frac{1}{2}$×$\frac{1}{6}$×0.011×299g/mol)×10×$\frac{1}{3.5}$×100%=78.3%;
故答案为:78.3%.
点评 本题考查实验制备方案,涉及对操作的分析评价、物质的分离提纯、离子方程式书写、物质含量测定、氧化还原反应滴定等,是对学生综合能力的考查,难度中等.

| A. | 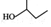 的名称为2-甲基-1-丙醇 的名称为2-甲基-1-丙醇 | B. | 氯乙烯和聚乙烯均能发生加成反应 | ||
| C. | C3H2Cl6 有4种同分异构体 | D. | C2H4和C4H8一定是同系物 |
| A. | 稀硫酸:Fe2+、Cl-、NO3-、K+ | B. | 澄清溶液:MnO4-、S2-、Na+、H+ | ||
| C. | 食盐水:K+、NO3-、SO42-、Mg2+ | D. | pH=7的溶液:Na+、HCO3-、SO42-、K+ |
| A. | 乙烯的结构简式为CH2CH2 | |
| B. | 光照条件下1mol CH4与3mol Cl2反应可制得1mol CHCl3 | |
| C. | 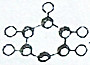 为苯分子的比例模型 为苯分子的比例模型 | |
| D. | HC≡C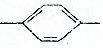 CH═CHCH3中所有碳原子有可能都在同一个平面内 CH═CHCH3中所有碳原子有可能都在同一个平面内 |

已知:浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+、Ca2+、Pb2+等其他金属离子.PbO2的氧化性大于MnO2.
有关金属离子的半径、形成氢氧化物沉淀时的pH见下表,阳离子吸附剂吸附金属离子的效果见图2.
| 离子 | 离子半径(pm) | 开始沉淀 时的pH | 完全沉淀 时的pH |
| Fe2+ | 74 | 7.6 | 9.7 |
| Fe3+ | 64 | 2.7 | 3.7 |
| Al3+ | 50 | 3.8 | 4.7 |
| Mn2+ | 80 | 8.3 | 9.8 |
| Pb2+ | 121 | 8.0 | 8.8 |
| Ca2+ | 99 | - | - |
(1)写出浸出过程中生成Mn2+反应的化学方程式SO2+MnO2=MnSO4.
(2)氧化过程中主要反应的离子方程式2Fe2++MnO2+4H+=2Fe3++Mn2++2H2O.
(3)在氧化后的液体中加入石灰浆,用于调节pH值,此处调节pH值用到的仪器是pH计,应调节至4.7≤pH<8.3范围.
(4)阳离子吸附剂可用于除去杂质金属离子.请依据图、表信息回答,决定阳离子吸附剂吸附效果的因素有吸附时间、金属离子半径、金属离子电荷等;吸附步骤除去的主要离子为:Pb2+、Ca2+.
(5)CaSO4是一种微溶物质,已知Ksp(CaSO4)=9.10×10-7.现将c mol•L-1 CaCl2溶液与2.00×10-2mol•L-1 Na2SO4溶液等体积混合(忽略体积的变化),则生成沉淀时,c的最小值是1.82×10-5..
| A. | 氢键、分子间作用力、离子键、共价键都是微粒间的作用力,其中氢键、离子键和共价键是化学键 | |
| B. | 石墨烯是一种从石墨材料中用“撕裂”方法剥离出的单层碳原子面材料,用这种方法从C60、金刚石等中获得“只有一层碳原子厚的碳薄片”也必将成为研究方向 | |
| C. | H、S、O三种元素组成的物质的水溶液与Na、S、O三种元素组成的物质的水溶液混合可能会观察到浑浊现象 | |
| D. | 测定中和热的实验中,应将酸、碱溶液一次性倒入量热装置中,并不断搅拌,待温度稳定后记下温度 |
| A. | 体积比为8:11 | B. | 密度之比为1:1 | ||
| C. | 物质的量之比为11:8 | D. | 原子个数之比为12:11 |
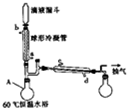 过氧乙酸常用作氧化剂和灭菌剂,实验室合成过氧乙酸并测定其含量的相关步骤如下:
过氧乙酸常用作氧化剂和灭菌剂,实验室合成过氧乙酸并测定其含量的相关步骤如下: