题目内容
下列实验操作及现象与结论正确的一组是( )
| 实验操作 | 实验现象 | 实验结论 | |
| A | 适量二氧化碳通入氯化钙溶液中 | 产生白色沉淀 | 碳酸的酸性比盐酸弱 |
| B | 二氧化硫通入石蕊溶液中 | 溶液先变红后褪色 | 二氧化硫有酸性和漂白性 |
| C | 取少量无色溶液,再加少量的四 氯化碳,振荡、静置 | 溶液分层,下层为无色 | 原无色溶液中一定不含碘离子 |
| D | 蔗糖中滴入浓硫酸和几滴水,并用玻璃棒搅拌 | 蔗糖变黑,体积膨胀,并放出刺激气味的气体 | 浓硫酸有脱水性和强氧化性 |
| A、A | B、B | C、C | D、D |
考点:化学实验方案的评价
专题:实验评价题
分析:A.二氧化碳与氯化钙不反应;
B.酸溶液能使紫色石蕊试剂变红,但二氧化硫不能使之褪色;
C.碘离子不易溶于四氯化碳;
D.蔗糖中含C、H、O三种元素,浓硫酸时其脱水后,碳与浓硫酸发生氧化还原反应.
B.酸溶液能使紫色石蕊试剂变红,但二氧化硫不能使之褪色;
C.碘离子不易溶于四氯化碳;
D.蔗糖中含C、H、O三种元素,浓硫酸时其脱水后,碳与浓硫酸发生氧化还原反应.
解答:
解:A.二氧化碳通入氯化钙溶液中,不反应无沉淀生成,故A错误;
B.二氧化硫溶于水,二氧化硫和水反应生成亚硫酸,溶液显酸性,因此可使紫色石蕊试液变红色,但不能使之褪色,故B错误;
C.碘离子不易溶于四氯化碳,原溶液可能含有碘离子,故C错误;
D.蔗糖中含C、H、O三种元素,浓硫酸时其脱水后,碳与浓硫酸发生氧化还原反应,则向蔗糖中加入浓硫酸,蔗糖变黑并有刺激性气味气体生成,说明浓硫酸具有脱水性和强氧化性,故D正确.
故选D.
B.二氧化硫溶于水,二氧化硫和水反应生成亚硫酸,溶液显酸性,因此可使紫色石蕊试液变红色,但不能使之褪色,故B错误;
C.碘离子不易溶于四氯化碳,原溶液可能含有碘离子,故C错误;
D.蔗糖中含C、H、O三种元素,浓硫酸时其脱水后,碳与浓硫酸发生氧化还原反应,则向蔗糖中加入浓硫酸,蔗糖变黑并有刺激性气味气体生成,说明浓硫酸具有脱水性和强氧化性,故D正确.
故选D.
点评:本题考查化学实验方案的评价,为高频考点,涉及物质性质及检验等,侧重实验基本操作和实验原理的考查,题目难度不大.

练习册系列答案
相关题目
下列有关实验原理或操作正确的是( )
| A、实验室将Na2SO3溶液直接加热蒸发结晶可得到Na2SO3晶体 |
| B、用湿润的pH试纸来检验溶液的pH值 |
| C、用KSCN溶液检验硫酸亚铁溶液是否氧化变质 |
| D、用四氯化碳萃取溴的苯溶液中的溴 |
如图是分离乙酸乙醋、乙酸和乙醇混合物的实验操作流程图:
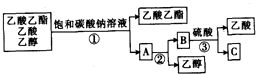
上述实验过程中所涉及的三次分离操作依次是( )

上述实验过程中所涉及的三次分离操作依次是( )
| A、①蒸馏 ②过滤 ③分液 |
| B、①分液 ②蒸馏 ③蒸馏 |
| C、①蒸馏 ②分液 ③分液 |
| D、①分液 ②蒸馏 ③结晶、过滤 |
化学与生产、生活息息相关,下列说法不正确的是( )
| A、自行车钢架生锈主要是电化学腐蚀所致 |
| B、玻璃容器内壁中沉积的CaSO4可用Na2CO3溶液浸泡后再加酸除去 |
| C、在工业合成氨中温度越高反应速度越快,越有利于提高N2的转化率 |
| D、生活中使用明矾净水,是利用了Al3+水解生成的Al(OH)3胶体吸附杂质的原理 |
X、Y、Z、W是原子序数依次增大的短周期元素,且互不同族;其中只有两种为金属;X原子的最外层电子数与次外层电子数相等;X与W、Y与Z这两对原子的最外层电子数之和均为9.单质Y和W都可与浓的NaOH溶液反应.下列说法不正确的是( )
| A、原子半径:Y>Z>W |
| B、非金属性最强的元素为W |
| C、Y的最高价氧化物对应的水化物不是强碱 |
| D、XW2分子中各原子最外层电子均达到电子结构 |
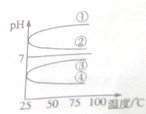 A、B、C、D、E五种溶液分别是NaOH、NH3?H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验:
A、B、C、D、E五种溶液分别是NaOH、NH3?H2O、CH3COOH、HCl、NH4HSO4中的一种.常温下进行下列实验: