题目内容
现有四种短周期元素X、Y、Z、W,其中:
①X、W原子的电子层数与最外层电子数之比分别为3:2和1:3
②Y原子是元素周期表中原子半径最小的
③Z是形成化合物种类最多的元素
④w的单质通常为气态
回答下列问题:
(1)W元素在周期表中的位置是 .
(2)上述四种元素中所能组成的含有非极性共价键的化合物的分子式 (填其中一种即可).
(3)向含1mol Na2SiO3的溶液中缓慢通入2mol的ZO2,反应的离子方程式是 .
(4)由Y、Z、W元素中的两种或三种可以组成多种分子,其中含有10个电子的分子是 (填化学式).
(5)已知X在空气中燃烧时,除了生成氧化物外,还可以生成一种氮化物.而在元素周期表中存在一种对角线规则,即某元素与它左上角的元素的性质十分相似.试写出元素X的左上角元素M在空气中燃烧的方程式: .
①X、W原子的电子层数与最外层电子数之比分别为3:2和1:3
②Y原子是元素周期表中原子半径最小的
③Z是形成化合物种类最多的元素
④w的单质通常为气态
回答下列问题:
(1)W元素在周期表中的位置是
(2)上述四种元素中所能组成的含有非极性共价键的化合物的分子式
(3)向含1mol Na2SiO3的溶液中缓慢通入2mol的ZO2,反应的离子方程式是
(4)由Y、Z、W元素中的两种或三种可以组成多种分子,其中含有10个电子的分子是
(5)已知X在空气中燃烧时,除了生成氧化物外,还可以生成一种氮化物.而在元素周期表中存在一种对角线规则,即某元素与它左上角的元素的性质十分相似.试写出元素X的左上角元素M在空气中燃烧的方程式:
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:四种短周期元素X、Y、Z、W,由①X、W原子的电子层数与最外层电子数之比分别为3:2和 1:3,则X有3个电子层,最外层电子数为2,即X为Mg,W有2个电子层,最外层电子数为6,即W为O元素;
由②Y原子是元素周期表中原子半径最小的,则Y为H元素;
由③Z是形成化合物种类最多的元素,则Z为C元素;
④W的单质通常为气态,该单质为氧气,与推断一致,
故X为Mg、Y为H元素、Z为C元素、W为O元素,
据此进行解答.
由②Y原子是元素周期表中原子半径最小的,则Y为H元素;
由③Z是形成化合物种类最多的元素,则Z为C元素;
④W的单质通常为气态,该单质为氧气,与推断一致,
故X为Mg、Y为H元素、Z为C元素、W为O元素,
据此进行解答.
解答:
解:四种短周期元素X、Y、Z、W,由①X、W原子的电子层数与最外层电子数之比分别为3:2和 1:3,则X有3个电子层,最外层电子数为2,即X为Mg,W有2个电子层,最外层电子数为6,即W为O元素;
由②Y原子是元素周期表中原子半径最小的,则Y为H元素;
由③Z是形成化合物种类最多的元素,则Z为C元素;
④W的单质通常为气态,该单质为氧气,与推断一致,
故X为Mg、Y为H元素、Z为C元素、W为O元素,
(1)W为O元素,O原子核电荷数为8,最外层含有6个电子,氧元素在周期表中的位置为:第二周期第ⅥA族,故答案为:第二周期第ⅥA族;
(2)Mg、H、C、O四种元素中所能组成的含有非极性共价键的化合物的分子式有:H2O2或C2H6等,故答案为:H2O2(或C2H6等);
(3)Z为C元素,因碳酸的酸性大于硅酸的酸性,则二氧化碳足量生成碳酸氢钠,反应的离子反应为:2CO2+2H2O+SiO32-═2HCO3-+H2SiO3↓,
故答案为:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3-;
(4)Y为H元素、Z为C元素、W为O元素,形成的含有10个电子的物质有:H2O或CH4等,故答案为:H2O(或CH4);
(5)X为Mg元素,左上角元素M为Li,类比镁与氧气的反应,Li在空气中燃烧的方程式有:4Li+O2═2Li2O、6Li+N2═2Li3N,
故答案为:4Li+O2═2Li2O、6Li+N2═2Li3N.
由②Y原子是元素周期表中原子半径最小的,则Y为H元素;
由③Z是形成化合物种类最多的元素,则Z为C元素;
④W的单质通常为气态,该单质为氧气,与推断一致,
故X为Mg、Y为H元素、Z为C元素、W为O元素,
(1)W为O元素,O原子核电荷数为8,最外层含有6个电子,氧元素在周期表中的位置为:第二周期第ⅥA族,故答案为:第二周期第ⅥA族;
(2)Mg、H、C、O四种元素中所能组成的含有非极性共价键的化合物的分子式有:H2O2或C2H6等,故答案为:H2O2(或C2H6等);
(3)Z为C元素,因碳酸的酸性大于硅酸的酸性,则二氧化碳足量生成碳酸氢钠,反应的离子反应为:2CO2+2H2O+SiO32-═2HCO3-+H2SiO3↓,
故答案为:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3-;
(4)Y为H元素、Z为C元素、W为O元素,形成的含有10个电子的物质有:H2O或CH4等,故答案为:H2O(或CH4);
(5)X为Mg元素,左上角元素M为Li,类比镁与氧气的反应,Li在空气中燃烧的方程式有:4Li+O2═2Li2O、6Li+N2═2Li3N,
故答案为:4Li+O2═2Li2O、6Li+N2═2Li3N.
点评:本题考查位置、结构、性质的关系及应用,题目难度中等,明确元素的推断是解答本题的关键,熟悉元素及其单质、化合物的性质即可解答,注意掌握原子结构与元素周期表、元素周期律的关系.

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案
相关题目
下列离子方程式书写正确的是( )
| A、金属钠溶于水:2Na+2H2O=2Na++2OH-+H2↑ |
| B、Cl2与H2O反应:Cl2+H2O=2H++Cl-+ClO- |
| C、硫酸铜溶液与氢氧化钡溶液反应:Cu2++2OH-=Cu(OH)2↓ |
| D、铁与稀硫酸反应:2Fe+6H+=2Fe3++3H2↑ |
对于3Fe(s)+4H2O(g)
Fe3O4(s)+4H2(g),反应的化学平衡常数的表达式为( )
| ||
A、K=
| ||
B、K=
| ||
C、K=
| ||
D、K=
|
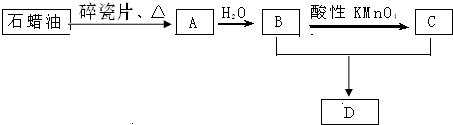
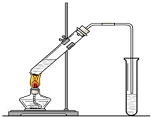
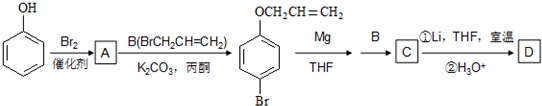
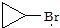 是化合物B的一种同分异构体,用1H核磁共振谱可以证明该化合物中有
是化合物B的一种同分异构体,用1H核磁共振谱可以证明该化合物中有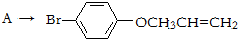 的有机反应类型:
的有机反应类型: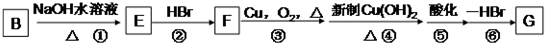
 实验设计:
实验设计: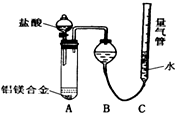 铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定已知质量的铝镁合金(设不含其它元素)中镁的质量分数,设计下列三种不同实验方案(所加试剂均为足量)进行探究.填写下列空白.
铝镁合金已成为轮船制造、化工生产等行业的重要材料.研究性学习小组的三位同学,为测定已知质量的铝镁合金(设不含其它元素)中镁的质量分数,设计下列三种不同实验方案(所加试剂均为足量)进行探究.填写下列空白.