题目内容
如图各个装置中能组成原电池的是( )
A、 稀硫酸 |
B、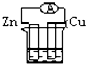 CuSO4溶液 |
C、 酒精溶液 |
D、 稀硫酸 稀硫酸 |
考点:原电池和电解池的工作原理
专题:电化学专题
分析:原电池的构成条件是:①有两个活泼性不同的电极,②将电极插入电解质溶液中,③两电极间构成闭合回路,④能自发的进行氧化还原反应,据此解答.
解答:
解:A.该装置两个电极材料相同,所以不能构成原电池,故A错误;
B.该装置符合原电池构成条件,所以能构成原电池,故B正确;
C.该装置不能自发的进行氧化还原反应,所以不能构成原电池,故C错误;
D.该装置不能形成闭合回路,所以不能构成原电池,故D错误;
故选B.
B.该装置符合原电池构成条件,所以能构成原电池,故B正确;
C.该装置不能自发的进行氧化还原反应,所以不能构成原电池,故C错误;
D.该装置不能形成闭合回路,所以不能构成原电池,故D错误;
故选B.
点评:本题考查了原电池的判断,知道原电池构成条件即可解答,这几个条件必须同时具备,缺一不可.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、标准状况下,22.4L NO与11.2L O2充分反应后得到的气体分子数为NA |
| B、一定条件下,6.4g铜与过量的硫反应,转移电子数目为0.2NA |
| C、16.9 g过氧化钡(BaO2)固体中阴、阳离子总数约为0.2NA |
| D、常温下,1L 1 mol﹒L-l的CH3COOH溶液中,所含溶质分子数为NA |
下列离子方程式正确的是( )
| A、Cl2通入水中:Cl2+H2O=2H++Cl-+ClO- |
| B、Ca(HCO3)2溶液与少量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O |
| C、氧化亚铁溶于稀硝酸:3Fe2++4H++NO3-═3Fe3++NO↑+3H2O |
| D、氢氧化铁与足量的氢碘酸溶液反应:Fe(OH)3+3H+=Fe3++3H2O |
在下列各组离子中,能大量共存的是( )
| A、Al3+、NH4+、AlO2-、Cl- |
| B、Cu2+、Fe2+、ClO-、SO42- |
| C、Na+、Ca2+、HCO3-、OH- |
| D、Cu2+、Fe3+、Cl-、NO3- |
实验室不需要用棕色试剂瓶保存的试剂是( )
| A、浓硝酸 | B、硝酸银 |
| C、氯水 | D、浓硫酸 |
已知Co2O3在酸性溶液中易被还原成Co2+,Co2O3、Cl2、FeCl3、I2氧化性依次减弱.下列反应在水溶液中不可能发生的是( )
| A、Co2O3+6 HCl=2CoCl2+Cl2↑+3H2O |
| B、Cl2+FeI2=FeCl2+I2 |
| C、3 Cl2+6 FeI2=2FeCl3+4 FeI3 |
| D、2Fe3++2I-=2Fe2++I2 |
下列有关高分子材料的表述不正确的是( )
| A、合成高分子材料都很难降解 |
| B、塑料、合成纤维、黏合剂、涂料等都是合成高分子材料 |
| C、棉花、羊毛、天然橡胶等属于天然高分子材料 |
| D、线型和体型高分子材料在溶解性、热塑性和热固性等方面有较大的区别 |