题目内容
体积相同的甲乙两个容器中,分别都充有等物质的量的SO2和O2,在相同温度下发生反应:2SO2+O2?2SO3,并达到平衡.在这过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为P%,则乙容器的转化率( )
| A、等于P% | B、无法判断 |
| C、小于P% | D、大于P% |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:2SO2+O2?2SO3该反应是气体体积减小的反应,甲容器保持体积不变,乙容器保持压强不变,过程中乙容器中压强大于甲容器,反应速率大于甲,相当于对甲容器平衡增大压强,平衡正向进行,乙容器中二氧化硫转化率大于甲容器.
解答:
解:甲容器保持体积不变,乙容器保持压强不变,过程中乙容器中压强大于甲容器,反应速率大于甲,相当于对甲容器平衡增大压强,平衡正向进行,乙容器中二氧化硫转化率大于甲容器,乙容器中SO2的转化率大于P%,故D正确,故选D.
点评:本题考查了化学平衡的影响因素分析判断,恒温恒容、恒温恒压容器的变化特征,题目难度中等,掌握分析方法是关键.

练习册系列答案
相关题目
已知H2+Cl2
2HCl,一定条件下的密闭容器中,某H2和Cl2的混合气体15g含有3.612×1023个分子,充分反应后,下列说法正确的是( )
| ||
| A、反应后所得气体比相同状况下空气的密度大 |
| B、反应后所得气体在标准状况下的体积为6.72L |
| C、反应后所得气体中H原子和Cl原子的物质的量之比为2:1 |
| D、反应后所得气体可被200mL 1.0mol/L NaOH溶液完全吸收 |
在标准状况下,有二氧化碳和氯化氢混合气体2.24L.用100mL氢氧化钠溶液恰好完全吸收生成正盐,则氢氧化钠溶液的浓度不可能是( )
| A、1.2mol?L-1 |
| B、1.5mol?L-1 |
| C、1.8mol?L-1 |
| D、2.5mol?L-1 |
已知298K,101kPa时,2SO2(g)+O2(g)?2SO3(g)△H=-197kJ?mol-1.在相同温度和压强下,向密闭容器中通入2mol SO2和1mol O2,达到平衡时,放出热量为Q1,向另一个体积相同的容器中通入1mol SO2,0.5mol O2和1mol SO3,达到平衡时放出热量为Q2,则下列关系正确的是( )
| A、Q2<Q1<197 kJ?mol-1 |
| B、2Q2=Q1=197 kJ?mol-1 |
| C、Q1<Q2<197 kJ?mol-1 |
| D、2Q2=Q1<197 kJ?mol-1 |
下列说法正确的是( )
| A、由极性键构成的分子全都是极性分子 |
| B、含有非极性键的分子不一定是非极性分子 |
| C、极性分子一定含有极性键,非极性分子一定含有非极性键 |
| D、以极性键结合的双原子分子,可能是非极性分子 |
在Na2S溶液中c(Na+)与c(S2-)的比值是( )
| A、大于2 | B、小于2 |
| C、2 | D、1/2 |
下列物质中既能跟某些金属单质或非金属单质反应,又能跟某些金属氧化物或非金属氧化物直接反应的是( )
| A、CO |
| B、AgNO3 |
| C、Al2O3 |
| D、NaOH溶液 |
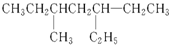 :
: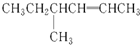 :
: :
: :
:
 中官能团的名称:
中官能团的名称: 中官能团的结构简式:
中官能团的结构简式: