题目内容
黑火药爆炸时发生多种化学反应,其中主要化学反应方程式为:2KNO3+3C+S═K2S+N2↑+3CO2↑
(1)上述反应中,原子半径最小的元素其原子结构示意图为 ;
(2)上述反应中,每生成1mol氧化产物转移电子的物质的量为 mol;
(3)收集黑吠药爆炸后的烟尘和气体产物,分别与酸性高锰酸钾溶液反应,均能使溶液紫红色退去.
①烟尘中能使酸性高锰酸钾溶液褪色的物质的化学式是 .
②气体产物与酸性高锰酸钾溶液反应的离子方程式 .
(1)上述反应中,原子半径最小的元素其原子结构示意图为
(2)上述反应中,每生成1mol氧化产物转移电子的物质的量为
(3)收集黑吠药爆炸后的烟尘和气体产物,分别与酸性高锰酸钾溶液反应,均能使溶液紫红色退去.
①烟尘中能使酸性高锰酸钾溶液褪色的物质的化学式是
②气体产物与酸性高锰酸钾溶液反应的离子方程式
考点:氧化还原反应,氧化还原反应的电子转移数目计算
专题:氧化还原反应专题
分析:(1)电子层越少原子半径越小,同周期原子序数大的半径小,则原子半径最小的元素为O;
(2)2KNO3+3C+S═K2S+N2↑+3CO2↑中,N、S元素的化合价降低,C元素的化合价升高;
(3)①产物烟尘中只有K2S具有还原性,能与高锰酸钾发生氧化还原反应;
②气体产物中可能有二氧化硫,具有还原性,能被酸性高锰酸钾溶液氧化.
(2)2KNO3+3C+S═K2S+N2↑+3CO2↑中,N、S元素的化合价降低,C元素的化合价升高;
(3)①产物烟尘中只有K2S具有还原性,能与高锰酸钾发生氧化还原反应;
②气体产物中可能有二氧化硫,具有还原性,能被酸性高锰酸钾溶液氧化.
解答:
解:(1)根据元素周期律知,原子半径最小的元素是O元素,其原子结构示意图为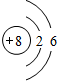 ,故答案为:
,故答案为: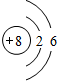 ;
;
(2)2KNO3+3C+S═K2S+N2↑+3CO2↑中,N、S元素的化合价降低,C元素的化合价升高,则二氧化碳为氧化产物,由C元素的化合价变化可知每生成1mol氧化产物转移电子的物质的量为1mol×(4-0)=4mol,故答案为:4;
(3)收集黑火药爆炸后的烟尘和气体产物,分别与酸性高锰酸钾溶液反应,均能使溶液紫红色退去,说明其烟尘和气体中含有还原性物质,
①烟尘中能使酸性高锰酸钾溶液褪色的物质必须具有还原性,所以是K2S,故答案为:K2S;
②二氧化硫具有还原性,能被酸性高锰酸钾溶液氧化生成硫酸根离子,高锰酸根离子被还原生成锰离子,离子方程式为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,
故答案为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+.
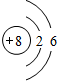 ,故答案为:
,故答案为: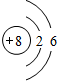 ;
;(2)2KNO3+3C+S═K2S+N2↑+3CO2↑中,N、S元素的化合价降低,C元素的化合价升高,则二氧化碳为氧化产物,由C元素的化合价变化可知每生成1mol氧化产物转移电子的物质的量为1mol×(4-0)=4mol,故答案为:4;
(3)收集黑火药爆炸后的烟尘和气体产物,分别与酸性高锰酸钾溶液反应,均能使溶液紫红色退去,说明其烟尘和气体中含有还原性物质,
①烟尘中能使酸性高锰酸钾溶液褪色的物质必须具有还原性,所以是K2S,故答案为:K2S;
②二氧化硫具有还原性,能被酸性高锰酸钾溶液氧化生成硫酸根离子,高锰酸根离子被还原生成锰离子,离子方程式为5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+,
故答案为:5SO2+2MnO4-+2H2O=5SO42-+2Mn2++4H+.
点评:本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重氧化还原反应基本概念及转移电子的考查,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
有甲、乙两瓶酸溶液,已知甲瓶溶液的pH=4,乙瓶溶液的pH=6,现将甲瓶溶液取出少量用蒸馏水稀释至100倍体积(温度不变),则下列叙述中正确的是( )
| A、稀释后两溶液的pH相等 |
| B、稀释后甲瓶溶液的pH一定小于乙溶液 |
| C、稀释后甲瓶溶液的pH小于或等于乙溶液 |
| D、稀释后甲瓶溶液的pH一定大于乙溶液 |

 硫单质及其化合物在工农业生产中有着重要的应用.
硫单质及其化合物在工农业生产中有着重要的应用.