题目内容
如表是元素周期表的一部分,根据①~⑩在周期表中的位置,用元素符号或化学式回答下列问题:

(1)金属性最强的元素是 ,最容易与H2反应单质是 .
(2)⑤位于周期表中第 周期, 族;其原子结构示意图为 .
(3)最高价氧化物所对应的水化物酸性最强的是 (填化学式).
(4)②与⑧形成的化合物属于 (填“离子化合物”或“共价化合物”).
(5)最高价氧化物既能与酸反应又能与碱反应的是 (填化学式).
(6)③和⑦对应的氢化物较稳定的是 (填化学式).
(7)⑤和⑥的原子半径较大是 ,⑤和⑥的最高价氧化物对应水化物的碱性较强的是 (填化学式).
(8)用电子式表示⑤和⑨元素形成的化合物的形成过程 .

(1)金属性最强的元素是
(2)⑤位于周期表中第
(3)最高价氧化物所对应的水化物酸性最强的是
(4)②与⑧形成的化合物属于
(5)最高价氧化物既能与酸反应又能与碱反应的是
(6)③和⑦对应的氢化物较稳定的是
(7)⑤和⑥的原子半径较大是
(8)用电子式表示⑤和⑨元素形成的化合物的形成过程
考点:位置结构性质的相互关系应用
专题:元素周期律与元素周期表专题
分析:由元素在周期表中的位置可知①为H元素,②为C元素,③为N元素,④为F元素,⑤为Na元素,⑥为Al元素,⑦为P元素,⑧为S元素,⑨为Cl元素,⑩为Ar元素,
同周期元素从左到右元素的金属性逐渐减弱,非金属性逐渐增强,同主族元素从上到下,元素的金属性逐渐增强,非金属性逐渐减弱,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,金属性越强,对应的最高价氧化物的碱性越强,结合元素性质的递变规律解答该题.
同周期元素从左到右元素的金属性逐渐减弱,非金属性逐渐增强,同主族元素从上到下,元素的金属性逐渐增强,非金属性逐渐减弱,元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,金属性越强,对应的最高价氧化物的碱性越强,结合元素性质的递变规律解答该题.
解答:
解:由元素在周期表中的位置可知①为H元素,②为C元素,③为N元素,④为F元素,⑤为Na元素,⑥为Al元素,⑦为P元素,⑧为S元素,⑨为Cl元素,⑩为Ar元素,(1)同周期元素从左到右元素的金属性逐渐减弱,非金属性逐渐增强,同主族元素从上到下,元素的金属性逐渐增强,非金属性逐渐减弱,则金属性最强的为Na,非金属性最强的为F,元素的非金属性越强,对应的单质越易与氢气发生反应,则最容易与H2反应单质是F2,
故答案为:Na;F2;
(2)⑤位于周期表中第三周期,ⅠA 族,原子核外有3个电子层,最外层电子数为1,则原子结构示意图为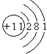 ,
,
故答案为:三;ⅠA; ;
;
(3)最高价氧化物所对应的水化物酸性最强的是HClO4,故答案为:HClO4;
(4)②与⑧形成的化合物为CS2,为共价化合物,故答案为:共价化合物;
(5)最高价氧化物既能与酸反应又能与碱反应的是Al2O3,故答案为:Al2O3;
(6)非金属性N>P,元素的非金属性越强,对应的氢化物越稳定,故答案为:NH3;
(7)同周期元素从左到右元素的原子半径逐渐减小,则原子半径较大的为Na,金属性Na>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性较强的为NaOH,
故答案为:Na;NaOH;
(8)⑤和⑨元素形成的化合物为NaCl,用电子表示形成过程为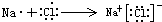 ,故答案为:
,故答案为: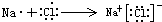 .
.
故答案为:Na;F2;
(2)⑤位于周期表中第三周期,ⅠA 族,原子核外有3个电子层,最外层电子数为1,则原子结构示意图为
 ,
,故答案为:三;ⅠA;
 ;
;(3)最高价氧化物所对应的水化物酸性最强的是HClO4,故答案为:HClO4;
(4)②与⑧形成的化合物为CS2,为共价化合物,故答案为:共价化合物;
(5)最高价氧化物既能与酸反应又能与碱反应的是Al2O3,故答案为:Al2O3;
(6)非金属性N>P,元素的非金属性越强,对应的氢化物越稳定,故答案为:NH3;
(7)同周期元素从左到右元素的原子半径逐渐减小,则原子半径较大的为Na,金属性Na>Al,元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,则碱性较强的为NaOH,
故答案为:Na;NaOH;
(8)⑤和⑨元素形成的化合物为NaCl,用电子表示形成过程为
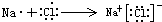 ,故答案为:
,故答案为: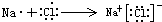 .
.
点评:本题考查位置结构性质等知识,题目难度不大,根据元素在周期表中的物质可推断出元素的种类,题中侧重于周期律的应用,学习中注意积累相关知识.

练习册系列答案
相关题目
下列根据实验现象所得出的结论中,正确的是( )
| A、某物质焰色反应呈黄色,结论:该物质一定是钠盐 |
| B、无色试液加入NaOH溶液,加热产生的气体使湿润的红色石蕊试纸变蓝,结论:试液中一定含有NH4+ |
| C、无色溶液中加入BaCl2溶液有白色沉淀产生,再加盐酸,沉淀不消失,结论:原溶液一定含有SO42- |
| D、无色溶液中加入稀盐酸产生无色无味气体,该气体能使澄清石灰水变浑浊,结论:原溶液一定含有CO32- |
一定条件下,可逆反应2A?B+3C,在下列四种状态中处于平衡的是( )
| A、νA=2mol/L?min (正反应速率);νA=2mol/L?min(逆反应速率) |
| B、νA=2mol/L?min(正反应速率);νC=2mol/L?min(逆反应速率) |
| C、νA=1mol/L?min (正反应速率);νB=2mol/L?min(逆反应速率) |
| D、νA=1mol/L?min(正反应速率);νC=1.5mol/L?min(逆反应速率) |
 Ⅰ.下列有关操作正确的是
Ⅰ.下列有关操作正确的是
