题目内容
20.配制500mL0.5mol/L Na2CO3溶液(1)需要Na2CO3固体的质量是多少?
(2)需要1mol/L Na2CO3溶液的体积是多少?
分析 (1)n(Na2CO3)=CV=0.5mol/L×0.5L=0.25mol,根据m=nM计算碳酸钠质量;
(2)根据溶液稀释前后溶质的物质的量不变计算浓碳酸钠体积.
解答 解:(1)n(Na2CO3)=CV=0.5mol/L×0.5L=0.25mol,m(Na2CO3)=nM=0.25mol×106g/mol=26.5g,
答:需要碳酸钠固体的质量是26.5g;
(2)溶液稀释前后溶质的物质的量不变,则浓碳酸钠体积=$\frac{0.25mol}{1mol/L}$=250mL,
答:需要1mol/L碳酸钠溶液的体积是250mL.
点评 本题考查物质的量的有关计算,明确各个物理量的关系是解本题关键,属于基础题,熟练掌握物质的量的有关公式并灵活运用.

练习册系列答案
相关题目
8.下列物质中属于化合物的是( )
| A. | N2 | B. | O2 | C. | .NaCl | D. | H2SO4溶液 |
9.卤代烃R-CH2-CH2-X中的化学键如图所示,则下列说法正确的是( )


| A. | 当该卤代烃发生取代反应时,被破坏的键是①和③ | |
| B. | 当该卤代烃发生消去反应时,被破坏的键是①和③ | |
| C. | 当该卤代烃发生水解反应时,被破坏的键② | |
| D. | 当该卤代发生消去反应时,被破坏的键是①和② |
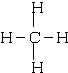 B.乙烯
B.乙烯
 2NH3
2NH3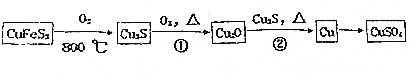
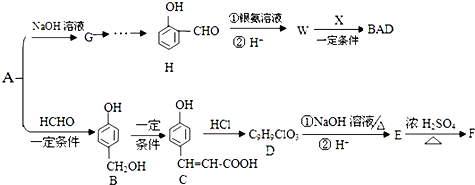
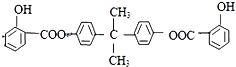
 .
. .
. .
. .
.