题目内容
12. 化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:
化学学科中的平衡理论主要包括:化学平衡、电离平衡、水解平衡和溶解平衡四种,且均符合勒夏特列原理.请回答下列问题:(1)常温下,某纯碱(Na2CO3)溶液中滴入酚酞,溶液呈红色,则该溶液呈碱性,原因是CO32-+H2O?HCO3-+OH-;(用离子方程式表示)
(2)在常温下将pH=2的盐酸10mL加水稀释到1L,则稀释后的溶液的pH值等于4;
(3)已知在H2S溶液中存在下列平衡:H2S═HS-+H+
①向H2S溶液中加入NaOH固体时,(不考虑温度变化)电离平衡向右移动,(填“左”或“右”)c(H+)减小.(填“增大”、“减小”或“不变”)
②向H2S溶液中加入NaHS固体时,电离平衡向左移动,(填“左”或“右”)c(S2-)增大.(填“增大”、“减小”或“不变”)
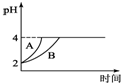
(4)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示.则图中表示醋酸溶液中pH变化曲线的是B(填“A”或“B”);设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2.则m1< m2.(选填“<”、“=”、“>”)
(5)难溶电解质在水溶液中存在溶解平衡.某MgSO4溶液里c(Mg2+)=0.002mol•L-1,如果生成Mg(OH)2沉淀,应调整溶液pH,使之大于10;(该温度下Mg(OH)2的Ksp=2×10-11)
分析 (1)碳酸钠为强碱弱酸盐,碳酸根离子水解导致溶液呈碱性;
(2)pH=2的盐酸,稀释100倍后溶液的pH变为4;
(3)①向H2S溶液中加入NaOH固体时,氢离子的浓度减小,电离平衡向右移动;
②向H2S溶液中加入NaHS固体时,硫氢根离子浓度变大,H2S═HS-+H+电离平衡向左移动,硫氢根离子的电离,c(S2-)增大;
(4)醋酸为弱酸,等pH时,醋酸浓度较大,与锌反应时,醋酸进一步电离出氢离子,则醋酸的pH变化较小,醋酸中存在电离平衡,氢离子和锌反应时促进醋酸电离,补充反应的氢离子,pH变化等量时,消耗的锌较多,以此解答;
(5)根据c(OH-)=$\sqrt{\frac{Ksp}{c(M{g}^{2+})}}$计算氢氧根离子浓度,从而确定溶液的pH,
解答 解:(1)碳酸钠为强碱弱酸盐,钠离子不水解、碳酸根离子水解导致溶液呈碱性,水解离子方程式为:CO32-+H2O?HCO3-+OH-,
故答案为:碱性;CO32-+H2O?HCO3-+OH-;
(2)pH=2的盐酸,稀释100倍后溶液的pH变为4,故答案为:4;
(3)①向H2S溶液中加入NaOH固体时,氢离子的浓度减小,电离平衡向右移动,故答案为:右;减小;
②向H2S溶液中加入NaHS固体时,硫氢根离子浓度变大,H2S═HS-+H+电离平衡向左移动,硫氢根离子的电离,c(S2-)增大,故答案为:左;增大;
(4)由于醋酸是弱电解质,与Zn反应同时,电离出H+,所以pH变化较缓慢,所以B曲线是醋酸溶液的pH变化曲线.由图知盐酸和醋酸的pH变化都是由2到4,盐酸中氢离子浓度逐渐减小,但醋酸中存在电离平衡,氢离子和锌反应时促进醋酸电离,补充反应的氢离子,所以醋酸是边反应边电离H+,故消耗的Zn多,所以m1<m2.
故答案为:B;<;
(5)0.002mol•L-1MgSO4溶液中c(Mg2+)=0.002mol/L,沉淀平衡时c(OH-)=$\sqrt{\frac{Ksp}{c(M{g}^{2+})}}$=$\sqrt{\frac{2×1{0}^{-11}}{0.002}}$mol/L=10-4 mol/L,则c(H+)=10-10 mol/L,所以溶液的pH=-lgc(H+)=10,故应调整溶液pH大于10,故答案为:10.
点评 本题考查了弱电解质的电离、盐的水解、弱电解的稀释的理解应用、溶度积有关计算、盐类水解等知识点,是高考的热点,应熟练掌握,难度中等.

| A. | K层 | B. | L层 | C. | M层 | D. | N层 |
| A. | 常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA | |
| B. | 0.5 mol O3与11.2 L O2所含的分子数一定相等 | |
| C. | 标准状况下,22.4 L的CCl4中含有的CCl4分子数为NA | |
| D. | 常温常压,22.4 L的NO2和CO2混合气体含有2NA个氧原子 |
| A. | 碳酸钠 | B. | 碳酸氢钠 | C. | 铝箔 | D. | 磁性氧化铁 |
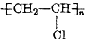 ,合成该塑料所需的原料是( )
,合成该塑料所需的原料是( )| A. | CH3Cl | B. | CH2═CHCl | C. | CH3CH2Cl | D. | CHCl═CHCl |
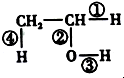 (1)在烷烃分子中,每增加一个碳原子,1mol 烷烃完全燃烧需要多消耗氧气(填字母)B.
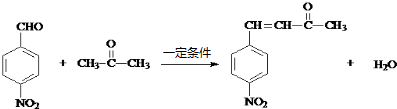
(1)在烷烃分子中,每增加一个碳原子,1mol 烷烃完全燃烧需要多消耗氧气(填字母)B.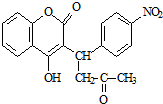 ,醋硝香豆素可以通过以下方法合成(部分反应条件省略).
,醋硝香豆素可以通过以下方法合成(部分反应条件省略).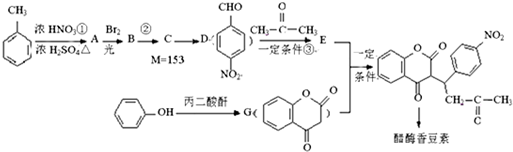
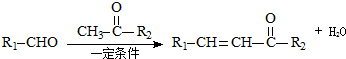
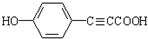
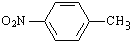 ;反应②的反应类型水解反应或取代反应.
;反应②的反应类型水解反应或取代反应.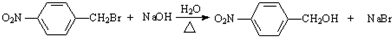 .
. .
. .
.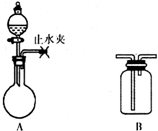 化学是一门以实验为基础的学科.
化学是一门以实验为基础的学科.