题目内容
氡是一种放射性元素,氡气吸入体内有害健康,氡的核电荷数是86,相对原子质量是222.科学家还发现某些放射性矿物分解放出的“锕射气”,是由质子数86,质量数219的原子组成,下列有关氡元素的说法正确的是( )
| A、氡气在标准状况下密度约是9.91 g?L-1 |
| B、氡气化学性质较活泼,因此对人体有害 |
| C、“锕射气”是氡的同位素 |
| D、氡原子核外有7个电子层,最外层有8个电子 |
考点:质子数、中子数、核外电子数及其相互联系,质量数与质子数、中子数之间的相互关系
专题:原子组成与结构专题
分析:A、根据标准状况密度的求算公式ρ=
计算;
B、氡为稀有气体元素,性质不活泼;
C、质子数相同,中子数不同的同种元素的不同原子互称同位素;
D、氡为第六周期元素,核外有6个电子层.
| M |
| Vm |
B、氡为稀有气体元素,性质不活泼;
C、质子数相同,中子数不同的同种元素的不同原子互称同位素;
D、氡为第六周期元素,核外有6个电子层.
解答:
解:A、在标准状况下,氡气的密度为ρ=
=
=9.91 g?L-1,故A正确;
B、氡为稀有气体元素,性质不活泼,对人体有害是因为它具有放射性,故B错误;
C、质子数相同,中子数不同的同种元素的不同原子互称同位素,氡的质子数为86,相对原子质量是222,“锕射气”的质子数86,质量数219,所以二者是同位素,故C正确;
D、氡为第六周期元素,核外有6个电子层,最外层有8个电子,故D错误;
故选AC.
| M |
| Vm |
| 222 |
| 22.4 |
B、氡为稀有气体元素,性质不活泼,对人体有害是因为它具有放射性,故B错误;
C、质子数相同,中子数不同的同种元素的不同原子互称同位素,氡的质子数为86,相对原子质量是222,“锕射气”的质子数86,质量数219,所以二者是同位素,故C正确;
D、氡为第六周期元素,核外有6个电子层,最外层有8个电子,故D错误;
故选AC.
点评:本题考查了稀有气体的原子结构和性质,侧重于基础知识的考查,题目难度不大.

练习册系列答案
 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案
相关题目
用NA代表阿伏加德罗常数的数值,下列表述正确的是( )
| A、200mL1mol/L Fe2(SO4)3溶液中,Fe3+和SO42-离子数的总和是NA |
| B、1L1mol/L CuCl2溶液中含有的Cu2+的个数为NA |
| C、0.05mol熔融的NaHSO4中含有的阳离子数为0.10NA |
| D、常温下,20L pH=12的Na2CO3溶液中含有的OH-离子数为0.2NA |
化学与生产、生活、社会密切相关.下列有关说法中不正确的是( )
| A、新能源汽车的推广与使用有助于减少光化学烟雾的产生 |
| B、针对甲型H1N1流感的扩散情况,要加强对环境、个人的消毒预防.其中消毒剂常选用含氯消毒剂、酒精、双氧水等适宜的物质 |
| C、华裔科学家高琨在光纤传输信息领域中取得突破性成就,光纤的主要成分是高纯度的单质硅 |
| D、建国60周年庆典晚会上,天安门广场燃放的焰火是某些金属元素魅力的展现 |
下列实验设计和结论正确的是( )
| A、采用加热蒸干高锰酸钾溶液的方法获得高锰酸钾晶体 |
| B、过滤时,为了加快过滤速率,可用玻璃棒在漏斗内搅拌 |
| C、某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性 |
| D、某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42- |
下列叙述正确的是( )
A、S2-的结构示意图是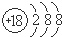 |
B、HCl的电子式为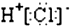 |
C、NH3的结构式为  |
| D、还原性:HCl>H2S |
下列基态原子的外围价电子排布式中,不正确的是( )
| A、3d94s2 |
| B、3d54s1 |
| C、3d64s2 |
| D、3d14s2 |
用FeCl3溶液腐蚀印刷电路板上铜箔的反应是:2Fe3++Cu=2Fe2++Cu2+,该反应的还原剂是( )
| A、Fe3+ |
| B、Cu |
| C、Fe2+ |
| D、Cu2+ |
下列表示物质组成和结构的化学用语中,不正确的是( )
| A、甲酸的结构简式:HO-CHO |
B、一氟甲烷电子式: |
| C、聚丙烯的最简式:CH2 |
| D、次氯酸的结构式:H-O-Cl |